Электроотрицательность
Между атомами в молекуле образуется определенная химическая связь, которую в современном научном мире описывает квантовая механика. Заряженные частицы в атоме взаимодействуют между собой, обеспечивая молекуле определенную устойчивость.
В зависимости от расстояния между атомами, полярности и прочности, химическая связь между атомами может быть:
Электроотрицательность — это способность атома в молекуле смещать к себе общие электронные пары. Она является необходимым показателем для описания молекулярных систем, определения типа связей в молекуле, распределения ионного заряда между взаимодействующими элементами. К факторам, которые влияют на эту величину, относятся: валентное состояние атома, степень окисления, координационное число и другие.
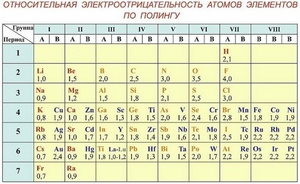
Приняв значение электроотрицательности водорода равной 2.1 произвольно и используя известные термодинамические данные, сравнивая электроотрицательность элементов с водородом, Поллинг составил первую шкалу относительных атомных электроотрицательностей.
Необходимо помнить, что электроотрицательность — величина не постоянная, а относительная, и позволяет лишь определить, в сторону какого элемента сдвигается общая электронная пара.
Помимо шкалы Поллинга, что изучают в школьном курсе химии, и которую можно найти на странице 276 учебника «Химия 8 класс» под редакцией В.В.Еремина, в мире существует около двадцати шкал определения электроотрицательности.
Таблица электроотрицательности Поллинга — справочный материал, и не всегда есть под рукой. Однако существуют общие закономерности электроотрицательности, и, зная расположение элемента в Периодической системе Д.И.Менделеева, можно косвенно оценить, в сторону какого из элементов в молекуле будет сдвигаться общая электронная пара.
Электроотрицательность химических элементов, расположенных правее, больше, чем у элементов, расположенных левее в одном периоде. Электроотрицательность элементов, расположенных выше, больше, чем у элементов, расположенных ниже в одной группе. Исходя из этих данных, самый высокий показатель у элементов, расположенных в правом верхнем углу, и самый низкий у элементов внизу слева.
По этим данным был составлен ряд электроотрицательности, в котором химические элементы расположены в порядке убывания ее величины: F, O, N, Cl, Br, S, C, P, H, Si, Mg, Li, Na.
Если таблица Поллинга под рукой, с помощью несложных арифметических действий можно определить тип связи в молекуле. Для этого нужно найти относительную электроотрицательность атомов, входящих в молекулу по таблице, и из большего значения вычесть меньшее, а по результату оценить связь.
Разность значений равна 0,5 или меньше — сила притяжения у атомов практически равна, электронное облако находится примерно посередине расстояния между атомами веществ, а связь является ковалентной неполярной. Если молекула состоит из двух одинаковых атомов, то разность значений электроотрицательностей равна 0. Атомы в молекуле с ковалентной полярной связью прочно соединены.
Разность значений составляет от 0,5 до 1,6 — сила притяжения у одного из атомов значительно больше, и он смещает общую электронную пару к себе, приобретая таким образом частичный отрицательный заряд. Атом, от которого общая электронная пара на более далеком расстоянии, приобретает частичный положительный заряд. Между атомами возникает ковалентная полярная связь. Сдвиг общей электронной пары приводит к определенному дисбалансу и молекула может вступать в определенные химические превращения.
Разность значений равна 2,0 и выше. В этом случае общая пара электронов достанется атому, чья электроотрицательность больше. Заряд у такого атома становится отрицательным, а у другого атома в молекуле за счет потери электрона — положительным. Между атомами возникает ионная связь. Ионная связь нестойкая, и молекулы легко вступают в реакции с другими атомами и полярными молекулами.
Разность значений составляет от 1,6 до 2,0. Самый сложный для определения тип связи, поскольку зависит от входящих в состав молекулы атомов. Если в молекулу входит атом металла, то связь ионная. Если в молекуле атомы металла отсутствуют — связь ковалентная полярная.
Электроотрицательность
Эле́ктроотрица́тельность (χ) — фундаментальное химическое свойство атома, количественная характеристика способности атома в молекуле смещать к себе общие электронные пары.
Современное понятие об электроотрицательности атомов было введено американским химиком Л. Полингом. Он использовал понятие электроотрицательности для объяснения того факта, что энергия гетероатомной связи A—B (A, B — символы любых химических элементов) в общем случае больше среднего геометрического значения гомоатомных связей A—A и B—B.
В настоящее время для определения электроотрицательностей атомов существует много различных методов, результаты которых хорошо согласуются друг с другом, за исключением относительно небольших различий, и во всяком случае внутренне непротиворечивы.
Первая и широко известная шкала относительных атомных электроотрицательностей Полинга охватывает значения от 0,7 для атомов франция до 4,0 для атомов фтора. Фтор — наиболее электроотрицательный элемент, за ним следует кислород (3,5) и далее азот и хлор (3,0). Активные щелочные и щёлочноземельные металлы имеют наименьшие значения электроотрицательности, лежащие в интервале 0,7—1,2, а галогены — наибольшие значения, находящиеся в интервале 4,0—2,5. Электроотрицательность типичных неметаллов находится в середине общего интервала значений и, как правило, близка к 2 или немного больше 2. Электроотрицательность водорода принята равной 2,1. Для большинства переходных металлов значения электроотрицательности лежат в интервале 1,5—2,0. Близки к 2,0 значения электроотрицательностей тяжёлых элементов главных подгрупп. Существует также несколько других шкал электроотрицательности, в основу которых положены разные свойства веществ. Но относительное расположение элементов в них примерно одинаково.
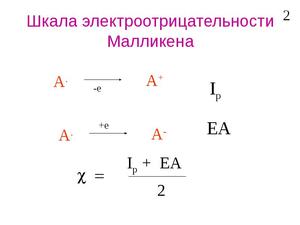
Теоретическое определение электроотрицательности было предложено американским физиком Р. Малликеном. Исходя из очевидного положения о том, что способность атома в молекуле притягивать к себе электронный заряд зависит от энергии ионизации атома и его сродства к электрону, Р. Малликен ввёл представление об электроотрицательности атома А как о средней величине энергии связи наружных электронов при ионизации валентных состояний (например, от А − до А + ) и на этой основе предложил очень простое соотношение для электроотрицательности атома:
где J1 A и εA — соответственно энергия ионизации атома и его сродство к электрону.
Помимо шкалы Малликена, описанной выше, существует более 20-ти различных других шкал электроотрицательности, среди которых шкала Л. Полинга (основана на энергии связи при образовании сложного вещества из простых), шкала Олреда-Рохова (основана на электростатической силе, действующей на внешний электрон) и др.
Строго говоря, элементу нельзя приписать постоянную электроотрицательность. Электроотрицательность атома зависит от многих факторов, в частности, от валентного состояния атома, формальной степени окисления, координационного числа, природы лигандов, составляющих окружение атома в молекулярной системе, и от некоторых других. В последнее время все чаще для характеристики электроотрицательности используют так называемую орбитальную электроотрицательность, зависящую от типа атомной орбитали, участвующей в образовании связи, и от её электронной заселённости, т. е. от того, занята атомная орбиталь неподелённой электронной парой, однократно заселена неспаренным электроном или является вакантной. Но, несмотря на известные трудности в интерпретации и определении электроотрицательности, она всегда остаётся необходимой для качественного описания и предсказания природы связей в молекулярной системе, включая энергию связи, распределение электронного заряда и степень ионности, силовую постоянную и т. д.
В период бурного развития квантовой химии как средства описания молекулярных образований (середина и вторая половина XX века) плодотворной оказался подход Л.Полинга, который в числе прочих исследований ввел собственную шкалу электроотрицательностей, в которой из «стандартных» элементов максимальную имеет фтор (

где 
Одним из наиболее развитых в настоящее время подходов является подход Сандерсона. В основу этого подхода легла идея выравнивания электроотрицательностей атомов при образовании химической связи между ними. В многочисленных исследованиях были найдены зависимости между электроотрицательностями Сандерсона и важнейшими физико-химическими свойствами неорганических соединений подавляющего большинства элементов периодической таблицы. [1] Очень плодотворной оказалась и модификация метода Сандерсона, основанная на перераспределении электроотрицательности между атомами молекулы для органических соединений. [2] [3] [4]
Электроотрицательность элементов по таблице Менделеева
Электроотрицательность — это характеристика атома, показывающая, насколько высока его способность притягивать к себе электроны. Когда химическая связь образована двумя разными элементами, электроны у одного из них всегда расположены более плотно, чем у другого. Тот атом, у которого электронная плотность выше, называется электроотрицательным, тот, у кого ниже — соответственно, электроположительным.
Как определить электроотрицательность
Существует несколько шкал, ориентируясь на которые, можно определить электроотрицательность того или иного элемента. Попробуем их перечислить:
Чтобы определить параметр «электроотрицательность» по таблице Менделеева, нужно всего лишь знать, что наиболее электроотрицательные свойства имеют те элементы, которые располагаются вверху таблицы и в правой ее части. То есть, чем выше и правее элемент находится в таблице Менделеева, тем выше у него электроотрицательность и наоборот, чем ниже и левее — тем выше у него электроположительность.
Шкала Полинга — наиболее часто используемая таблица электроотрицательности. Названа она в честь американского химика Лайнуса Полинга, который впервые ввел понятие электроотрицательности. Согласно шкале Поллинга, электроотрицательность всех имеющихся в природе элементов лежит в интервале от 0,7 (таковой она является у щелочного металла франция) до 4,0 (у газа-галогена фтора). В таблице приводятся относительные и неточные величины.
Шкала Малликена рассматривает электроотрицательность как величину энергии связи между валентными электронами. Приводятся максимально точные расчеты.
Расположение элементов в каждой из таблиц является идентичным, несмотря на то, что методы определения отличаются друг от друга, и величины тоже.
Самые высокие значения электроотрицательности
Фтор, один из галогенов — это элемент, обладающий наивысшей электроотрицательностью, а точнее — 3,98. Его химическая активность невероятно высока, настолько, что химики называют его не иначе как «все разгрызающий».
Следом за фтором идет кислород. Электроотрицательность кислорода немного пониже — 3,44, но тоже достаточно высока.
Следом за ними (спускаясь все ниже по правой части таблицы Менделеева) идут:
Большая часть неметаллов имеет электроотрицательность, колеблющуюся между значениями 2 и 3. У отличающихся наиболее высокой активностью металлов, от франция до бериллия, она колеблется от значения 0,7 до 1,57.
Как определить валентные электроны
Валентностью называют способность атома вступать во взаимодействие с другими атомами, образуя с ними определенные химические связи. Валентными электронами именуются электроны, непосредственно участвующие в образовании химической связи. Основными создателями, внесшими в теорию валентности наибольший вклад, являются русский ученый Бутлеров и немецкий ученый Кекуле. Электроны, которые принимают участие в образовании химической связи, называют валентными.
Атом, как мы все знаем из школьного курса, устроен таким образом, что довольно-таки напоминает по своему устройству Солнечную систему. В центре атома находится огромное ядро, чья масса чуть менее, чем полностью равняется массе всего атома, а вокруг него по орбиталям вращаются мелкие электроны, неодинаковые по своим внутренним характеристикам. Ядро атома окажется не таким уж и большим, если сравнить его размеры с длиной расстояния до орбиталей, по которым вращаются атомы. Чем дальше от ядра и чем ближе к внешней электронной оболочке находится электрон конкретно взятого атома, тем быстрее он вступает во взаимодействие с электронами других атомов.
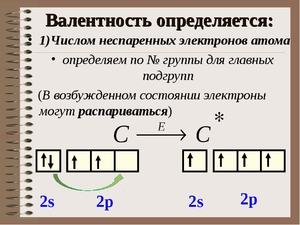
Итак, перед нами таблица Менделеева. Найти на ней нужно третий период. Последовательно перебираем элементы главных подгрупп в нем. Существует правило, согласно которому валентность элемента определяется по номеру его группы и равняется количеству электронов на внешней оболочке его атома.
Помимо главных, есть еще и побочные подгруппы. Когда дело касается их, учитываются еще и d-электроны на предыдущем подуровне. В таблице Менделеева все эти значения легко можно отыскать. Попробуем определить высшую валентность хрома. На внешнем уровне у хрома находится 1 электрон, на d-подуровне — 5. Следовательно, его высшая валентность равна 6. У марганца на внешнем уровне 2 электрона, на d-подуровне — 5. Значит, его высшая валентность — 7.
Все вышеописанное, за некоторыми исключениями, действительно для элементов всех других побочных подгрупп (помимо тех, в которые включены марганец и хром). Вот исключения:
Видео
Это видео поможет вам лучше усвоить такое понятие, как электроотрицательность.
Электроотрицательность
Элементы с высокой электроотрицательностью, атомы которых имеют большое сродство к электрону и высокую энергию ионизации, т. е. склонные к присоединению электрона или смещению пары связывающих электронов в свою сторону, называются неметаллами.
К ним относятся: водород, углерод, азот, фосфор, кислород, сера, селен, фтор, хлор, бром и иод. По ряду признаков к неметаллам относят также особняком стоящую группу благородных газов (гелий-радон).
К металлам относится большинство элементов Периодической системы.
Для металлов характерны низкая электроотрицательность, т. е. низкие значения энергии ионизации и сродства к электрону. Атомы металлов либо отдают электроны атомам неметаллов, либо смешают от себя пары связывающих электронов. Металлы отличаются характерным блеском, высокой электрической проводимостью и хорошей теплопроводностью. Они в большинстве своем обладают прочностью и ковкостью.
Такой набор физических свойств, отличающих металлы от неметаллов, объясняется особым типом связи, существующей в металлах. Все металлы имеют четко выраженную кристаллическую решетку. В ее узлах наряду с атомами находятся катионы металлов, т.е. атомы, потерявшие свои электроны. Эти электроны образуют обобществленное электронное облако, так называемый электронный газ. Эти электроны находятся в силовом поле многих ядер. Такая связь называется металлической. Свободная миграция электронов по объему кристалла и обусловливает особые физические свойства металлов.
Общая и неорганическая химия для студентов заочного отделения ИХТИ
Периодический закон Д.И. Менделеева и периодичность свойств атомов. Конспект
1. Современная формулировка периодического закона и структура периодической системы Д.И.Менделеева
В 1869 г. Д.И. Менделееву удалось сформулировать периодический закон – важнейший закон природы:
свойства химических элементов, а, следовательно, и свойства образуемых ими простых и сложных веществ состоят в периодической зависимости от их атомного веса.
Согласно этой формулировке наблюдалось несоответствие положения некоторых элементов в периодической системе Менделеева:
В начале 20 века закон Менделеева и его система были обоснованы на квантово-механическом уровне. Существо этого закона было полностью сохранено, а в качестве фундаментальной константы атома стал использоваться
заряд ядра атома
(соответствующий порядковому номеру элемента),
что позволило устранить наблюдавшиеся несоответствия.
Исходя из структуры электронной оболочки атомов число элементов
в III периоде – должно было бы быть 18;
в IV периоде – должно было бы быть 32;
в V периоде – должно было бы быть 50.
Это обусловлено тем, что заполнение d-состояний электронами запаздывает на один период, а заполнение f-состояний – на два периода.
Отличие реальной системы от теоретически возможной заключается в том, что в первой не учитывалось электрон-электронное взаимодействие. Теоретический учет этого взаимодействия – чрезвычайно сложная задача. На качественном уровне приходится учитывать три эффекта –
эффект экранирования электронами ядра атома,
эффект проникновения электронов к ядру,
взаимное отталкивание электронов, принадлежащих одному и тому же энергетическому слою
Эффект экранирования ядра связан с тем, что внутренние электроны атома частично заслоняют ядро, в результате чего уменьшается его воздействие на внешний электрон. Эффект экранирования учитывается некоторой постоянной Sэкр, называемой константой экранирования. Заряд ядра с учетом экранирования называется эффективным зарядом и определяется соотношением Zэфф. = Z – Sэкр. Экранирование внешнего электрона возрастает с увеличением общего числа электронов в атоме.
Эффект проникновения электронов к ядру обусловлен тем, что электрон, согласно положениям квантовой механики, может находиться в любой точке атома. Это означает, что внешний электрон часть времени находится вблизи ядра, проникая через слои внутренних электронов, и не испытывает при этом их экранирующего действия.
Распределение электронной плотности относительно ядра изображают кривой распределения вероятности нахождения электрона в шаровом слое радиуса r толщиной dr, объем которого dV = 4pr 2 dr.
Для одного и того же энергетического слоя наибольшую проникающую способность проявляют s-электроны, меньшую – p-электроны, еще меньшую – d-электроны (рис.1). Число максимумов на кривой определяется числом n. Для 3s-электрона Nmax = n, для р-электрона Nmax = (n – 1), для d-электрона Nmax = (n – 2). Эффект проникновения увеличивает прочность связи электрона с ядром.
Взаимное отталкивание электронов, принадлежащих одному и тому же энергетическому слою, оказывает большое влияние на прочность связи электрона с ядром. Это отталкивание особенно сильно проявляется между двумя электронами с противоположными спинами, находящимися на одной орбитали.
Эти эффекты приводят к изменению эффективного заряда ядра атома, что позволяет объяснить реальную структуру электронной оболочки атома.
В настоящее время система Д.И. Менделеева представляет собой предельно краткую и четкую физико-химическую энциклопедию. В современной формулировке периодический закон Д.И.Менделеева звучит следующим образом: свойства элементов, а также свойства и формы образуемых ими соединений находятся в периодической зависимости от заряда ядра атомов элементов.
На основе периодического закона разработаны графические системы Д.И. Менделеева. В настоящее время их насчитывается более 3 тысяч.
Наиболее распространены два варианта таблицы – короткопериодный и длиннопериодный.
Периоды – горизонтальные ряды, объединяющие элементы с одинаковым значением главного квантового числа n. Номер периода соответствует числу заполненных электронами энергетических уровней атома каждого конкретного элемента.
Группы – вертикальные ряды, объединяющие элементы с одинаковым числом валентных электронов.
Современная периодическая таблица состоит из 7 периодов: первый содержит всего два элемента, второй и третий – по 8 элементов (малые периоды), четвертый и пятый – по 18 элементов, шестой – 32 элемента, седьмой период не завершен, но должен содержать также 32 элемента (большие периоды).
Каждый период начинается с двух s-элементов, в атомах которых впервые появляется электрон со значением n, соответствующим номеру заполняемого периода, и заканчивается шестью p-элементами. В больших периодах между s- и р-элементами размещается по десять d- элементов. Все f-элементы условно помещаются в ячейки лантана (лантаноиды) и актиния (актиноиды), а их символы обычно выносятся за пределы периодической таблицы в виде рядов.