Статьи
Что лучше использовать для системы обогрева дома: воду или антифриз
Стандартным теплоносителем для автономных систем обогрева частных домов является вода. Ее используют уже в течение многих лет. Но последнее время производители стали предлагать переход на антифриз, отмечая ряд его преимуществ. Чтобы понять, стоит ли применять незамерзающую жидкость, не является ли она обычным маркетинговым ходом, что вообще лучше для установленной отопительной системы, следует рассмотреть и провести сравнение двух видов теплоносителя.
Замена теплоносителя в системе отопления загородного дома
В современных системах автономного обогрева вместо обычной воды применяется антифриз. У такого вещества есть срок службы. Поэтому по его истечению надо проводить замену незамерзающей жидкости в котле во избежание появления проблем в работе всей отопительной установки. Поменять теплоноситель в частном доме можно самостоятельно. Для этого надо знать ряд правил, учитывать важные моменты и следовать алгоритму.
Применение антифриза в отопительной системе частного дома
Даже если система отопления отличается повышенной надежностью и хорошим качеством исполнения, вероятность промерзания в зимний период исключить нельзя. Применение антифриза в отопительной системе частного дома существенно снижает риск этой неприятности. Рассмотрим, какие преимущества у « незамерзаек », каким требованиям они должны отвечать, каковы правила их использования.
Водно-гликолевый раствор: что это?
Моноэтиленгликоль: история получения, свойства, область использования
Моноэтиленгликоль (МЭГ) — двухатомный спирт, простейший представитель категории многоатомных спиртов, называемых также полиолами. Это бесцветная, несколько маслянистая жидкость со сладковатым привкусом и без запаха. Многие задают вопрос: есть ли различия между моноэтиленгликолем и этиленгликолем? Различия нет. Это наименования одного и того же соединения.
Наши менеджеры не только оформят заказ, но и помогут грамотно сформировать его, а также предоставят всю необходимую информацию и материалы для успешной реализации.
Для заказа продукции вы можете обратиться в отдел сбыта по телефону +7(8313) 27-52-47.
Отгрузка продукции производится в любой подходящей для Вас таре и отправляется любым, удобным для Вас способом, в следующие города:
Антифриз на основе этиленгликоля марки, различия, состав
Состав антифриза.
Концентрат антифриза / охлаждающей жидкости состоит примерно из следующих компонентов:
Гликоль присутствует для снижения температуры замерзания и повышения температуры кипения охлаждающей жидкости. Небольшое количество воды либо содержится в используемых добавках, или добавляется для лучшего смешивания продуктов. Она позволяет присадкам лучше растворяться в гликоле и предотвращает выпадению осадка во время хранения.
Присадки, используемые при производстве охлаждающих жидкостей, имеют основное влияние на конечное качество антифриза, его свойства и срок эксплуатации
Очень важно качество самих компонентов пакета присадок, правильность и полнота их подбора, выполнение технологических процессов смешения. В дешевых охлаждающих жидкостях эти условия часто не выполняются
Градация присадок по выполняемым функциям.
Буферные присадки:
Присадки или химические вещества — фосфаты, бораты, или соли органических кислот.
Эффект — поддержание надлежащего рН, нейтрализация кислых материалов, которые попадают в охлаждающую жидкость.
Ингибиторы коррозии:
Присадки или химические вещества — нитраты, силикаты, меркаптобензотиазол (добавка для защиты желтого металла), толилтриазол (добавка для защиты желтого металла), и соли органических кислот.
Эффект — предотвращение коррозии различных металлов системы охлаждения.
Антикавитационные присадки:
Присадки или химические вещества — нитриты и молибдаты.
Преимущества и эффект — особенно эффективны при кавитации чугуна, защита от коррозии.
Пеногасители:
Присадки или химические вещества — Полигликоли и силиконы.
Эффект — предотвращение образования устойчивой пены, которая может привести к проблемам с отдачей тепла / коррозией.
Контроль отложений и окалины:
Присадки или химические вещества — фосфонаты и водорастворимые полимеры, такие как полиакрилаты.
Эффект — Предотвращает накопление окалины или отложений на поверхности теплоотдачи.
Антиобрастание:
Присадки или химические вещества — поверхностно-активные вещества / моющие средства с низким пенообразованием.
Эффект — предотвращение накопления нефтепродуктов и грязи, которые блокируют отдачу тепла и способствуют коррозии.
В чем разница G12 и G11, G12 и G13
Основные виды антифризов, такие как G11, G12 и G13 отличаются по виду используемых присадок: органические и неорганические.
Общие сведения об антифризах, в чем между ними отличие и как подбирать нужную ОЖ
Через то, что антифриз G11 создает слой подобный накипи в чайнике, он не подходит для охлаждения современных авто, имеющих радиаторы с тонкими каналами. К тому же, температура кипения такой охлаждайки составляет 105 °С, а строк службы не более 2-х лет или 50-80 тыс. км. пробега.
Зачастую антифриз G11 окрашивается в зеленый
или синий цвета
. Такую ОЖ применяют для автомобилей, выпущенных до 1996
года и машины с большим объёмом охлаждающей системы.
G11 плохо подходит к алюминиевым радиаторам и блокам, так как его присадки не могут должным образом защищать этот металл при высоких температурах.
В Европе авторитетная спецификация классов антифризов принадлежит концерну Volkswagen поэтому соответствующая маркировка VW TL 774-C предусматривает использование в антифризе неорганических присадок и имеет обозначение G 11. Спецификация VW TL 774-D предусматривает наличие карбо-кислотных добавок на органической основе и маркируется как G 12. Стандартами VW TL 774-F и VW TL 774-G маркируются классы G12 + и G12 ++, а самый сложный и дорогостоящий антифриз G13 регламентируется стандартом VW TL 774-J. Хотя другие производители такие как Форд или Тойота имеют свои стандарты качества. Кстати разницы между тосолом и антифризом нету. Тосол – одна из марок русского минерального антифриза, которая не рассчитан на работу в моторах с алюминиевым блоком.
Органические и неорганические антифризы смешивать категорически нельзя, поскольку возникнет процесс свертывания и в результате появится осадок в виде хлопьев!
А жидкости классов G12, G12 + и G13 разновидности органических антифризов
«Long Life». Применяются в системах охлаждения современных авто
выпускаемых начиная с 1996 г. G12 и G12 + на основе этиленгликоля но только G12 plus предполагает использование гибридной технологии
производства в которой объединили силикатную технологию с карбоксилатную. В 2008 году появился еще и класс G12++, у такой жидкости, органическая основа сочетается с небольшим количеством минеральных присадок (называется лобридной
Lobrid или SOAT coolants). У гибридных антифризах органические присадки смешиваются вместе с неорганическими (могут применяться силикаты, нитриты и фосфаты). Такое объединение технологий дало возможность устранять главный недостаток антифриза G12 – не только устранять коррозию, когда она уже появилась, но и выполнять профилактическое действие.
G12+, в отличии от G12 или G13 может быть смешана с жидкостью класса G11 или G12, но все равно такой «микс» не рекомендован.
Охлаждающая жидкость класса G13
начала производится с 2012-го и рассчитана для автомобильных двигателей работающих в экстремальных режимах
. С технологической точки зрения отличий от G12 не имеет, единственная разница в том, что сделана на пропилен гликоле
, который менее ядовитый, быстрее разлагается, а значит, наносит меньший вред окружающей среде
при его утилизации и его цена значительно выше G12-го антифриза. Изобретался исходя из требований к повышению экологических норм. Антифриз G13, как правило, фиолетового или розового цвета, хотя на самом деле может окрашиваться любым цветом, так как это всего лишь краситель, от которого её характеристики не зависят, разные производители могут выпускать ОЖ с разными цветами и оттенками.
Разница в действии карбоксилатного и силикатного антифризов
Типы антифризов для отопления
Антифриз для отопления создан на основе водных растворов этиленгликоля и пропиленгликоля. Эти соединения в чистом виде представляют собой достаточно агрессивные среды для отопительных систем. Однако существуют специальные присадки для защиты от коррозии, появления пены, накипи, повреждения отдельных элементов сети и арматуры.
Эти присадки значительно увеличивают термическую стойкость, которая обеспечивается в диапазонах температур от – 70 до + 110 °С. Отмечается отсутствие термической деструкции даже при температуре + 165 — + 175 °С.
Антифриз в системе отопления нормально реагирует на материалы, которые применяются в отопительных сетях:
Этиленгликолевые антифризы
Отечественные антифризы для систем отопления, которые широко представлены на рынке, созданы на основе этиленгликоля.
Они изготавливаются в таких вариантах исполнения:
Заполнение системы отопления антифризом начинается с приготовления раствора. Для этого его необходимо своими руками разбавить водой. Цена этиленгликоля невысока, поэтому антифриз на его основе обычно не очень дорогой.
Этот недостаток ограничивает использование антифризов на основе этиленгликоля в двухконтурных сетях теплоснабжения, в которых теплоноситель может попасть в контур для горячей воды. Поэтому применения таких антифризов ограничивается только одноконтурными системами отопления.
Пропиленгликолевые антифризы
В конце прошлого века на рынки западных стран поступили нетоксичные антифризы, которые изготавливались на основе пропиленгликоля. Преимущество этих антифризов – полная безвредность.
Это качество является самым важным для двухконтурных систем теплоснабжения. Эти антифризы тоже появились на нашем рынке. Инструкция позволяет их использовать при температуре до – 35 °С.
Пропиленгликоль является утвержденной пищевой добавкой Е1520, которая часто встречается в кондитерских изделиях в качестве агента, который способствует смягчению, удержанию влаги и дисперсии вещества.
Триэтиленгликолевые антифризы
При высоких рабочих температурах (до 180 °С) применяют антифризы на основе триэтиленгликоля. Это вещество имеет высокие показатели температурной стабильности. Однако такие теплоносители не являются продукцией для широкого использования. Обычно триэтиленгликолевые антифризы используются в специальных системах отопления, в которых радиаторы отопления для антифриза также рассчитаны на высокие температуры.
Моноэтиленгликоль и этиленгликоль в чем разница
Часто на специализированных форумах можно встретить вопрос: есть ли разница между этиленгликолем и моноэтиленгликолем (МЭГ)? Специалисты уверенно утверждают, что это одно и то же вещество, обладающие аналогичными физическими свойствами и рабочими характеристиками при использовании в качестве антифриза. А вот разница между моно- и диэтиленгликолем действительно присутствует.
Диэтиленгликоль (в литературе встречается название дигликоль или ДЭГ) обладает лучшей растворимостью, более высокой вязкостью и температурой кипения, а также меньшей летучестью. Температура замерзания у ДЭГ чуть выше, чем у моноэтиленгликоля, но это не сказывается на сфере применения и способностях проводить тепло.
Важно заметить, что дигликоль отлично растворяется в воде и смешивается с многими органическими соединениями – пропиленгликолем, одноатомными спиртами (этанол), карбитолами, целлозольвами, фенолом, ацетоном, пиридином, фурфуролом. Растворимость остается высокой в широком диапазоне рабочих температур. ДЭГ не взаимодействует с растительными и минеральными маслами и не растворяется в них.
Сфера применения
На практике водные растворы диэтиленгликоля используются в качестве антифриза реже, чем привычная нам моноэтиленгликолевая смесь. Это объясняется не физическими характеристиками вещества (они не различаются столь существенно), а различными объемами производства и доступностью на рынке. Теплоноситель на основе пропиленгликоля или этиленгликоля более доступен, да и стоимость его производства не так высока.
Помимо инженерных систем дигликоль широко используется как селективный растворитель при экстракции нефтепродуктов и ароматических углеводородов – бензола, толуола, ксилола. Он отлично растворяет перечисленные вещества и не оказывает влияние на нафтеновые и парафиновые углеводороды. За счет лучшей растворимости в воде растворитель на основе ДЭГ гораздо эффективнее, что позволяет получать на химическом производстве готовый продукт различной степени чистоты.
Еще одно направление использования – удаление водяного пара из прокачиваемого по трубопроводным системам газа. Решение этой задачи позволяет минимизировать риск образования конденсата и ледяных пробок внутри труб. Кроме того, диэтиленгликоль позволяет эффективно очищать газ от посторонних примесей – диоксида углерода и сероводорода.
Дигликоль незаменим при производстве некоторых полимерных материалов – термостойких и огнестойких полиуретанов, ненасыщенных полиэфирных смол, устойчивых к воздействию щелочи алкидных смол, модифицирующих компонентов. Это синтез активаторов полимеризации, стабилизаторов, пластификаторов, антиоксидантов, отвердителей эпоксидных смол.
Технология изготовления и безопасность
Сегодня в химической промышленности распространены две технологии получения диэтиленгликоля: совместный синтез с МЭГ и получение непосредственно из этиленгликоля.
Что касается мер предосторожности, то токсичность дигликоля ниже, чем у привычных нам соединений на основе МЭГ. Это существенно расширяет сферу применения теплоносителей, имеющих в составе диэтиленгликоль. Пары не представляют опасности даже при вдыхании, токсичен лишь прием вещества внутрь. Отработанная в инженерных системах водная смесь утилизируется или очищается ионно-обменными смолами.
широкого применения
для дезинфекции на объектах железнодорожного транспорта, пищевой промышленности, ЛПУ, ветеринарного надзора
для железнодорожного транспорта, сертифицированные ВНИИЖТ- «Фаворит К» и «Фаворит Щ», внутренняя и наружная замывка вагонов.
Основной промышленный метод получения этиленгликоля — гидратация этилена окиси при 10 ат и 190—200°С или при 1 ат и 50—100°С в присутствии 0,1—0,5% серной (или ортофосфорной) кислоты; в качестве побочных продуктов при этом образуются диэтиленгликоль и незначительное количество высших полимергомологов этиленгликоля.
Применение
Важным свойством этиленгликоля является способность понижать температуру замерзания воды, поэтому вещество нашло широкое применения как компонент автомобильных антифризов и тормозных жидкостей. Корозионно активен, поэтому применяется с ингибиторами коррозии.
Этиленгликоль является исходным сырьём для производства взрывчатого вещества нитрогликоля.
Также применяется в производстве целлофана, полиуретанов и ряда других продуктов. В ограниченных масштабах этиленгликоль так же применяют как растворитель печатных и некоторых других красок, в производстве чернил и паст для шариковых ручек, в органическом синтезе.
Меры безопасности
| Этиленгликоль | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование | этандиол-1,2 |
| Традиционные названия | гликоль, этиленгликоль, 1,2-диоксиэтан, 1,2-этандиол |
| Хим. формула | C2H6O2 |
| Рац. формула | C2H4(OH)2 |
| Физические свойства | |
| Состояние | бесцветная жидкость |
| Молярная масса | 62,068 г/моль |
| Плотность | 1,113 г/см³ |
| Термические свойства | |
| Т. плав. | −12,9 °C |
| Т. кип. | 197,3 °C |
| Т. всп. | 111 °C |
| Пр. взрв. | 3,2 ± 0,1 об.% [1] |
| Давление пара | 0,06 ± 0,01 мм рт.ст. [1] |
| Химические свойства | |
| pKa | 15,1 ± 0,1 [2] |
| Оптические свойства | |
| Показатель преломления | 1,4318 |
| Классификация | |
| Рег. номер CAS | 107-21-1 |
| PubChem | 174 |
| Рег. номер EINECS | 203-473-3 |
| SMILES | |
| RTECS | KW2975000 |
| ChEBI | 30742 |
| ChemSpider | 13835235 |
| Безопасность | |
| ПДК | 5 мг/м 3 |
| ЛД50 | 4700 мг/кг (крысы, перорально) |
| Токсичность | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
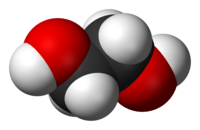
Этиленглико́ль (гликоль, 1,2-диоксиэтан, этандиол-1,2), HO—CH2—CH2—OH — кислородсодержащее органическое соединение, двухатомный спирт, простейший представитель полиолов (многоатомных спиртов). В очищенном виде представляет собой прозрачную бесцветную жидкость слегка маслянистой консистенции. Не имеет запаха и обладает сладковатым вкусом. Токсичен. Попадание этиленгликоля или его растворов в организм человека может привести к необратимым изменениям в организме и к летальному исходу. [3]
Содержание
История открытий и производства
Этиленгликоль впервые был получен в 1859 году французским химиком Вюрцем из диацетата этиленгликоля омылением гидроксидом калия и в 1860-м гидратацией этиленоксида. Он не находил широкого применения до Первой мировой войны, когда в Германии его стали получать из дихлорэтана для использования в качестве замены глицерина при производстве взрывчатых веществ. В США полупромышленное производство начато в 1917 году через этиленхлоргидрин. Первое крупномасштабное производство начато с возведением завода в 1925 году около Саут Чарлстона (Западная Вирджиния, США) компанией «Carbide and Carbon Chemicals Co.» (англ.). К 1929 году этиленгликоль использовался практически всеми производителями динамита.
В 1937 компания Carbide начала первое крупномасштабное производство, основанное на газофазном окислении этилена до этиленоксида. Монополия компании Carbide на данный процесс продолжалась до 1953 года.
Получение
В промышленности этиленгликоль получают путём гидратации оксида этилена при 10 атм и 190‒200 °С или при 1 атм и 50‒100 °С в присутствии 0,1‒0,5% серной или ортофосфорной кислоты, достигая 90% выхода. Побочными продуктами при этом являются диэтиленгликоль, триэтиленгликоль и незначительное количество высших полимергомологов этиленгликоля.
Применение
Благодаря своей дешевизне этиленгликоль нашёл широкое применение в технике.
1,3-диоксоланы могут быть получены также при реакции этиленгликоля с карбонильными соединениями в присутствии триметилхлорсилана [4] или комплекса диметилсульфат-ДМФА [5] 1,3-диоксалана устойчивы к действию нуклеофилов и оснований. Легко регенерируют исходное карбонильное соединение в присутствии кислоты и воды.
Этиленгликоль также применяется:
Очистка и осушение
Осушается молекулярным ситом 4А, полуводным сульфатом кальция, сульфатом натрия, Mg+I2, фракционной перегонкой под пониженным давлением, азеотропной отгонкой с бензолом. Чистота полученного продукта легко определяется по плотности.
Таблица плотности водных растворов этиленгликоля, 20°С
| Концентрация % | 30 | 35 | 40 | 45 | 50 | 55 | 60 |
|---|---|---|---|---|---|---|---|
| Плотность, г/мл | 1,050 | 1,058 | 1,067 | 1,074 | 1,082 | 1,090 | 1,098 |
Меры безопасности
Этиленгликоль — горючее вещество. Температура вспышки паров 120 °C. Температура самовоспламенения 380 °C. Температурные пределы воспламенения паров в воздухе, °С: нижний — 112, верхний — 124. Пределы воспламенения паров в воздухе от нижнего до верхнего, 3,8‒6,4% (по объему).
Похожие записи:
Моноэтиленгликоль и этиленгликоль в чем разница
Часто на специализированных форумах можно встретить вопрос: есть ли разница между этиленгликолем и моноэтиленгликолем (МЭГ)? Специалисты уверенно утверждают, что это одно и то же вещество, обладающие аналогичными физическими свойствами и рабочими характеристиками при использовании в качестве антифриза. А вот разница между моно- и диэтиленгликолем действительно присутствует.
Диэтиленгликоль (в литературе встречается название дигликоль или ДЭГ) обладает лучшей растворимостью, более высокой вязкостью и температурой кипения, а также меньшей летучестью. Температура замерзания у ДЭГ чуть выше, чем у моноэтиленгликоля, но это не сказывается на сфере применения и способностях проводить тепло.
Важно заметить, что дигликоль отлично растворяется в воде и смешивается с многими органическими соединениями – пропиленгликолем, одноатомными спиртами (этанол), карбитолами, целлозольвами, фенолом, ацетоном, пиридином, фурфуролом. Растворимость остается высокой в широком диапазоне рабочих температур. ДЭГ не взаимодействует с растительными и минеральными маслами и не растворяется в них.
Сфера применения
На практике водные растворы диэтиленгликоля используются в качестве антифриза реже, чем привычная нам моноэтиленгликолевая смесь. Это объясняется не физическими характеристиками вещества (они не различаются столь существенно), а различными объемами производства и доступностью на рынке. Теплоноситель на основе пропиленгликоля или этиленгликоля более доступен, да и стоимость его производства не так высока.
Помимо инженерных систем дигликоль широко используется как селективный растворитель при экстракции нефтепродуктов и ароматических углеводородов – бензола, толуола, ксилола. Он отлично растворяет перечисленные вещества и не оказывает влияние на нафтеновые и парафиновые углеводороды. За счет лучшей растворимости в воде растворитель на основе ДЭГ гораздо эффективнее, что позволяет получать на химическом производстве готовый продукт различной степени чистоты.
Еще одно направление использования – удаление водяного пара из прокачиваемого по трубопроводным системам газа. Решение этой задачи позволяет минимизировать риск образования конденсата и ледяных пробок внутри труб. Кроме того, диэтиленгликоль позволяет эффективно очищать газ от посторонних примесей – диоксида углерода и сероводорода.
Дигликоль незаменим при производстве некоторых полимерных материалов – термостойких и огнестойких полиуретанов, ненасыщенных полиэфирных смол, устойчивых к воздействию щелочи алкидных смол, модифицирующих компонентов. Это синтез активаторов полимеризации, стабилизаторов, пластификаторов, антиоксидантов, отвердителей эпоксидных смол.
Технология изготовления и безопасность
Сегодня в химической промышленности распространены две технологии получения диэтиленгликоля: совместный синтез с МЭГ и получение непосредственно из этиленгликоля.
Что касается мер предосторожности, то токсичность дигликоля ниже, чем у привычных нам соединений на основе МЭГ. Это существенно расширяет сферу применения теплоносителей, имеющих в составе диэтиленгликоль. Пары не представляют опасности даже при вдыхании, токсичен лишь прием вещества внутрь. Отработанная в инженерных системах водная смесь утилизируется или очищается ионно-обменными смолами.
широкого применения
для дезинфекции на объектах железнодорожного транспорта, пищевой промышленности, ЛПУ, ветеринарного надзора
для железнодорожного транспорта, сертифицированные ВНИИЖТ- «Фаворит К» и «Фаворит Щ», внутренняя и наружная замывка вагонов.
Основной промышленный метод получения этиленгликоля — гидратация этилена окиси при 10 ат и 190—200°С или при 1 ат и 50—100°С в присутствии 0,1—0,5% серной (или ортофосфорной) кислоты; в качестве побочных продуктов при этом образуются диэтиленгликоль и незначительное количество высших полимергомологов этиленгликоля.
Применение
Важным свойством этиленгликоля является способность понижать температуру замерзания воды, поэтому вещество нашло широкое применения как компонент автомобильных антифризов и тормозных жидкостей. Корозионно активен, поэтому применяется с ингибиторами коррозии.
Этиленгликоль является исходным сырьём для производства взрывчатого вещества нитрогликоля.
Также применяется в производстве целлофана, полиуретанов и ряда других продуктов. В ограниченных масштабах этиленгликоль так же применяют как растворитель печатных и некоторых других красок, в производстве чернил и паст для шариковых ручек, в органическом синтезе.
Меры безопасности
| Этиленгликоль | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование | этандиол-1,2 |
| Традиционные названия | гликоль, этиленгликоль, 1,2-диоксиэтан, 1,2-этандиол |
| Хим. формула | C2H6O2 |
| Рац. формула | C2H4(OH)2 |
| Физические свойства | |
| Состояние | бесцветная жидкость |
| Молярная масса | 62,068 г/моль |
| Плотность | 1,113 г/см³ |
| Термические свойства | |
| Т. плав. | −12,9 °C |
| Т. кип. | 197,3 °C |
| Т. всп. | 111 °C |
| Пр. взрв. | 3,2 ± 0,1 об.% [1] |
| Давление пара | 0,06 ± 0,01 мм рт.ст. [1] |
| Химические свойства | |
| pKa | 15,1 ± 0,1 [2] |
| Оптические свойства | |
| Показатель преломления | 1,4318 |
| Классификация | |
| Рег. номер CAS | 107-21-1 |
| PubChem | 174 |
| Рег. номер EINECS | 203-473-3 |
| SMILES | |
| RTECS | KW2975000 |
| ChEBI | 30742 |
| ChemSpider | 13835235 |
| Безопасность | |
| ПДК | 5 мг/м 3 |
| ЛД50 | 4700 мг/кг (крысы, перорально) |
| Токсичность | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Этиленглико́ль (гликоль, 1,2-диоксиэтан, этандиол-1,2), HO—CH2—CH2—OH — кислородсодержащее органическое соединение, двухатомный спирт, простейший представитель полиолов (многоатомных спиртов). В очищенном виде представляет собой прозрачную бесцветную жидкость слегка маслянистой консистенции. Не имеет запаха и обладает сладковатым вкусом. Токсичен. Попадание этиленгликоля или его растворов в организм человека может привести к необратимым изменениям в организме и к летальному исходу. [3]
Содержание
История открытий и производства
Этиленгликоль впервые был получен в 1859 году французским химиком Вюрцем из диацетата этиленгликоля омылением гидроксидом калия и в 1860-м гидратацией этиленоксида. Он не находил широкого применения до Первой мировой войны, когда в Германии его стали получать из дихлорэтана для использования в качестве замены глицерина при производстве взрывчатых веществ. В США полупромышленное производство начато в 1917 году через этиленхлоргидрин. Первое крупномасштабное производство начато с возведением завода в 1925 году около Саут Чарлстона (Западная Вирджиния, США) компанией «Carbide and Carbon Chemicals Co.» (англ.). К 1929 году этиленгликоль использовался практически всеми производителями динамита.
В 1937 компания Carbide начала первое крупномасштабное производство, основанное на газофазном окислении этилена до этиленоксида. Монополия компании Carbide на данный процесс продолжалась до 1953 года.
Получение
В промышленности этиленгликоль получают путём гидратации оксида этилена при 10 атм и 190‒200 °С или при 1 атм и 50‒100 °С в присутствии 0,1‒0,5% серной или ортофосфорной кислоты, достигая 90% выхода. Побочными продуктами при этом являются диэтиленгликоль, триэтиленгликоль и незначительное количество высших полимергомологов этиленгликоля.
Применение
Благодаря своей дешевизне этиленгликоль нашёл широкое применение в технике.
1,3-диоксоланы могут быть получены также при реакции этиленгликоля с карбонильными соединениями в присутствии триметилхлорсилана [4] или комплекса диметилсульфат-ДМФА [5] 1,3-диоксалана устойчивы к действию нуклеофилов и оснований. Легко регенерируют исходное карбонильное соединение в присутствии кислоты и воды.
Этиленгликоль также применяется:
Очистка и осушение
Осушается молекулярным ситом 4А, полуводным сульфатом кальция, сульфатом натрия, Mg+I2, фракционной перегонкой под пониженным давлением, азеотропной отгонкой с бензолом. Чистота полученного продукта легко определяется по плотности.
Таблица плотности водных растворов этиленгликоля, 20°С
| Концентрация % | 30 | 35 | 40 | 45 | 50 | 55 | 60 |
|---|---|---|---|---|---|---|---|
| Плотность, г/мл | 1,050 | 1,058 | 1,067 | 1,074 | 1,082 | 1,090 | 1,098 |
Меры безопасности
Этиленгликоль — горючее вещество. Температура вспышки паров 120 °C. Температура самовоспламенения 380 °C. Температурные пределы воспламенения паров в воздухе, °С: нижний — 112, верхний — 124. Пределы воспламенения паров в воздухе от нижнего до верхнего, 3,8‒6,4% (по объему).