Что такое мозаичный эмбрион?
Преимплантационное генетическое тестирование эмбрионов на анеуплоидии (PGT-A) – это генетический анализ, который используется для повышения успешности ЭКО путем получения информации о хромосомном здоровье эмбриона.
Эмбрионы с правильным набором хромосом 46 – (эуплоидные) имеют больше шансов на имплантацию и развитие успешной беременности, чем эмбрионы с неправильным набором хромосом (анеуплоидные). У здорового человека в клетках 46 хромосом. На самом деле у нас есть две пары каждой хромосомы, одну из которых мы получаем от нашей биологической матери, а другую – от нашего биологического отца.
PGT-A проводится по причине того, что у анеуплоидных эмбрионов очень высока вероятность неудачной имплантации или прерывания беременности.
Вероятность получения анеуплоидного эмбриона увеличивается с возрастом.
Бывают такие варианты, когда из пары хромосом присутствует только одна хромосома – моносомия. Или же наоборот, вместо 2 хромосом, их 3, что называется трисомией. В результате преимплантационного генетического тестирования, эмбрион, у которого есть такие хромосомные изменения, называется анеуплоидным.
Однако недавние достижения в технологии PGT-A выявили третий вариант результатов PGT-A, которые находятся где-то посередине. Такой вариант, получивший название мозаичных эмбрионов (содержит сочетание анеуплоидных и эуплоидных клеток). Причина в том, что секвестирование ДНК для тестирования PGT стало более продвинутым и более чувствительным. Эта обновленная технология известна как NGS (следующее поколение секвестрования).
Теперь мы стали видеть более мелкие детали, тогда как раньше это было невозможно.
Сейчас можно услышать — «40% мозаика», что означает, что 40% клеток анеуплоидные, а 60% – эуплоидные (по данным биопсии).
Мозаицизм не обязательно присутствует во всем эмбрионе, он может быть только в определенных его участках. При биопсии эмбриона (бластоцисты) берутся клетки трофэктодермы (ТЭ), которыя в будущем формируют плаценту, а внутриклеточную массу (ВКМ), из которой будет формироваться плод, не затрагивают.
Мы должны помнить, что мозаицизм, выявленный в образце трофэктодермы, не всегда указывает на наличие мозаицизма в внутриклеточной массе, что, в свою очередь, не приводит к появлению мозаицизма у самого плода.
Какая частота мозаичных эмбрионов по данным PGT–A?
Мозаика встречается примерно у 15-90% эмбрионов на стадии дробления и у 30-40% бластоцист (5-ти суточной стадии развития эмбриона) (Spinella et al. 2018), возникает с одинаковой частотой независимо от возраста (Munne et al., 2017), от всех протестированных эмбрионов методом PGT-A.
Очевидно, что эуплоидные эмбрионы – имею выше шанс достичь наступления успешной беременности. В этом случае наиболее частый вопрос, который пациенты задают при получении результатов PGT-A: «Как влияет этот мозаичный результат на беременность или ребенка?».
Ответ сложен. Хотя мозаицизм существовал всегда, его можно было обнаружить только в течение нескольких лет, поэтому последующие исследования все еще продолжаются.
Тем не менее есть некоторые руководящие принципы и рекомендации профессионального медицинского сообщества.
Почему происходит мозаицизм эмбриона?
Причина возникновения полностью анеуплоидных эмбрионов является ошибка мейоза в яйцеклетке или сперматозоиде, и эта ошибка затем переносится в каждую клетку эмбриона.
В мозаичных эмбрионах ошибка возникает после оплодотворения, поражаются только те клетки, которые происходят от клетки с нарушением при ее делении. Важен тот факт, что уровень мозаицизма напрямую зависит от времени митотической ошибки. Если ошибка произойдет в ранней фазе деления клеток, тогда будет затронуто больше клеток, чем если бы это произошло на более позднем этапе.
Вероятно, мозаицизм эмбриона может быть результатом быстрого деления клеток и расслабления «контрольных точек», характерных для раннего развития эмбриона, и что это переходная фаза во время развития (McCoy 2017).
Для проведения PGT-A эмбриолог проводит получение, как правило, около 5-8 клеток у эмбриона на стадии бластоцисты, что для эмбриона полностью безопасным.
И так в образце биопсии для PGT-A если 5 из 5 клеток являются эуплоидными, то эмбрион является эуплоидным.
Соответственно, при проведении тестирования 5 клеток, мозаицизм минимально может составить 20% (1 из 5 клеток), а самый высокий показатель может быть 80% (4 из 5 клеток).
Международное общество по преимплантационной генетической диагностике (PGDIS) по выполнению PGT-A, рекомендуют классифицировать результаты следующим образом:
Рекомендации по переносу мозаичных эмбрионов
Международное собщество по преимплантационной генетической диагностике (PGDIS) рекомендовало отдавать приоритет мозаичным эмбрионам для переноса в зависимости от уровня мозаицизма и конкретной задействованной хромосомы.
Поскольку мозаицизм – относительно новый термин, по этой теме не так много данных, большинство рекомендаций сводятся к тому, что при переносе мозаичного эмбриона важно смотреть, какие хромосомы затронуты и могут ли быть связанные синдромы:
Grati et al. (2018) установили основные рекомендации в зависимости от вовлеченности конкретной хромосомы, оценили каждую из трисомий мозаичного эмбриона.
Приоритетные рассмотрения:
Какой показатель успешности мозаичных эмбрионов при переносе?
Показатели успешности мозаичных эмбрионов следует оценивать в зависимости от % мозаицизма (какой процент клеток у эмбриона содержит анеуплоидию).
Munne et al. (2017): 56% развивающаяся беременность (если мозаицизм 20-40%) при 22% развивающейся беременности (если мозаицизм > 40%);
Spinella et al. (2018): 42% живорождений (при 50% мозаичных эмбрионах). Частота выкидышей одинакова в обеих группах.
Мозаицизм низкого уровня может иметь сравнимый успех с переносом эуплоидных эмбрионов.
Важным показателем является репродуктивный возраст женщины при переносе мозаичного эмбриона.
Виктор и др. (2019) обнаружили, что возможность имплантации мозаичных эмбрионов может уменьшаться с возрастом – с 56% у женщин моложе 34 лет до 27% у женщин старше 34 лет.
Авторы предполагают, что такие показатели могут быть по причине того, что самокоррекция более эффективна в более молодом репродуктивном возрасте.
Что такое самокоррекция эмбриона? Что происходит с анеуплоидными клетками в мозаичном эмбрионе?
Большинство мозаичных эмбрионов становятся полностью анеуплоидными или эуплоидными к 12 дню развития (Popovic et al. (2019).
Способность исправлять себя можно объяснить следующим образом: в мозаичном эмбрионе клетки с анеуплоидией могут делиться медленнее, истощаться и погибнуть с большей вероятностью в сравнении с хромосомно здоровыми (эуплоидными) клетками, которые растут быстрее.
Но если анеуплоидных клеток слишком много, они могут вытеснить эуплоидные клетки и привести к остановке развития эмбриона либо к дальнейшему развитию эмбриона с не правильным набором хромосом.
Аномальные клетки могут перемещаться в трофэктодерму (будущую плаценту), в то время как эуплоидные клетки сосредотачиваться во внутриклеточной массе (клетки из которых происходит развитие эмбриона). На самом деле это способ самокоррекции, который мозаичный эмбрион может использовать для удаления измененных клеток из ВКМ.
Существует вероятно определенный порог, при котором такая самокоррекция может происходить.
Является ли мозаицизм с моносомией приоритетным для переноса эмбриона?
Отсутствие хромосомы (моносомия) у эмбриона редко приводит к развитию беременности и рождению ребенка (за исключением отсутствия одной X половой хромосомы) – синдром Тернера (кариотип 45 X0). Эмбрион не может иметь только одну копию хромосомы (это существенная потеря важного генетического материала), что приводит к невозможности развития.
По этим причинам мозаичный эмбрион с моносомией может быть лучшим выбором для переноса.
При переносе эмбриона с моносомией эуплоидные (хромосомно здоровые) клетки вытесняют моносомию, у эмбриона происходит самокоррекция и происходит развитие здоровой беременности.
Второй вариант, если анеуплоидные клетки перерастают, при моносомии, как правило, происходит остановка на раннем этапе развития, имплантация не наступает. Потому, что для развития эмбриона ему нужны две пары хромосом.
Что такое сегментарный мозаицизм?
Сегментарный хромосомный мозаицизм – это изменение, при котором затрагивается только участок (сегмент) хромосомы. Это может происходить на одной хромосоме (одиночная сегментарная мозаика) либо на нескольких хромосомах (множественная сегментная мозаика). Основываясь на данных многих исследований, сегментарные мозаики могут быть сопоставимы с эуплоидными эмбрионами по частоте имплантации (за исключением, возможно, нескольких сегментарных мозаик).
Мозаицизм целой хромосомы – это изменение при которой затрагивается вся хромосома, а не только ее сегмент.
Сложный аномальный эмбрион – это эмбрион, у которого 3 или более измененных хромосомы или хромосомных сегментов.
Мозаицизм целой хромосомы может иметь меньший успех в сравнении с эуплоидными эмбрионами. Fragouli et al. (2017): 13% против 47% живорождений. Таким образом, сегментная мозаика может быть приоритетнее для переноса эмбриона, чем мозаицизм целой хромосомы.
Сложные аномальный мозаицизм имеет меньший шанс успеха по сравнению с эуплоидными эмбрионами. Munne et al. (2017): 10% против 40% развивающихся беременностей на перенос эмбриона.
Как видно, при принятии правильного решения о переносе мозаичного эмбриона, важна грамотное консультирование репродуктолога, генетическое консультирование пары для достижения успешной, безопасной беременности и рождения здорового малыша в семье.
Хромосомная анеуплоидия эмбрионов, полученных в циклах ЭКО без стимуляции
W. Verpoest, B.C. Fauser, E. Papanikolaou, C. Staessen, L. Van Landuyt, P. Donoso, H. Tournaye,I. Liebaers и P. Devroey
ПГС все чаще проводится в программах экстракорпорального оплодотворения с целью выявления численных хромосомных аномалий (анеуплоидии) эмбрионов, что направлено на повышение эффективности репродуктивного лечения. В настоящей работе описывается распространенность анеуплоидии среди эмбрионов, полученных в результате нестимулированных циклов ЭКО и ПГС, и беременности, закончившиеся рождением двух живых детей.
В естественном, нестимулированном менструальном цикле у всех пациенток проводилось трансвагинальное ультразвуковое исследование и гормональный анализ сыворотки с определением концентрации ФСГ, лютеинизирующего гормона, эстрадиола и прогестерона. В случае снижения концентрации эстрадиола и одновременного подъема уровня прогестерона овуляцию считали ложной и от забора ооцита отказывались. С целью снижения риска отсутствия оплодотворения во всех циклах использовали ИКСИ.
Оплодотворение оценивали через 18 часов, далее развитие эмбриона оценивали на 2 и 3-й день перед биопсией. Биопсию эмбриона проводили на 6-клеточной или более стадии развития. Проводили анализ хромосом X, Y, 13, 18 и 21 на первом этапе и хромосом 16 и 22 – на втором этапе.
Перенос эмбриона проводили на стадии бластоцисты на 5-й день после забора ооцита. Поддержка лютеиновой фазы не проводилась.
Средний возраст пациенток составил 31,4 года. Показаниями для лечения бесплодия в исследуемой группе служили необъяснимое бесплодие у 12 пациенток, олигоастенотератозооспермия у 17 пациенток и блокада маточных труб у одной пациентки.
Результаты данного исследования, в первую очередь, демонстрируют тот факт, что отсутствие экзогенной стимуляции яичников не исключает возникновения многочисленных хромосомных аномалий эмбрионов. Во многих исследованиях с использованием ооцитов, как животных, так и человека, было подтверждено увеличение частоты анеуплоидии после индукции овуляции. В исследованиях последних лет было показано, что в ооцитах после индукции овуляции имеет место повышенная частота нарушений геномного импринтинга. Возможно, это обусловлено не только исходными материнскими факторами, такими как возраст, но и внешними факторами, в частности, субоптимальными или аномальными биохимическими характеристиками фолликулярной жидкости и развитием цитоплазмы. Кроме того, частота анеуплоидии в ооцитах человека, как известно, существенно выше, чем в ооцитах различных видов животных, что, насколько можно полагать, связано со стимуляцией яичников, поскольку это единственная группа, в которой определялась анеуплоидия ооцитов. Другие факторы, такие как качество спермы и условия культивирования эмбрионов, также могут оказывать влияние на хромосомные характеристики эмбриона, давая толчок таким аномалиям, как мозаицизм. Эти аномалии невозможно исключить, пропуская этап стимуляции яичников.
Во-вторых, исследование подтвердило, что анеуплоидия присутствует в единичных бластомерах эмбрионов молодых женщин в возрасте до 36 лет. Хотя известно, что частота анеуплоидии в возрасте старше 36 лет увеличивается, немногое известно о частоте анеуплоидии у молодых женщин, поскольку ПГС в этой группе обычно не проводится.
Признавая ограничения этого исследования в отношении размера выборки, важно также понимать, что ПГС, будучи единственным доступным средством для оценки хромосомной состоятельности эмбриона, не может считаться оптимальным методом оценки влияния стимуляции яичников на статус хромосом ооцитов. ПГС позволяет оценить всего один или два бластомера эмбриона, который состоит как минимум из шести бластомеров, что является потенциальным источником ошибок, включая диагностику мозаицизма.
Данные настоящего исследования показывают, что исключение стимуляции яичников у молодых женщин не исключает возникновения численных хромосомных аномалий.
Анеуплоидия: у женщин в возрасте высокие шансы родить ребенка с паталогией
» data-image-caption=»» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/08/aneuplodiya.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/08/aneuplodiya.jpg?fit=825%2C550&ssl=1″/>
Анеуплоидия — генетический сбой, при котором клетки содержат не кратное гаплоидному набору (более или менее 46) число хромосом. Сюда, например, относится синдром Дауна. Ученые узнали, почему у женщин в возрасте больше шансов родить ребенка с анеуплодией.
» data-image-caption=»» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/08/aneuplodiya.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/08/aneuplodiya.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/08/aneuplodiya.jpg?resize=892%2C595″ alt=»анеуплодия» width=»892″ height=»595″ srcset=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/08/aneuplodiya.jpg?w=892&ssl=1 892w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/08/aneuplodiya.jpg?resize=450%2C300&ssl=1 450w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/08/aneuplodiya.jpg?resize=825%2C550&ssl=1 825w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2017/08/aneuplodiya.jpg?resize=768%2C512&ssl=1 768w» sizes=»(max-width: 892px) 100vw, 892px» data-recalc-dims=»1″/>
За последнее столетие достижения медицины улучшили качество и продолжительность жизни человека, но продолжительность детородного периода у женщин остается неизменной. Ученые знают, что запас ооцитов ограничен и формируется до рождения, а качество половых клеток постепенно снижается с возрастом, что приводит к сложностям с зачатием и увеличению связанных с возрастом анеуплоидий.
Ученые выяснили, почему у возрастных пар чаще рождаются дети с генетическими патологиями. Обзор исследований был опубликован в научном журнале “Тенденции в клеточной биологии».
Человеческие хромосомы «слабее»
«За день до овуляции, ооциты (женские половые клетки) начинают делиться. В идеале зрелые яйцеклетки. содержат полный набор из 23 хромосом, но этот процесс может проходить с ошибками, особенно в половых клетках людей в возрасте. Результат неправильного числа хромосом — генетические нарушения, такие как синдром Дауна, и выкидыши. Начиная исследования, мы хотели понять, что контролирует сегрегацию хромосом, когда яйцеклетка развивается, и где происходят сбои, приводящие к неправильному числу хромосом», — говорит Мелина Шух, директор департамента мейоза института биофизической химии в Германии.
Человеческие ооциты содержат пакет ДНК матери в 46 хромосомах. Когда они делятся (процесс называется мейоз) — все 46 хромосом собираются вдоль средней линии ооцита и вытягиваются в двух направлениях, после этого происходит ряд метаморфоз результат которых — яйцеклетка с 23 хромосомами. Ученые анализировали мейоз в животных и человеческих клетках, в результате чего выяснилось, что по сравнению с животными яйцеклетками, человеческие ооциты не могут в полной мере контролировать правильность распределения и прикрепления хромосом до сегрегации, так, как это происходит у животных. Это приводит к появлению яйцеклеток, которые получили слишком мало или слишком много (22 или 24) хромосомы — состояние, известное как анеуплоидия. Т.е. получается, что анеуплодия — это ошибка, сбой в программе, а не целенаправленный процесс.
Исследователи также обнаружили, что связи человеческих хромосом часто нестабильны, поэтому они могут перестраиваться во время мейоза, который может длиться целый день, что значительно больше, чем у других млекопитающих.
Чем старше женщина, тем выше шанс генетических патологий
Исследованию подверглись половые клетки женщин разных возрастов. Подтвердилось, что у женщин от 35 лет риск генетических изменений у плода всегда выше. Возрастные причины анеуплоидии в большей степени связаны с ухудшением структуры хромосом. «Мы обнаружили, что у женщин в возрасте хромосомы могут изменяться еще до мейза, что связано с ослаблением их структуры, кроме этого, с возрастом разрушаются и участки, где образуются новые связи (кинетохоры), что приводит к ошибкам сегрегации хромосом», — говорят специалисты. Они подтверждают, что посещение генетика для возрастных пар — мероприятие не для галочки.
Как бороться с анеуплодием: пренатальная диагностика, ЭКО, тест Принетекс
На данный момент не существует способа терапевтического лечения яйцеклеток с хромосомными аномалиями, ученые доказали, что это у многих женщин это возрастное явление. Да и нужно ли насильственным путем перестраивать хромосомы — вопрос спорный. Но это не значит, что женщина в возрасте должна отказаться от беременности. Современная медицина предлагает сразу несколько методов выявления хромосомных патологий у плода. Плюс можно забеременеть с помощью вспомогательных репродуктивных технологий, в том числе и использующих донорские половые клетки.
Что касается тестов, то врачи рекомендуют беременным женщинам проходить скрининги, достоверно определяющие, есть ли у плода такие нарушения. Первичный этап — неинвазивные методы диагностики беременных — УЗИ и анализы венозной крови ( пренатальный скрининг ), которые могут выявлять определенные параметры, свойственные анеуплоидии.
Если такие риски обнаружены, женщины могут обратиться для прохождения инвазивной диагностики (в этом случае проводится биопсия). Также можно сделать тест Пренетикс (ДНК ребенка выделяется из материнской крови).
Отдельно стоит рассказать про тест Prenetix. Этот инновационный метод считается лучшим для выявления анеуплодий, так как он использует в качестве материала для исследования венозную кровь будущей мамы, взятую обычным способом. Беременной женщине не нужно терпеть неприятные ощущения, связанные с биопсией и другими манипуляциями. Пройти тестирование можно в 10 недель беременности. Точность теста Пренетикс превышает 99%, но стоит он очень дорого.
Что касается ЭКО, то здесь вопрос возрастных анеуплодий решается с помощью преимплантационной генетической диагностики (ПГД). Генетический анализ исключает подсадку эмбрионов с генетическими нарушениями.
«Конечно, для многих пар ЭКО — эмоционально сложная задача, но все-таки сегодня именно ВРТ реальный выход из ситуации», — говорит ученый Мелина Шух. — «Также я хочу добавить, что в нашем исследовании есть положительный аспект. Мы узнали, что у многих женщин в возрасте «за 40» все-таки остаются яйцеклетки без каких-либо отклонений».
Где делают пренатальную диагностику на анеуплодии в Санкт-Петербурге
Сдать генетические анализы и пройти пренатальное обследование при беременности можно в СПБ в специализированной клинике Диана. Здесь выполняются все виды анализов и УЗИ. Скрининги беременных проводятся на новейшем аппарате экспертного уровня в форматах 3Д и 4Д. Диск выдается на руки. Расшифровку проводит врач высшей категории. К генетическим анализам прикладывается заключение генетика.
Преимплантационный генетический анализ эмбрионов
Каждая из 100 триллионов клеток в организме человека (за исключением красных кровяных клеток) содержит весь человеческий геном. Хромосомы – это струноподобные элементы внутри ядра (в центре) каждой клетки вашего тела. Они содержат генетическую информацию, ДНК. Ген занимает определенное место на хромосоме. В норме, есть 23 идентичных пары хромосом (2 метра ДНК) в каждой клетке, в общей сложности 46 хромосом. Каждый партнер во время оплодотворения обычно предоставляет 23 хромосомы. Если яйцеклетка или сперматозоид имеют аномальную упаковку хромосом, эмбрион, который они создают, также будет иметь хромосомные аномалии. Иногда это связано с перестройкой хромосом, или недостатком части хромосомы. В некоторых случаях есть отсутствующие хромосомы, или дополнительная хромосома (анеуплоидии), ведущие к наследственным заболеваниям. Любой эмбрион, в котором отсутствует хромосома (моносомия) перестанет расти до имплантации (фатальная аномалия). Если анеуплоидии включают хромосомы 13, 18, 21, Х или Y, беременность может дойти до родов. Наиболее распространенной из этих несмертельных аномалий является трисомия 21, или синдром Дауна, при которой присутствует дополнительная 21-я хромосома. Другие включают синдром Тернера у женщин и синдром Клайнфельтера у мужчин.
История преимплантационной генетической диагностики (ПГД)
Первые живорождения после ПГД были зарегистрированы в Лондоне в 1989 году. Две двойни девочек-близнецов родились от пяти пар с риском передачи связанного с Х-хромосомой заболевания. В настоящее время с помощью методов генетического анализа или ПГД могут быть обнаружены около 90% аномальных эмбрионов. Не все хромосомные или генетические заболевания могут быть определены этими процедурами, так как в ходе одной процедуры может быть диагностировано только ограниченное число хромосом. Многочисленные исследования на животных и некоторые исследования на человеке показывают, что микрохирургия эмбриона (биопсия), необходимая для удаления клеток, не влияет на нормальное развитие ребенка. Эта процедура, однако, была выполнена относительно небольшому числу пациентов во всем мире, поэтому точные негативные последствия, если таковые имеются, неизвестны. Несмотря на то, что после генетического анализа для выявления анеуплоидии всем мире на сегодняшний день было рождено уже много детей, эта процедура все еще относительно нова. В исследованиях на животных не было обнаружено никаких очевидных проблем и предварительные данные с эмбрионами человека позволяют предположить справедливость этого вывода. В исследовании, проведенном в Университетском колледже Лондона, исследователи недавно рассмотрели 12 преимплантационных эмбрионов с новой техникой, которая сочетает в себе амплификацию всего генома (WGA) и сравнительную гибридизацию генома (CGH). В результате в 8 из 12 изученных эмбрионов были обнаружены значительные хромосомные аномалии. Это может объяснить, почему люди имеют в лучшем случае 25% шансов на достижение жизнеспособной беременности в месяц при естественном зачатии.
Как передаются по наследству генетические заболевания
В диаграммах ниже, D или d представляет дефектный ген, а N или n представляет нормальный ген. Мутации не всегда приводят к болезни.
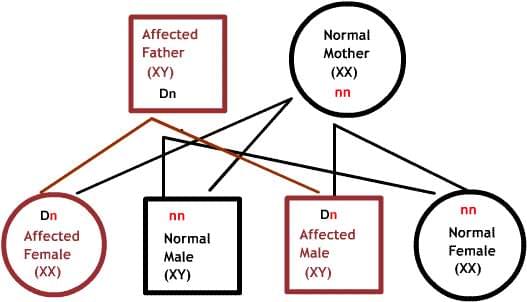
Доминантные заболевания:
Один из родителей имеет один дефектный ген, который доминирует над своей нормальной парой. Так как потомки наследуют половину своего генетического материала от каждого из родителей, есть 50% риск наследования дефектного гена, и, следовательно, заболевания.
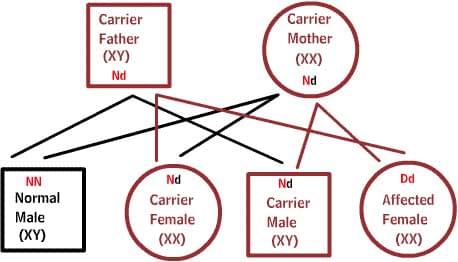
Рецессивные заболевания:
Оба родителя являются носителями одного дефектного гена, но при этом имеют нормальную пару гена. Для наследования заболевания необходимы две дефектных копии гена. Каждый потомок имеет 50% шанс быть носителем, и 25% шанс унаследовать заболевание.
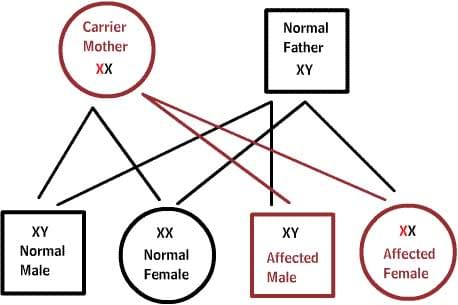
X-сцепленные заболевания:
Нормальные женщины имеют XX хромосомы, а нормальные мужчины XY. Женщины, которые имеют нормальный ген на одной из Х-хромосом, защищены от дефектного гена на их другой Х-хромосоме. Однако, у мужчины отсутствует такая защита в связи с наличием только одной Х-хромосомы. Каждый мужской потомок от матери, которая несет в себе дефект, имеет 50% шанс унаследовать дефектный ген и заболевание. Каждый женский потомок имеет 50% шанс быть носителем, как и ее мать. (на рисунке ниже X представляет нормальный ген а X представляет дефектный ген)
Возможные преимущества генетического анализа
Преимплантационная генетическая диагностика позволяет отобрать и перенести не измененные (хромосомно нормальные) эмбрионы, которые могут привести к большей частоте имплантации на эмбрион, сокращению потерь беременности и рождению большего числа здоровых детей. Генетическая диагностика предлагает парам альтернативу мучительному выбору по поводу того, чтобы прервать пострадавшую беременность после пренатальной диагностики, производимой путем амниоцентеза или биопсии ворсин хориона (CVS) на более поздних стадиях беременности. Почти все генетически связанные заболевания, которые могут быть диагностированы в перинатальном периоде либо амниоцентезом или CVS, могут быть обнаружены и ПГД. Процедура должна уменьшить психологическую травму для пар, которые несут повышенный риск генетических заболеваний для потомства.
Преимущества преимплантационной генетической диагностики (ПГД) могут включать в себя:
Возможные риски генетического анализа
Кандидаты для биопсии эмбриона и ПГД
Кандидаты для биопсии эмбриона и ПГД включают в себя:
Пары с повторными неудачами ЭКО.
Используемые методы
Для анализа на наличие генетических дефектов эмбриона, из него необходимо удалить либо первое полярное тельце из неоплодотворенной яйцеклетки и/или 1 или 2 клетки от каждого эмбриона. Это называется биопсией яйцеклетки или эмбриона и обычно делается перед тем, как происходит оплодотворение, или через 3 дня после оплодотворения. Биопсия на 6-10 клеточной стадии не оказывает отрицательного влияния на преимплантационное развитие. На этом этапе каждая клетка имеет полный набор хромосом. Обычно из эмбриона удаляется только одна клетка, так как ожидается, что будут одинаковыми со всеми другими клетками в эмбрионе. Иногда необходимо удалить вторую клетку из эмбриона, например, если сигнал в первой не обнаружен. Для диагноза предрасположенности с помощью первого и второго полярных телец, как показателей генетического статуса яйцеклетки, используется анализ методом FISH. Недостатком анализа полярных телец заключается в том, что он не принимает во внимание отцовские анеуплоидии.
Анализ биопсированной клетки использует один из двух методов:
Вся информация носит ознакомительный характер. Если у вас возникли проблемы со здоровьем, то необходима консультация специалиста.