Фосфор (P, Phosphorus)
История фосфора
Фосфор открыл в 1669 году алхимик из Гамбурга Хенниг Бранд, который проводил опыты с выпариванием человеческой мочи, пытаясь получить философский камень. Вещество, образовавшееся после многочисленных манипуляций, оказалось похожим на воск, необыкновенно ярко, с мерцанием, горело. Новому веществу было дано название phosphorus mirabilis (от латинского чудотворный носитель огня). Несколькими годами позже фосфор получил Иоганн Кункель, а также, независимо от двух первых учёных, Р. Бойлем.
Общая характеристика фосфора
Фосфор является элементом XV группы III периода периодической системы химических элементов Д.И. Менделеева, с атомным номером 15 и атомной массой 30,974. Принятое обозначение – Р.
Нахождение в природе
Фосфор содержится в морской воде и земной коре в основном в виде минералов, которых около 190 (самые важные – апатит и фосфорит). Входит в состав всех частей зелёных растений, белков, ДНК.
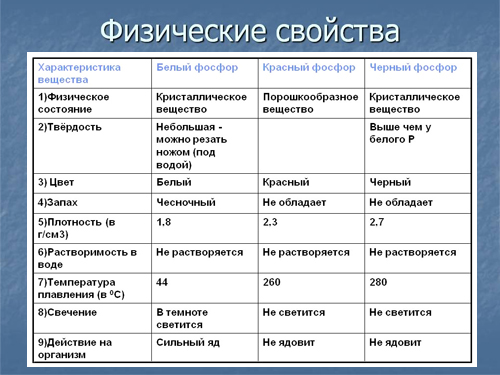
Физические и химические свойства
фосфор является неметаллом с высокой химической активностью, в свободном виде практически не встречается. Известны четыре модификации фосфора – красный, белый, чёрный и металлический.
Суточная потребность в фосфоре
Для нормального функционирования организм взрослого человека должен получать 1,0-2,0 г фосфора в сутки. Для детей и подростков норма составляет 1,5-2,5 г, для беременных и кормящих женщин возрастает до 3,0-3,8 г (calorizator). Суточная потребность в фосфоре увеличивается во время регулярных спортивных тренировок и при физических нагрузках.
Продукты питания богатые фосфором
Признаки нехватки фосфора
Недостаточное количество фосфора в организме характеризуется усталостью и слабостью, может сопровождаться потерей аппетита и внимания, частыми простудными заболеваниями, тревогой и чувством страха.
Признаки избытка фосфора
Признаками избытка фосфора в организме служат кровотечения и кровоизлияния, развивается анемия, возникает почечнокаменная болезнь.
Полезные свойства фосфора и его влияние на организм
Фосфор обеспечивает нормальные рост костной и зубной тканей организма, поддерживает их в здоровом состоянии, также участвует в синтезе белка, играет важную роль в обмене жиров, белков и углеводов. Без фосфора не могут функционировать мышцы, и не происходит умственная деятельность.
Усвояемость фосфора
При приёме минеральных комплексов стоит помнить о наилучшем балансе фосфора и кальция (3:2), а также о том, что чрезмерное количество магния и железа замедляет процесс усвоения фосфора.
Применение фосфора в жизни
Фосфор широко применяется в промышленности и сельском хозяйстве, прежде всего из-за его горючести. Его используют в производстве топлива, спичек, взрывчатых веществ, фосфорных удобрений и защиты поверхностей металлов от коррозии.
Красный фосфор
Фосфор — один из самых распространённых элементов земной коры, его содержание составляет 0,08—0,09 % её массы. В свободном состоянии не встречается из-за высокой химической активности. Образует около 190 минералов, важнейшими из которых являются апатит Ca5(PO4)3F, фосфорит Ca3(PO4)2 и другие. Фосфор содержится во всех частях зелёных растений, ещё больше его в плодах и семенах (см. фосфолипиды). Содержится в животных тканях, входит в состав белков и других важнейших органических соединений (АТФ), является элементом жизни.
Содержание
История
Фосфор открыт гамбургским алхимиком Хеннингом Брандом в 1669 году. Подобно другим алхимикам, Бранд пытался отыскать эликсир жизни или философский камень, а получил светящееся вещество. Существуют данные, что фосфор умели получать еще арабские алхимики в XII в. То, что фосфор — простое вещество, доказал Лавуазье.
Происхождение названия
В 1669 Хеннинг Бранд при нагревании смеси белого песка и выпаренной мочи получил светящееся в темноте вещество, названное сначала «холодным огнём». Вторичное название «фосфор» происходит от греческих слов «фос» — свет и «феро» — несу.
Получение
Фосфор получают из апатитов или фосфоритов в результате взаимодействия с коксом и песком при температуре 1500 °С:
Образующиеся пары белого фосфора конденсируются в приёмнике под водой. Вместо фосфоритов восстановлению можно подвергнуть и другие соединения, например, метафосфорную кислоту:
Физические свойства
Элементарный фосфор в обычных условиях представляет собой несколько устойчивых аллотропических модификаций; вопрос аллотропии фосфора сложен и до конца не решён. Обычно выделяют четыре модификации простого вещества — белую, красную, черную и металлический фосфор. Иногда их ещё называют главными аллотропными модификациями, подразумевая при этом, что все остальные являются разновидностью указанных четырёх. В обычных условиях существует только три аллотропических модификации фосфора, а в условиях сверхвысоких давлений — также металлическая форма. Все модификации различаются по цвету, плотности и другим физическим характеристикам; заметна тенденция к резкому убыванию химической активности при переходе от белого к металлическому фосфору и нарастанию металлических свойств.
Белый фосфор
Белый фосфор представляет собой белое вещество (из-за примесей может иметь желтоватый оттенок) с температурой плавления 44,1 °С. По внешнему виду он очень похож на очищенный воск или парафин, легко режется ножом и деформируется от небольших усилий. Отливаемый в инертной атмосфере в виде палочек (слитков), он сохраняется в отсутствии воздуха под слоем очищенной воды или в специальных инертных средах. Химически белый фосфор чрезвычайно активен. Например, белый фосфор медленно окисляется кислородом воздуха уже при комнатной температуре и светится (бледно-зелёное свечение). Явление такого рода свечения вследствие химических реакций окисления называется хемилюминесценцией или устаревшим термином — фосфоресценцией. Белый фосфор не только активен химически, но и весьма ядовит (вызывает поражение костей, костного мозга, некроз челюстей) и легкорастворим в органических растворителях. Летальная доза белого фосфора для взрослого мужчины составляет 0,05—0,1 г. Растворимостью белого фосфора в сероуглероде пользуются для промышленной очистки его от примесей. Плотность белого фосфора из всех его модификаций наименьшая и составляет около 1823 кг/м³.
Жёлтый фосфор
Красный фосфор
Красный фосфор, также называемый фиолетовым фосфором, — это более термодинамически стабильная модификация элементарного фосфора. Впервые он был получен в 1847 году в Швеции австрийским химиком А. Шрёттером при нагревании белого фосфора при 500 °С в атмосфере угарного газа (СО) в запаянной стеклянной ампуле.
Красный фосфор имеет формулу (Р4)n и представляет собой полимер со сложной структурой. В зависимости от способа получения и степени дробления красного фосфора, имеет оттенки от пурпурно-красного до фиолетового, а в литом состоянии — тёмно-фиолетовый с медным оттенком металлический блеск. Химическая активность красного фосфора значительно ниже, чем у белого; ему присуща исключительно малая растворимость. Растворить красный фосфор возможно лишь в некоторых расплавленных металлах (свинец и висмут), чем иногда пользуются для получения крупных его кристаллов. Так, например, немецкий физико-химик И. В. Гитторф в 1865 году впервые получил прекрасно построенные, но небольшие по размеру кристаллы (фосфор Гитторфа). На воздухе красный фосфор воспламеняется при высоких температурах (при переходе в белую форму во время возгонки), и у него полностью отсутствует явление хемолюминесценции. Ядовитость его в тысячи раз меньше, чем у белого, поэтому он применяется гораздо шире, например, в производстве спичек. Плотность красного фосфора также выше, и достигает 2400 кг/м³ в литом виде. При хранении на воздухе красный фосфор в присутствии влаги постепенно окисляется, образуя гигроскопичный оксид, поглощает воду и отсыревает («отмокает»), образуя вязкую фосфорную кислоту; поэтому его хранят в герметичной таре. При «отмокании» — промывают водой от остатков фосфорных кислот, высушивают и используют по назначению.
Чёрный фосфор
Чёрный фосфор — это наиболее стабильная термодинамически и химически наименее активная форма элементарного фосфора. Впервые чёрный фосфор был получен в 1914 году американским физиком П. У. Бриджменом из белого фосфора в виде чёрных блестящих кристаллов, имеющих высокую (2690 кг/м³) плотность. Для проведения синтеза чёрного фосфора Бриджмен применил давление в 2·10 9 Па (20 тысяч атмосфер) и температуру около 200 °С. Начало быстрого перехода лежит в области 13 000 атмосфер и температуре около 230 °С.
Чёрный фосфор представляет собой чёрное вещество с металлическим блеском, жирное на ощупь и весьма похожее на графит, и с полностью отсутствующей растворимостью в воде или органических растворителях. Поджечь чёрный фосфор можно, только предварительно сильно раскалив в атмосфере чистого кислорода до 400 °С. Удивительным свойством чёрного фосфора является его способность проводить электрический ток и свойства полупроводника. Температура плавления чёрного фосфора 1000 °С под давлением 18·10 5 Па.
Металлический фосфор
При 8,3·10 10 Па чёрный фосфор переходит в новую, ещё более плотную и инертную металлическую фазу с плотностью 3,56 г/см³, а при дальнейшем повышении давления до 1,25·10 11 Па — ещё более уплотняется и приобретает кубическую кристаллическую решётку, при этом его плотность возрастает до 3,83 г/см³. Металлический фосфор очень хорошо проводит электрический ток.
Химические свойства
Химическая активность фосфора значительно выше, чем у азота. Химические свойства фосфора во многом определяются его аллотропной модификацией. Белый фосфор очень активен, в процессе перехода к красному и чёрному фосфору химическая активность резко снижается. Белый фосфор на воздухе светится в темноте, свечение обусловлено окислением паров фосфора до низших оксидов.
В жидком и растворенном состоянии, а также в парах до 800 °С фосфор состоит из молекул Р4. При нагревании выше 800 °С молекулы диссоциируют: Р4 = 2Р2. При температуре выше 2000 °С молекулы распадаются на атомы.
Взаимодействие с простыми веществами
Фосфор легко окисляется кислородом:
Взаимодействует со многими простыми веществами — галогенами, серой, некоторыми металлами, проявляя окислительные и восстановительные свойства:
Не взаимодействует с водородом.
Взаимодействие с водой
Взаимодействует с водой, при этом диспропорционирует:
Взаимодействие со щелочами
В растворах щелочей диспропорционирование происходит в большей степени:
Восстановительные свойства
Сильные окислители превращают фосфор в фосфорную кислоту:
Реакция окисления также происходит при поджигании спичек, в качестве окислителя выступает бертолетова соль:
Применение
Фосфор является важнейшим биогенным элементом и в то же время находит очень широкое применение в промышленности. Красный фосфор применяют в производстве спичек. Его вместе с тонко измельчённым стеклом и клеем наносят на боковую поверхность коробка. При трении спичечной головки в состав который входят хлорат калия и сера, происходит воспламенение.
Элементарный фосфор
Пожалуй, первое свойство фосфора, которое человек поставил себе на службу, — это горючесть. Горючесть фосфора очень велика и зависит от аллотропической модификации.
Наиболее активен химически, токсичен и горюч белый («жёлтый») фосфор, потому он очень часто применяется (в зажигательных бомбах и пр.).
Красный фосфор — основная модификация, производимая и потребляемая промышленностью. Он применяется в производстве спичек, взрывчатых веществ, зажигательных составов, топлив, а также противозадирных смазочных материалов.
Соединения фосфора в сельском хозяйстве
Фосфор (в виде фосфатов) — один из трёх важнейших биогенных элементов (NPK), участвует в синтезе АТФ. Большая часть производимой фосфорной кислоты идёт на получение фосфорных удобрений — суперфосфата, преципитата, аммофоски и др.
Соединения фосфора в промышленности
Фосфаты широко используются:
Фосфатные связующие
Способность фосфатов формировать прочную трёхмерную полимерную сетку используется для изготовления фосфатных и алюмофосфатных связок
Биологическая роль соединений фосфора
Фосфор присутствует в живых клетках в виде орто- и пирофосфорной кислот, входит в состав нуклеотидов, нуклеиновых кислот, фосфопротеидов, фосфолипидов, коферментов, ферментов. Кости человека состоят из гидроксилапатита 3Са3(РО4)3·CaF2. В состав зубной эмали входит фторапатит. Основную роль в превращениях соединений фосфора в организме человека и животных играет печень. Обмен фосфорных соединений регулируется гормонами и витамином D. Суточная потребность человека в фосфоре 800-1500 мг. При недостатке фосфора в организме развиваются различные заболевания костей.
Токсикология элементарного фосфора
Острые отравления фосфором проявляются жжением во рту и желудке, головной болью, слабостью, рвотой. Через 2-3 суток развивается желтуха. Для хронических форм характерны нарушение кальциевого обмена, поражение сердечно-сосудистой и нервной систем. Первая помощь при остром отравлении — промывание желудка, слабительное, очистительные клизмы, внутривенно растворы глюкозы. При ожогах кожи обработать пораженные участки растворами медного купороса или соды. ПДК паров фосфора в воздухе 0,03 мг/м3.
Токсикология соединений фосфора
Некоторые соединения фосфора (фосфин) очень токсичны. Боевые отравляющие вещества зарин, зоман, табун являются соединениями фосфора.
Красный фосфор — стабильная и безопасная форма фосфора
Считается, что фосфор — это светящийся в темноте минерал, ядовитый и огнеопасный. Но это только часть правды об этом удивительном элементе. Фосфор бывает и иным, с прямо противоположными свойствами.
Что такое красный фосфор?
Фосфор может существовать в нескольких вариантах 
Красный фосфор представляет собой очень интересное вещество, естественный неорганический полимер с формулой (Р4)n и весьма сложной структурой из пирамидально связанных атомов.
Свойства красного фосфора в некоторой степени зависят от условий его получения. Изменяя температуру, свет и катализаторы, можно создавать виды красного фосфора с прогнозируемыми свойствами.
Первооткрывателем красного фосфора является австриец А.Шрёттер, который получил его, нагревая запаянную ампулу с белым фосфором и угарным газом при температуре +500 °С.
Свойства красного фосфора

Красный фосфор, в отличие от своего более известного «собрата», белого фосфора, является твердым веществом, не люминесцирует, практически ни в чем не растворим (ни в воде, ни в органических растворителях, ни в сероуглероде). Он не ядовит, самовоспламеняется на воздухе только при температуре +240-260 °С (на самом деле воспламеняется не сам красный фосфор, а его пары, которые после охлаждения превращаются в белый огнеопасный фосфор).
Плотность красного фосфора выше, чем у белого и равна 2,0 – 2,4 г/см3 (в зависимости от конкретной модификации).
На воздухе красный фосфор поглощает влагу, окисляется, превращаясь в оксид; продолжая впитывать влагу, переходит в густую фосфорную кислоту («отмокает»). Ввиду этого, реактив следует герметично укупоривать, лишая доступа к воздушной влаге. При нагревании красный фосфор не плавится, а возгоняется (испаряется). После конденсации пары вещества превращаются в белый фосфор.
Применение красного фосфора
Красный фосфор практически не токсичен и гораздо безопаснее 
Сам красный фосфор в основном применяется для изготовления спичек. Он входит в «тёрочную» смесь, которую наносят на коробок. Также его используют в смазочных материалах, в зажигательных составах, топливе, в производстве ламп накаливания.
Не знаете, где купить красный фосфор?
Купить красный фосфор и различные другие химреактивы можно в одном из крупнейших магазинов оборудования для лабораторий, «ПраймКемикалсГрупп». У нас доступные цены и удобная доставка по Москве и области, а квалифицированные менеджеры помогут сделать выбор.
Как фосфор влияет на здоровье человека?
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Фосфор является важным минералом, который есть в каждой клетке тела для выполнения их нормальных функций. Большая часть фосфора в организме находится как фосфат (PO 4). Около 85% фосфора организма содержится в костях. Как фосфор влияет на здоровье человека?
Фосфор и его воздействие на организм человека
Как и кальций, фосфор является наиболее распространенным минералом в организме. Эти 2 важных питательных вещества тесно сотрудничают для здоровья крепких костей и зубов. Около 85% фосфора в организме найдено в костях и зубах, но он также присутствует в клетках и тканях по всему организму.
Фосфор помогает отфильтровывать отходы в почках и играет важную роль в том, как организм использует энергию. Он также помогает снизить боль в мышцах после тяжелой тренировки. Фосфор необходим для роста, восстановления и «ремонта» всех тканей и клеток, а также для производства генетических строительных блоков, ДНК и РНК. Фосфор также необходим, чтобы помочь сбалансировать и использовать другие витамины и минеральные вещества, включая витамин D, йод, магний и цинк.
Применение фосфора для лечения
Эти недомогания требуют обязательного обследования врача.
Фосфаты используются так же в клизмах, как и слабительное. Большинство людей получают большое количество фосфора в рационе. Иногда спортсмены используют фосфатные добавки перед соревнованиями или тяжелыми тренировками, чтобы помочь уменьшить боль в мышцах и снизить усталость, хотя и неясно, насколько это помогает или улучшает производительность.
Фосфор в рационе
Большинство людей получают большое количество фосфора в рационе. Минеральные добавки фосфора содержатся в молоке, зернах и продуктах, богатых белком. Некоторые медицинские обстоятельства, такие как диабет, голодание, алкоголизм, может привести к тому, что уровень фосфора в организме падает.
То же самое касается условий, которые не дают людям возможности поглощать питательные вещества, это такие заболевания как болезнь Крона и целиакия. Некоторые лекарства могут вызвать снижение уровня фосфора, в том числе некоторые антациды и диуретики (мочегонные таблетки).
Усвоение фосфора
В организме уровень этого минерала регулируется почками, которые также находятся под влиянием ПТГ. Поглощение фосфора может быть уменьшено путем антацидов, железа, алюминия или магния, который может образовывать нерастворимые фосфаты, которые выводятся с калом. Кофеин вызывает увеличение вывода фосфора почками.

Пищевые источники фосфора
Продукты, богатые белком, такие как мясо, птица, рыба, яйца, молочные продукты, орехи и бобовые, являются хорошим источником фосфора. Другие источники включают цельное зерно, картофель, сухофрукты, чеснок, а также газированные напитки.
Поскольку фосфор входит в состав всех клеток, легко найти пищу, особенно животного происхождения, которая может обеспечить организм фосфором. Большинство белковых продуктов – продукты с высоким содержанием фосфора. Мясо, рыба, курица, индейка, молоко, сыр и яйца содержат его значительные количества. Большинство красного мяса и птицы содержат гораздо больше фосфора, чем кальция, от 10 до 20 раз больше, в то время как рыба обычно содержит приблизительно 2 или 3 раза больше фосфора, чем кальция. Молочные продукты содержат более сбалансированное кальций-фосфорное соотношение.
Семена и орехи также содержат высокие уровни фосфора (хотя в них гораздо меньше кальция), что и цельное зерно, пивные дрожжи, зародыши пшеницы и отруби. Большинство фруктов и овощей содержат некоторые дозы фосфора и могут помочь сбалансировать соотношение фосфора и кальция в здоровой диете.

Симптомы дефицита фосфора
Симптомы дефицита фосфора включают потерю аппетита, беспокойство, боль в костях, хрупкие кости, жесткие суставы, усталость, прерывистое дыхание, раздражительность, онемение, слабость и изменение веса. У детей это снижение роста и разрушение костей и зубов.
Слишком много фосфора в организме на самом деле вызывает больше опасений, чем слишком малое его количество. Слишком большой уровень фосфора, как правило, вызван заболеваниями почек или тем, что люди потребляют слишком много диетического фосфора и недостаточно диетического кальция.
Некоторые исследования показывают, что более высокое потребление фосфора связано с повышенным риском сердечно-сосудистых заболеваний. По мере того как количество фосфора повышается, возникает большая потребность в кальции. Тонкий баланс между кальцием и фосфором необходим для правильной плотности костей и профилактики остеопороза.
Доступные формы фосфора
Элементный фосфор белое или желтое восковое вещество, которое горит при контакте с воздухом. Фосфор высоко токсичен и используется в медицине только в качестве гомеопатического лечения. По этому причине вы должны принимать препараты с фосфором только под руководством квалифицированного специалиста. Вместо этого, медицинские работники могут использовать один или несколько из следующих неорганических фосфатов, которые не являются токсичными при типичных нормальных дозах:

Педиатрические дозы фосфора
Дозы фосфора для взрослых
| Взрослые 19 лет и старше | 700 мг |
| Беременные и кормящие женщины в возрасте до 18 лет | 1250 мг |
| Беременные и кормящие женщины 19 лет и старше | 700 мг |

Фосфор для пожилых людей (51 год и старше)
В настоящее время нет никаких доказательств того, что дозы фосфора для пожилых людей отличаются от доз молодых людей (700 мг / сут). Хотя некоторые поливитаминные / минеральные добавки содержат более чем на больше 15% текущей суточной дозы фосфора, разнообразная диета может легко обеспечить адекватную дозу фосфора для большинства пожилых людей.
Питательные взаимодействия фосфора с другими элементами
Исследования в США 11 взрослых мужчин обнаружили, что диета с высоким содержанием фруктозы (20% от общего числа калорий) привела к увеличению их мочевого пузыря, потере фосфора и отрицательному балансу фосфора (например, ежедневные потери фосфора были выше, чем его суточная доза). Этот эффект был более выраженным, когда рацион мужчин содержал низкий уровень магния.
Выводы данного исследования очень важны, поскольку потребление фруктозы в США растет быстрее после введения в 1970 году богатого фруктозой кукурузного сиропа, в то время как потребление магния за последнее столетие снизилось.
Кальций и витамин D
Фосфор легко всасывается в тонком кишечнике, и любой избыток фосфора выводится через почки. Регулирование содержания кальция в крови и фосфора взаимосвязаны через действие паратиреоидного гормона (ПТГ) и витамина D. Небольшое снижение в крови уровня кальция (например, в случае недостаточного потребления кальция) воспринимается паращитовидными железами, что приводит к повышенной секреции паратиреоидного гормона (ПТГ).
Этот гормон стимулирует превращение витамина D в его активную форму (кальцитриол) в почках.
Повышение вывода фосфора с мочой является выгодным, в результате чего уровень кальция в крови снижается до нормального, потому что высокий уровень в крови фосфата подавляет превращение витамина D в его активную форму в почках.
Насколько высокое потребление фосфора вредно для здоровья костей?
Некоторые исследователи обеспокоены увеличением количества фосфатов в пище, которую можно отнести к фосфорной кислоте в безалкогольных напитках и фосфатных добавках в ряде продуктов. Поскольку фосфор не так жестко регулируется организмом как кальций, сывороточный уровень фосфатов может немного подняться с высоким содержанием фосфора, особенно после еды.
Высокий уровень фосфатов в крови уменьшают образование активной формы витамина D (кальцитриола) в почках, снижение содержания кальция в крови и может привести к увеличению PTH-релиза паращитовидных желез. Тем не менее, высокий уровень фосфора также может привести к снижению вывода кальция с мочой. Повышенный уровень ПТГ может оказать неблагоприятное воздействие на кости с содержанием минералов, но этот эффект наблюдался лишь у людей, сидящих на диетах с высоким содержанием фосфора и низким содержанием кальция.
Кроме того, аналогично повышенные уровни ПТГ были зарегистрированы в диетах с низким содержанием кальция, но с малым содержанием фосфора. В недавнем исследовании молодых женщин ученые не обнаружили никаких неблагоприятных эффектов богатой фосфором диеты (3.000 мг / сут). Она не воздействовала негативно на кости, уровень гормонов и биохимические маркеры костного рассасывания, даже когда диетическое потребление кальция было сохранено почти до 2000 мг / день.
В настоящее время нет убедительных доказательств того, что диетические дозы фосфора могут отрицательно повлиять на минеральную плотность костной ткани. Тем не менее, замена фосфатсодержащих безалкогольных напитков и закусок из молока и других продуктов, богатых кальцием, действительно представляет серьезную опасность для здоровья костей.
Возможные взаимодействия фосфора
Если вы в настоящее время проходите лечение с любым из нижеперечисленных препаратов, вы не должны использовать фосфор-препараты, не посоветовавшись с вашим лечащим врачом.
Алкоголь может выщелачивать фосфор из костей и вызывает низкий его уровень в организме.
Антациды, содержащие алюминий, кальций или магний (например, Mylanta, Amphojel, маалокс, Riopan, и Alternagel) могут связывать фосфаты в кишечнике. Если использовать эти антациды в долгосрочной перспективе, это может привести к низкому уровню фосфатов (гипофосфатемии).
Некоторые противосудорожные препараты (в том числе фенобарбитал и карбамазепин или Tegretol) могут снизить уровень фосфора и увеличение уровня щелочной фосфатазы, фермента, который помогает удалить фосфат из организма.
Препараты желчной кислоты снижают уровень холестерина. Они могут уменьшить пероральную абсорбция фосфатов с пищей или добавками. Оральные добавки фосфата должны быть приняты, по крайней мере, за 1 час до или через 4 часа после этих препаратов. Желчная кислота включает:
Кортикостероиды, в том числе преднизолон или метилпреднизолон (Медрол), повышают уровень фосфора в моче.
Высокие дозы инсулина могут снизить уровни фосфора у людей с диабетическим кетоацидозом (состояние, вызванное тяжелой недостаточностью инсулина).
Калий или калийсберегающие диуретики
Использование фосфорных добавок вместе с калием или калийсберегающими диуретиками могут привести к слишком большому уровню калия в крови (гиперкалиемия). Гиперкалиемия может стать серьезной проблемой, в результате чего возникают опасные для жизни нарушения сердечного ритма (аритмии). Калий и калийсберегающие диуретики включают:
Это препараты, называемые ангиотензин-превращающим ферментом (АПФ), используемые для лечения высокого кровяного давления, они могут снизить уровень фосфора. Они включают:
Другие медикаменты
Другие препараты могут тоже снижать уровень фосфора. Они включают циклоспорин (используется для подавления иммунной системы), сердечные гликозиды (дигоксин или Lanoxin), гепарины (разжижающие кровь препараты), а также нестероидные противовоспалительные препараты (например, ибупрофен или Advil).
Заменители соли, в которых также содержится высокий уровень калия и фосфора, могут привести к снижению их уровня при использовании в долгосрочной перспективе.
Меры предосторожности
Из-за возможных побочных эффектов и взаимодействий лекарств купленных по рецепту и без рецепта, вы должны принимать добавки с фософором только под наблюдением знающего врача.
Слишком много фосфата может быть токсичным для организма. Это может привести к диарее и кальцификации органов и мягких тканей, и может влиять на способность организма использовать железо, кальций, магний и цинк. Спортсмены и другие люди с большой физической активностью могут принимать добавки, содержащие фосфат, но должны делать это только изредка и под руководством и направлением врача.
Это может вызвать остеопороз (хрупкость костей), а также привести к заболеваниям десен и зубов. Баланс диетического кальция и фосфора может снизить риск развития остеопороза.