Как ортофосфорная кислота борется с ржавчиной и накипью
Ортофосфорная кислота и ее свойства
Являясь относительно слабой кислотой по сравнению со своими собратьями из таблицы химических элементов, ортофосфорная кислота является неорганическим веществом. Обычно она выглядит как россыпь мелких прозрачных кристаллов. Сами по себе, в обычных условиях, они практически не проявляют химической активности. Но как только эти кристаллы будут нагреты до температуры превышающей 42 градуса Цельсия, начнут проявляться их основные химические свойства.
Кристаллы ортофосфорной кислоты под воздействием высокой температуры начнут плавиться, благодаря чему превратятся в жидкое вещество, которое и используется в быту. Стоит отметить и то, что концентрация химически активных компонентов в ортофосфорной кислоте обычно не превышает 85%.
Наиболее важным свойством данной кислоты является ее растворимость, благодаря которой можно самостоятельно получать растворы различной концентрации в зависимости от сферы применения данного вещества. Также кислота не имеет запаха и, что немаловажно, отлично реагирует с другими химическими веществами.
Меры предосторожности
При работе с любыми кислотами самое важное — это собственная безопасность. Ортофосфорная кислота не исключение. Перед тем как использовать ее, нужно убедиться в наличии подготовленного респиратора и резиновых перчаток. Ведь ортофосфорная кислота является достаточно опасным химикатом, вызывающим ожоги кожи. Испарения этой кислоты не менее опасны: их действие может привести к сильнейшему отравлению или ожогу дыхательных путей. Стоит помнить и о том, что ортофосфорная кислота легко воспламеняется и может привести к пожару. Именно по этим причинам большинство действий с этим веществом должны проводиться на открытом воздухе или в обильно вентилируемых комнатах. Главное, не позволять кислоте попасть на кожу, но если это все-таки случилось, стоит немедленно вымыть под проточной водой пострадавший участок. В том случае, если химическому ожогу подвергся значительная часть кожи, нужно незамедлительно обратиться к врачу.
Как победить накипь? Советы опытных хозяек
Для устранения ржавчины и накипи в домашних условиях используется слабый раствор ортофосфорной кислоты. Она превращает ржавчину в черный налет, который потом можно легко очистить с металлического изделия. Также ортофосфорная кислота незаменима при устранении накипи на посуде.
Избавление от ржавчины
Большим достоинством ортофосфорной кислоты является ее способность образовывать защищающую от ржавчины пленку на изделии, а не просто избавляться от массы окислов. Процесс образования подобного защищающего барьера легко описать: кислота, разрушая оксид железа, фосфарицирует (укрепляет) верхний слой металла. После таких манипуляций на металлических изделиях часто можно наблюдать сероватую и маслянистую пленочку, которая появляется вместо ржавчины.
Существует множество способов удаления ржавчины, зависящие от степени поражения ржавчиной и величины предмета, который предстоит очистить:
Травление деталей благодаря полному погружению.
Если дома имеется достаточно ортофосфорной кислоты и большая емкость, самым простым путем избавления от ржавчины будет полное помещение изделия в смесь. Для этого следует повторить порядок выполнения работы:
Все этапы взаимосвязаны поэтому, пропустив любой из них, вы не добьетесь желаемого результата. Так, если не выполнить обезжиривание, травление будет проходить неравномерно и неочищенные участки придется повторно очищать другими способами. Метод травления с полным погружением подходит для изделий, пораженных тем или иным уровнем коррозии, однако время на очистку может увеличиться в зависимости от толщины слоя ржавчины.
Как сделать унитаз белоснежным и удалить ржавые пятна
Совет! Чтобы избежать образования нежелательного гидроксида, после промывки нужно высушить деталь, причем сушить можно каким угодно удобным путем.
Как распределить кислоту по поверхности.
Вещь, пораженная ржавчиной, может оказаться внушительных размеров, а большой тары и кислоты в достаточном объеме может под рукой не оказаться. В таком случае ортофосфорную кислоту стоит нанести прямо на деталь. Сделать это можно валиком, распылителем или кистью из натурального материала. При таком подходе очень важно брать во внимание уровень поражения ржавчиной. Когда коррозия глубоко въелась в деталь, лучшим решением будет снять верхний слой вручную или используя болгарку.
Затем проводится обезжиривание, после которого требуется распределить данный раствор кислоты по изделиям без пробелов и держать на них 2 часа. После этого нужно убрать кислоту нейтрализующей смесью, последний раз смыть и просушить. Если же коррозия является незначительной, возможно справиться не прибегая к механической очистке просто повторить процедуру несколько раз.
Избавление от коррозии на ваннах, унитазах и раковинах.
Из-за того что ортофосфорная кислота отлично борется со следами ржавой воды на санфаянсе и эмалированных поверхностях, ее используют взамен бытовой химии. Не поможет это обладателям акриловых ванн.
Порядок действий для очистки фаянсовых и эмалированных поверхностей:
Главным достоинством такого способа избавления от коррозии будет то, что эмаль не разрушается из-за трения. На заметку хозяйкам, которые применяют для этих же целей «Кока-колу»: она действует именно так благодаря ортофосфорной кислоте в составе. Таким образом, выгоднее применять ортофосфорную кислоту в правильной объёме, а продукты применять по их прямому назначению.
Способы удаления ржавых пятен на одежде в домашних условиях
Преобразователь ржавчины.
Модификатором или преобразователем ржавчины является тот же раствор ортофосфорной кислоты, но уже с некоторыми добавками. Их разделяют на несколько групп, в зависимости от этих добавок:
Что выбрать?
При выборе метода избавления от ржавчины, нужно, прежде всего, учитывать место применения кислоты. Например, чтобы очистить деталь методом полного погружения, необходимо большое количество ортофосфорной кислоты. А если требуется не только избавиться от ржавчины, но и создать подготовительный слой для нанесения лакокрасочного покрытия, то смесь, приготовленная своими руками, не подойдет. Для таких целей стоит приобрести заводской преобразователь, в котором уже будут все нужные добавки.
Как бороться с накипью?
Для начала необходимо разобраться что же такое накипь. На самом деле, это не растворенные, осевшие на деталях техники соли кальция и магния. Вот почему для их удаления прекрасно подходит кислота. Несмотря на то, что кислота чаще всего применяется лимонная, ортофосфорная кислота также будет являться отличным средством, ведь ее часто применяют в промышленных масштабах. Так, чаще всего ее используют для удаления накипи из теплообменного оборудования.
Для борьбы против накипи следует смешать слабый раствор ортофосфорной кислоты и затем залить его в емкость, пораженную накипью, например, в чайник. Этот раствор нужно оставить на час, а затем тщательно промыть изделие от кислоты. Если этот способ не помогает, попробуйте повторить данную процедуру или слегка нагреть раствор. Это повысит его эффективность.
Фосфорная кислота [H3PO4]: Структура | Свойства | Применение
В чистом виде фосфорная кислота представляет собой бесцветное твердое вещество. В менее концентрированном виде это вязкая жидкость без запаха с плотностью 1,885 г/мл. Обычно она нелетучая и нетоксична, но 85-процентный раствор по-прежнему может повредить глаза и вызвать сильное раздражение кожи.
Давайте копнем глубже и выясним, как образуется фосфорная кислота, как она выглядит на молекулярном уровне, каковы ее физические и химические свойства и где она используется.
Профиль фосфорной кислоты
Молярная масса: 97,994 г/моль
Внешний вид: густая бесцветная жидкость.
Точка кипения: 212 °C
Точка плавления: 42,35 °C (кристаллического твердого вещества)
Динамическая вязкость: от 2,4 до 9,4 сантипуаз (85% водный раствор).
Плотность: 1,83 г / см 3 (твердое вещество); 1,68 г / см 3 (85% водный раствор при 25 °C)
Структура
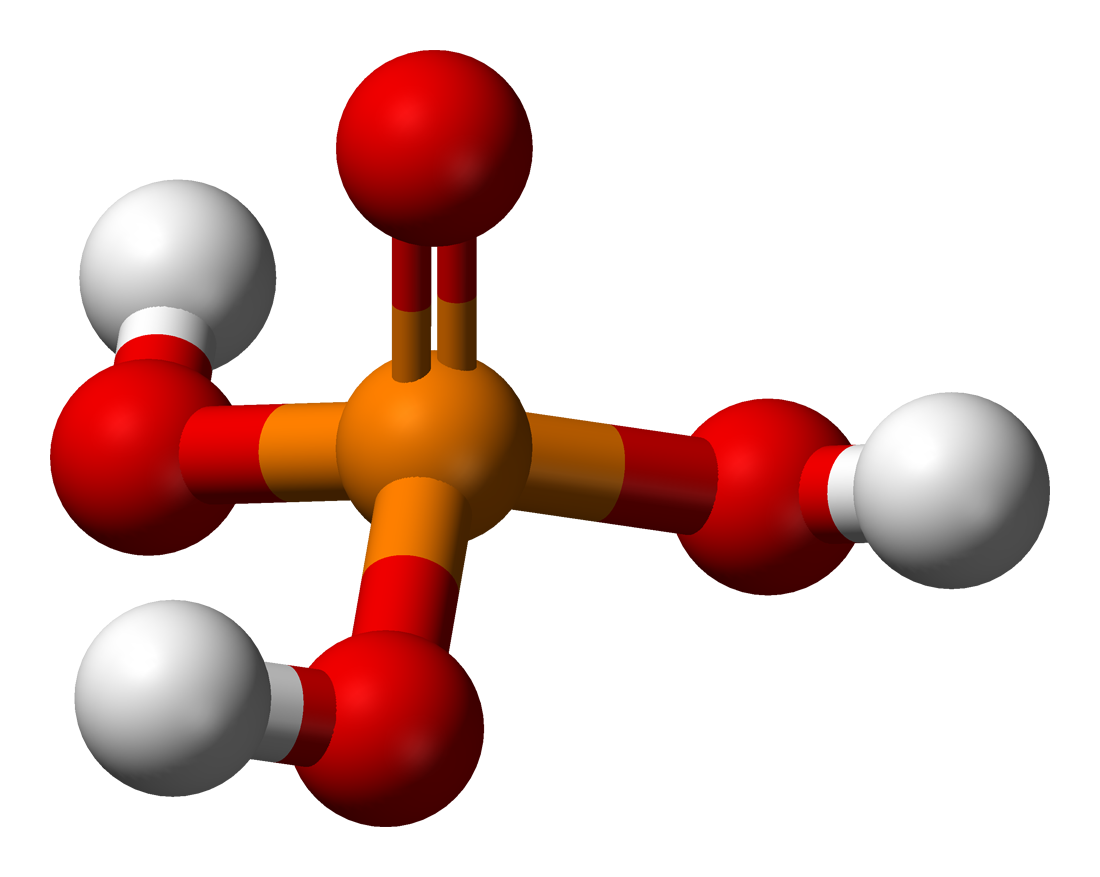
Соединение H3PO4 имеет в общей сложности 32 валентных электрона. Поскольку фосфор является наименее электроотрицательным, он помещается в центре. Атомы водорода присоединяются к внешней стороне атомов кислорода, образуя он-Группы.
В этой структуре каждый атом имеет полную внешнюю оболочку: атомы фосфора и кислорода имеют восемь валентных электронов, а атомы водорода имеют вокруг себя два валентных электрона.
В структуре все еще есть 32 валентных электрона, и каждый атом имеет формальный заряд, равный нулю. Таким образом, это наиболее вероятная или вероятная структура Льюиса для H3PO4.
Соединение содержит 3 одинарные связи ОН, 3 одинарные связи PO и 1 двойную связь P = O. Каждая одинарная связь является сигма-связью, а двойная связь состоит из сигма-связи и пи-связи.
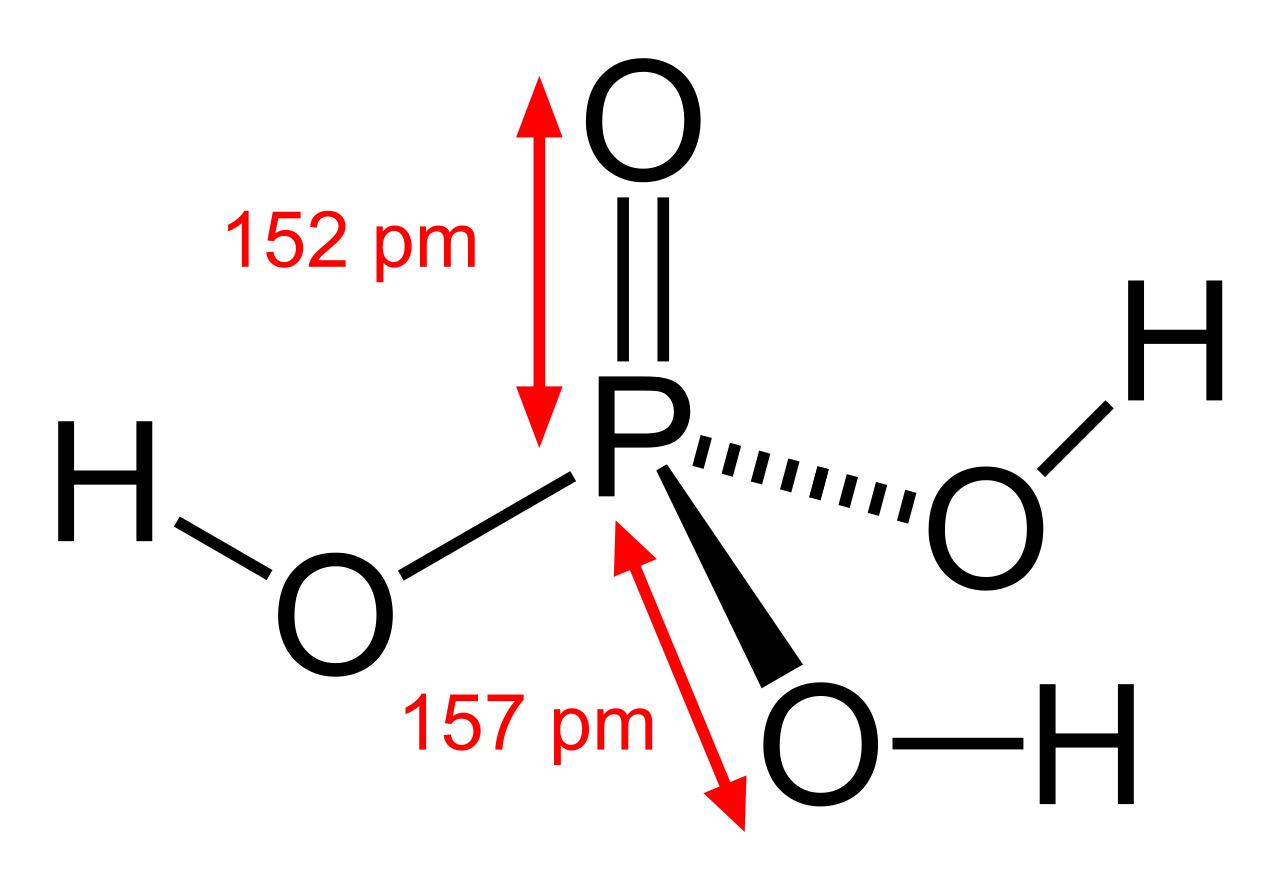
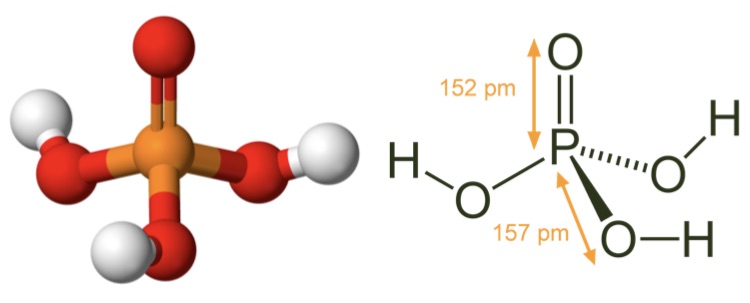
Фосфорная кислота: шарообразная модель и размеры структурной формулы
Молекулярная геометрия PO (OH)3 является тетраэдрической, а кристаллическая структура-моноклинной. А поскольку распределение зарядов на центральных атомах асимметрично, то молекула считается полярной.
Последние достижения в области нанотехнологий, включая методы поглощения рентгеновских лучей вблизи краев и методы рассеяния рентгеновских лучей под большим углом, позволили ученым точно определить структуру фосфорной кислоты. Расстояние связи P=O в структуре близко к 152 пикометрам, и расстояния P=O-O были уточнены до 309 пикометров, с углом связи близким к тетраэдрическому.
Как она производится?
Фосфорная кислота может быть синтезирована либо мокрым способом, либо термическим способом.
В последнем в качестве сырья используются воздух, вода и элементарный фосфор. Он включает в себя три важных этапа: сгорание, увлажнение и запотевание. Вот как это происходит:
Во-первых, жидкий элементарный фосфор сжигается в камере сгорания при высоких температурах в диапазоне от 1650 до 2760 °C. Эта реакция окисления происходит в окружающем воздухе и производит пятиокись фосфора.
Затем продукт гидратируют водой с образованием сильной фосфорной кислоты (в жидком состоянии).
На последнем этапе для удаления фосфорно-кислотного тумана из потока дымовых газов используются высоконапорные каплеуловители.
Концентрация фосфорной кислоты, синтезированной в этом процессе, обычно составляет от 75 до 85 процентов. Такие уровни концентрации необходимы для производства высококачественной химической продукции. Несколько эффективных установок извлекают чрезвычайно концентрированную фосфорную кислоту (до 99,9%), используя тот же тепловой процесс.
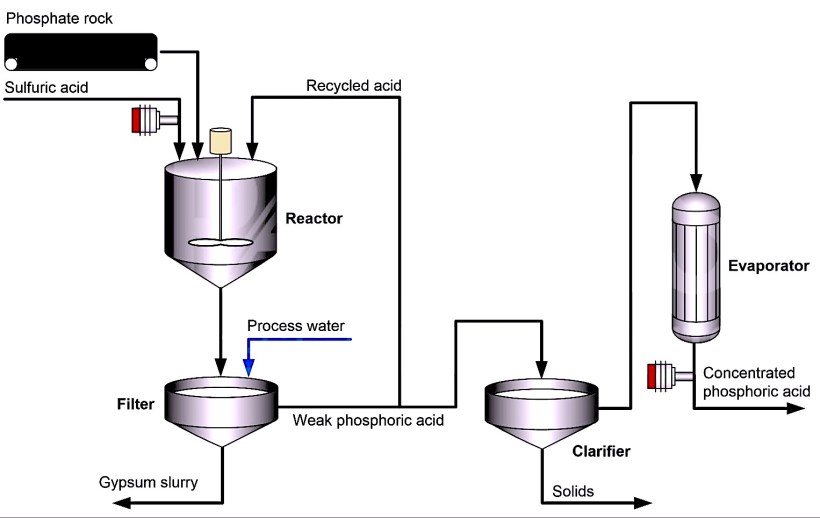
Однако почти 80% фосфорной кислоты производится мокрым способом. В этом методе серная кислота обрабатывается природным фосфатсодержащим минералом, таким как гидроксиапатит.
Минерал высушивают, крошат, а затем подают в реактор вместе с серной кислотой. В результате реакции сульфат сливается с кальцием (из минерала), образуя сульфат кальция (гипс).
Затем добавляется обработанная вода, и гипс вместе с другими нерастворимыми примесями удаляется через фильтр. Фосфорная кислота, полученная этим мокрым способом, содержит 25-30% пятиокиси фосфора.
Обычно эта кислота дополнительно концентрируется, чтобы соответствовать требованиям, предъявляемым к производству удобрений. В большинстве случаев фосфорная кислота концентрируется до 40-55% пятиокиси фосфора с помощью двух / трех вакуумных испарителей.
Свойства
Чистая фосфорная кислота в лаборатории выглядит как плотное, бесцветное, бесформенное кристаллическое твердое вещество, которое плавится при температуре 42,35 °C. Ее физические свойства зависят от чистоты, концентрации кислоты, а также от температуры, при которой вы ее видите.
Фосфорная кислота менее агрессивна и менее опасна по сравнению с азотной и серной кислотами. Это негорючее вещество как в жидкой, так и в твердой форме.
Когда кислота подвергается воздействию тепла, а затем охлаждается до комнатной температуры, она образует прозрачное, хрупкое стекло. После такого воздействия тепла состав кислоты остается прежним.
Обычно фосфорная кислота выпускается в виде бесцветного сиропа с концентрацией в воде 85 процентов и плотностью 1,885 граммов на миллилитр.
В водном растворе фосфорная кислота действует как трипротовая кислота, имеющая три ионизируемых атома водорода. Соединение может потерять эти атомы в виде протонов (ионов H + ).
Кислота растворима как в воде, так и в этаноле. Однако большинство ее солей не растворимы в воде, если нет сильной минеральной кислоты.
Области применения
Фосфорная кислота имеет несколько важных применений. Ее соли, такие как фосфаты аммония и кальция, широко используются в качестве удобрений. Кислота используется для производства электролитов, средств для удаления ржавчины, модификаторов рН, травителей, бытовых чистящих средств и дезинфицирующих средств.
Поскольку это вещество нетоксично и имеет умеренно кислую природу, оно также используется в напитках, пищевых ароматизаторах, косметике, средствах для ухода за зубами и кожей. Давайте подробнее рассмотрим, чем полезна фосфорная кислота.
В менее концентрированной форме она используется для производства различных видов безопасных фосфорных удобрений, которые помогают растениям расти. Фактически, почти 90% синтезированной фосфорной кислоты используется в качестве удобрений.
Многие безалкогольные напитки, в том числе Coca-Cola, содержат фосфорную кислоту. Это придает напитку слегка кисловатый вкус. Несмотря на то, что его концентрация достаточно низкая, экстремальный прием таких напитков может вызвать эрозию зубов и даже привести к образованию почечных камней.
Фосфорная кислота в качестве электролита имеет полезные характеристики, такие как хорошая ионная проводимость, низкая летучесть, стабильность при относительно высоких температурах и устойчивость к диоксиду углерода и монооксиду углерода.
Поскольку чистая фосфорная кислота обладает высокой протонной проводимостью и превосходной термостабильностью, полибензимидазол (PBI), допированный фосфорной кислотой, является наиболее многообещающим среди мембран на основе PBI, которые могут обеспечить хорошую производительность топливных элементов даже при низком уровне увлажнения и температуре 200 °С.
Специфическое применение фосфорной кислоты:
Глобальный рынок
Многие развивающиеся страны начали сосредотачиваться на увеличении добычи фосфатов и производства фосфатов. Правительства некоторых стран уже сотрудничали с различными поставщиками по всему миру для создания заводов по добыче минералов для производства фосфорной кислоты.
В 2019 году объем мирового рынка фосфорной кислоты оценивался в 45,85 миллиарда долларов. Ожидается, что к 2027 году он достигнет более 61 миллиарда долларов, а совокупный годовой темп роста составит 3,7%.
Рынок подразделяется на Азиатско-Тихоокеанский регион, Европу, Северную Америку, Латинскую Америку, Ближний Восток и Африку. Ожидается, что в ближайшем будущем Азиатско-Тихоокеанский регион будет доминировать на мировом рынке. Рост рынка фосфорной кислоты в этих регионах будет дополнительно подпитываться развитым сельскохозяйственным сектором Индии и Китая.
Применение ортофосфорной кислоты
Нередко металл и изделия из него подвергаются характерной «болезни», которая проявляется в виде рыжего налета, разъедающего металл. Речь идет о ржавчине. Ее образование происходит благодаря воздействию на поверхность металлического изделия углекислого газа, кислорода и воды. Безусловно, для того чтобы продлить срок службы изделия из металла необходимо как можно скорее начать борьбу с коррозией. Помочь в этом может обработка ортофосфорной кислотой.
Характеристики ортофосфорной кислоты
Ортофосфорная или попросту фосфорная кислота представляется в виде продукта, имеющего неорганическое происхождение. В условиях нормальной комнатной температуры ортофосфорная кислота имеет вид небольших ромбовидных кристалликов.
Чаще всего же ортофосфорная кислота имеет вид сиропообразного 85%-процентного раствора, не имеющего характерного запаха. Кристаллики ортофосфорной кислоты довольно хорошо растворяются в воде или этаноле.
Уравнение ортофосфорной кислоты
Применяется ортофосфорная кислота в следующих отраслях человеческой деятельности:
Если температура окружающей среды, например, в условиях лабораторных исследований превышает показатели в 213 градусов Цельсия, ортофосфорная кислота преобразуется в пирофосфорную кислоту. Состав ортофосфорной кислоты и ее химическая формула, соответственно, изменяется.
Таблица 1. Физико-химические показатели ортофосфорной кислоты согласно ГОСТ 10678-76.
| Наименование показателя | Норма | ||
|---|---|---|---|
| Марка А | Марка Б | ||
| 1-й сорт | 2-й сорт | ||
| 1. Внешний вид | Бесцветная жидкость прозрачная в слое 15-20 мм при рассмотрении на белом фоне | Бесцветная или со слабо-желтым оттенком жидкость в слое 15-20 мм при рассмотрении на белом фоне | Бесцветная или окрашенная жидкость с оттенком от слабо-желтого до коричневого, не прозрачная в слое 15-20 мм при рассмотрении на белом фоне |
| 2. Массовая доля ортофосфорной кислоты (H3PO4), %, не менее | 73 | 73 | 73 |
| 3. Массовая доля хлоридов, %, не более | 0,005 | 0,01 | 0,02 |
| 4. Массовая доля сульфатов, %, не более | 0,010 | 0,015 | 0,020 |
| 5. Массовая доля нитратов, %, не более | 0,0003 | 0,0005 | 0,0010 |
| 6. Массовая доля железа, %, не более | 0,005 | 0,010 | 0,015 |
| 7. Массовая доля тяжелых металлов сероводородной группы, %, не более | 0,0005 | 0,002 | 0,005 |
| 8. Массовая доля мышьяка, %, не более | 0,0001 | 0,006 | 0,008 |
| 9. Массовая доля восстанавливающих веществ, %, не более | 0,1 | 0,2 | Не нормируется |
| 10. Наличие метафосфорной кислоты | Выдерживает испытание | ||
| 11. Массовая доля взвешенных частиц, %, не более | Выдерживает испытание | 0,3 | |
| 12. Наличие желтого фосфора | Выдерживает испытание | Не нормируется | |
Таблица 2. Физико-химические показатели ортофосфорной кислоты согласно ГОСТ 6552-80.
| Наименование показателя | Норма | ||
|---|---|---|---|
| Химически чистый (х.ч.) ОКП 26 1213 0023 08 | Чистый для анализа (ч.д.а.) ОКП 26 1213 0022 09 | Чистый (ч.) ОКП 26 1213 0021 10 | |








 Современная наука довольно часто позволяет использовать одно и то же химическое вещество или один и тот же химический состав в совершенно различных целях. То же самое можно сказать и о вариантах применения ортофосфорной кислоты.
Современная наука довольно часто позволяет использовать одно и то же химическое вещество или один и тот же химический состав в совершенно различных целях. То же самое можно сказать и о вариантах применения ортофосфорной кислоты. Как и любая другая кислота, ортофосфорная требует от человека предельной внимательности, аккуратности и выполнения всех правил безопасности при работе с кислотами.
Как и любая другая кислота, ортофосфорная требует от человека предельной внимательности, аккуратности и выполнения всех правил безопасности при работе с кислотами. Ортофосфорная кислота, влияние которой на ржавчину широко известно, может применяться как в промышленных масштабах, так и для удаления коррозии металла в домашних условиях. Разумеется, что подобные действия должны проводиться с учетом описанных выше правил безопасности.
Ортофосфорная кислота, влияние которой на ржавчину широко известно, может применяться как в промышленных масштабах, так и для удаления коррозии металла в домашних условиях. Разумеется, что подобные действия должны проводиться с учетом описанных выше правил безопасности. Учитывая, что существует несколько вариантов очищения металла с применением ортофосфорного соединения, следует рассмотреть каждый из них подробнее.
Учитывая, что существует несколько вариантов очищения металла с применением ортофосфорного соединения, следует рассмотреть каждый из них подробнее.





