Болезнь Альцгеймера: ген, от которого я без ума
Болезнь Альцгеймера, настигающая большинство людей в старости, является одной из самых острых проблем здравоохранения
Автор
Редакторы
В начале XX века с помощью немецкого психиатра Алоиса Альцгеймера мир узнал о существовании новой нейродегенеративной болезни. И хотя долгое время исследователи не воспринимали генетическую предрасположенность в качестве важного фактора для развития болезни Альцгеймера, вскоре ситуация изменилась. Однако и сейчас о природе этого заболевания идут ожесточенные споры: кто же во всем виноват — β-амилоид или APOE4?
Бета-амилоид, образующий при болезни Альцгеймера нерастворимые бляшки в нервных клетках, традиционно считался основной причиной нейротоксичности при этом заболевании, однако в действительности дело обстоит не так просто. В частности, токсичными могут быть не только фибриллярные, но и промежуточные сферические агрегаты Aβ (см. «Альцгеймеровский нейротоксин: ядовиты не только фибриллы» [14]), на вероятность развития БА положительно влияет недосып (см. «Новый шаг к пониманию болезни Альцгеймера: возможно, недосыпание является одним из факторов риска» [15]), ну а на сладкое — в реальности бета-амилоид может быть вообще не нейротоксином, а компонентом врождённого иммунитета в нервной системе человека (см. «Возможно, β-амилоид болезни Альцгеймера — часть врождённого иммунитета» [16]). — Ред.
Профессор Роузес сразу понял, что его коллега нашел нечто важное. Двумя годами ранее ими было обнаружено, что экспрессия некоторых генов из хромосомы 19 способствует развитию деменции, а поскольку Роузес знал, что ген, кодирующий ApoE, также находится на этой хромосоме, его молниеносно осенила идея участия ApoE в развитии болезни Альцгеймера (БА).
В организме человека есть три варианта гена APOE, кодирующих изоформы белка Е2, Е3 и Е4, и Роузес решил выяснить их влияние на развитие болезни Альцгеймера. Для определения отдельных аллелей нужно было провести полимеразную цепную реакцию (ПЦР) [17]. Так как ученый имел весьма скромный опыт работы с ПЦР, он хотел привлечь в свою команду нейрофизиологов, но получил отказ: хотя они и были заняты охотой за генами, которые лежат в основе болезни Альцгеймера, АРОЕ показался им неподходящим кандидатом. Роузес вспоминает, как позже в лаборатории ходили разговоры: «. начальник совсем потерял голову от своих безумных идей».
Но Роузес не сдавался. Он попросил помощи у своей жены, генетика Энн Сондерс (Ann Saunders), которая использовала ПЦР в своих исследованиях. Она только что родила дочь и была в декретном отпуске, и потому они заключили соглашение. «Она сделала все эксперименты, пока я присматривал за ребенком», — говорит профессор. В течение трех недель супруги собрали данные, которые в дальнейшем легли в основу серии знаковых публикаций. Они выяснили, что аллель APOE4 способствует развитию БА [1].
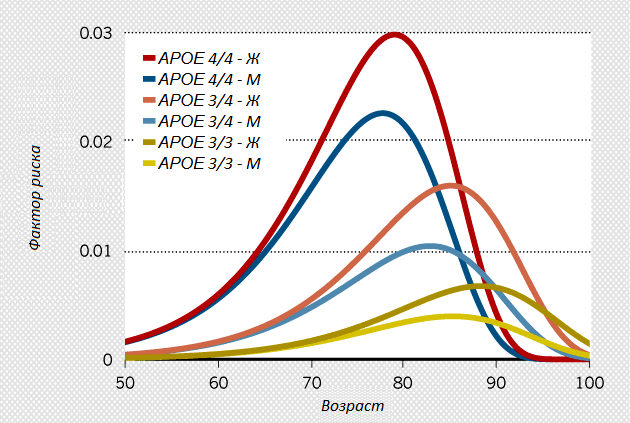
Сегодня, двадцать лет спустя, APOE4 остается ведущим фактором риска для наиболее распространенной формы деменции. Наследование одной копии APOE4 вчетверо повышает риск возникновения заболевания, двух копий — в 12 раз (рис. 1). Однако данные Роузеса в основном не воспринимали всерьез или критиковали. Впоследствии, даже когда мнение об ApoE поменялось, большинство ученых все равно продолжали работать с β-амилоидом, как бы «зациклившись» на классике. Но некоторые лаборатории все равно исследовали ApoE, несмотря на равнодушие финансирующих учреждений и научного сообщества и на отсутствие ресурсов, необходимых для проведения масштабных экспериментов.
Рисунок 1. Носители аллеля APOE4 более подвержены развитию болезни Альцгеймера по сравнению с теми, кто унаследовал две копии аллеля APOE3
Долгое время было неизвестно, какие функции белок ApoE выполняет в головном мозге, и постепенно эта головоломка стала интересовать многих нейрофизиологов. Интерес к липопротеинам продолжал расти, — отчасти потому, что клинические испытания лекарств, нацеленных на β-амилоид, часто заканчивались неудачей. Многие исследователи начали скрупулезно изучать белок ApoE4 и, как следствие, привлекли внимание фармацевтических компаний. «Амилоидные подходы» постепенно перестали использовать, зато начали разрабатывать препараты, направленные на аполипопротеин.
«Несмотря на отсутствие уверенных доказательств, амилоидная гипотеза стала в свое время сильным научным постулатом», — говорит Завен Хачатурян, президент некоммерческой компании «Предотвратим Болезнь Альцгеймера» (Prevent Alzheimer’s Disease 2020) и бывший координатор деятельности, связанной с исследованием БА в Национальных институтах здоровья США. До недавнего времени, по его словам «никто не пытался задать фундаментальный вопрос — правильно ли мы определили основную предпосылку болезни?».
Жесткая конкуренция
Существуют разные доводы относительно того, почему открытие Роузеса было проигнорировано. Многие сходятся во мнении, что генетик выбрал неудачное время для обнародования своих результатов. В 1991 году Джон Харди (John Hardy) и Дэвид Олсоп (David Allsop) предложили «гипотезу амилоидного каскада». Они утверждали, что болезнь Альцгеймера является результатом аномального накопления β-амилоидных бляшек в тканях мозга [3]. Научное сообщество поддержало предложенную идею, которую вскоре начали активно финансировать.
Но Роузес не подписался под этой теорией: «. амилоиды являются одними из многих веществ, которые формируют бляшки; в конечном итоге они разрушают клетки и вызывают атрофию мозга. У меня и мысли не было, что это было причиной деменции». Говоря так, он, возможно, хотел скрыть возможную связь ApoE/Аβ, и случайно создал конкуренцию между двумя гипотезами за финансирование. К сожалению, Роузес так и не получил гранты для работы с ApoE.
Были и технические препятствия для изучения ApoE. Белок входит в состав различных липопротеинов плазмы крови и является довольно сложной фармакологической мишенью при работе с головным мозгом. ApoE имеет липофильную часть и поэтому при биохимическом анализе может агрегировать с другими молекулами. Работа с такими белками требует глубокого понимания биохимии липопротеинов и методик работы с ними.
Три оставшихся препарата, которые нацелены на β-амилоид, в настоящее время проходят испытания на больных, а также на людях с высоким риском БА, у которых еще не развились симптомы. Позитронно-эмиссионная томография показала, что мозг подопытных с высоким риском развития БА отличается от здорового мозга за десятилетия (!) до того, как начинает накапливаться β-амилоид или разрушаться нейроны [4]. В результате исследований, которые будут проводиться в течение следующих шести лет, ученые поймут, способны ли данные лекарства отсрочить наступление заболевания или нет. Среди исследователей и представителей фармацевтической индустрии появилось ощущение, что это — последний шанс для амилоидной гипотезы. На фоне этих сомнений ApoE вновь оказался в центре внимания.
По словам Мака, если испытания закончатся неудачей, ученые будут отчитываться перед инвесторами, предоставляя все данные доклинических и ранних клинических испытаний. Он надеется, что исследователи АроЕ вскоре получат большое преимущество. Несмотря на препятствия в этой области, у ученых продолжает крепнуть подозрение, что именно ApoE4 является предпосылкой для возникновения болезни. Этот факт подтверждают группы Мака и Гольцмана (Holtzman) в опытах на трансгенных мышах, которые несут в себе изоформы ApoE человека.
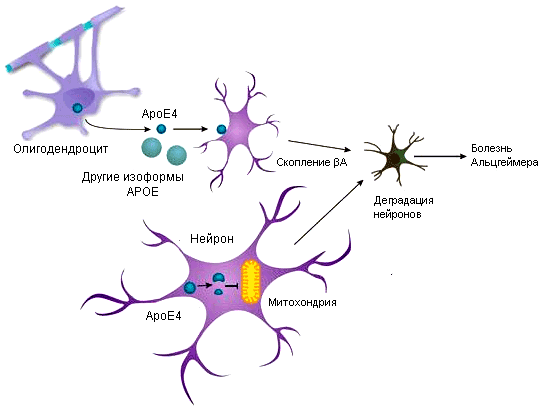
Скорее всего, ApoE участвует в развитии БА двумя различными путями, один из которых — амилоид-зависимый. И у животных, и у человека ApoE4 способствует отложению Aβ в мозговом веществе, в то время как ApoE3 считается «нейтральной» изоформой, а ApoE2 — «защитной» формой, уменьшающей накопление бляшек [5]. «Это достаточно убедительные данные», — говорит Хольцман.
Другой механизм не предусматривает взаимосвязи с амилоидом. Когда нейроны находятся в состоянии стресса, они экспрессируют ApoE для своего восстановления. «Плохая» форма — ApoE4, — как правило, разрушается на токсичные фрагменты, которые повреждают митохондрии и модифицируют цитоскелет.
Рисунок 2. Две расходящиеся гипотезы о том, как АроЕ способствует болезни
Оценить вклад этих двух механизмов в риск развития болезни Альцгеймера крайне сложно, говорит Хольцман, но он и его коллеги считают, что трансформация вредоносной изоформы ApoE в «нейтральную» может стать перспективным подходом для лечения БА. В Гладстоне исследователи начали изучать этот вопрос, и уже найдены небольшие регуляторные молекулы, которые трансформируют ApoE4 в ApoE3-образный белок и тем самым снижают аномальную фрагментацию первого [7]. В культуре клеток даже низкие концентрации этих молекул могут уменьшить разрушение митохондрий и дисфункцию нейронов [8]. В настоящее время эти молекулы проходят испытания на животных, и если они в конечном счете окажутся безопасными и эффективными, врачи будут назначать их пациентам, предрасположенных к БА, так же, как статины — больным с высоким уровнем холестерина и с повышенным риском сердечно-сосудистых заболеваний.
Более чем достаточно
Несмотря на отсутствие грантов на исследования ApoE, Роузес никогда не сдавался. Но через несколько лет, когда его группа обнаружила связь между ApoE и болезнью Альцгеймера, он устал от постоянного денежного противостояния и оставил науку. Проработав в фармацевтической индустрии десять лет, в течение которых он не переставал исследовать ApoE, в 2008 году он снова возвращается в Дьюковский университет.
В 2009 году его группа описала участок некодирующей ДНК с геном TOMM40, который располагается рядом с APOE на девятнадцатой хромосоме. Этот участок ДНК (сокращенно — 523) варьирует по длине и, в зависимости от этого, может определять уровень экспрессии генов TOMM40 и АРОЕ [9].
По словам Роузеса, это было важное открытие, так как белок, кодируемый геном TOMM40 — Tom40, — является необходимым для «здоровых» митохондрий. Tom40 образует канал во внешней митохондриальной мембране, через который импортируются белки, необходимые для нормального деления этой органеллы. «Мы знали о существовании такого механизма в течении 10 лет, — говорит ученый, — но то, что он приводит к болезни Альцгеймера, мы и не подозревали».
Роузес продолжал утверждать, что участок 523 можно использовать для разработки терапии и более точного предсказания болезни. Подавляющее большинство людей рискует встретиться со своим Альцгеймером, если только проживет достаточно долго, а ведь носителями аллеля APOE4 являются только 25% населения. Значит, тест на носительство этого аллеля никогда не будет до конца точным предиктором. Но генотипирование по обоим генам — АРОЕ и TOMM40 — может существенно увеличить точность, как говорит Роузес. В его лаборатории открыли, что APOE3 — наиболее частая изоформа — обычно наследуется вместе или с коротким, или с очень длинным участком 523. И у носителей двух аллелей APOE3 возраст наступления заболевания будет зависеть от конкретного варианта участка 523, наследуемого вместе с APOE.
Некоторым лабораториям удалось найти доказательства, подтверждающие гипотезу Роузеса, однако у других повторить исследования на TOMM40 так и не удалось, и возникли сомнения в реальности влияния этого гена на риск развития БА [10]. Однако Роузес не сомневается в правильности своих гипотез и считает, что геномные исследования, не подтвердившие его результатов, обладали недостаточной силой для выявления сцепливания TOMM40 и болезни Альцгеймера.
Роузес надеется, что вскоре он сможет подкрепить свои результаты клиническими исследованиями, которые будут проводиться в основанной им компании Zinfandel Pharmaceuticals. Вместе с японской фармацевтической компанией Takeda Зинфандель в настоящее время финансирует фазу III клинических испытаний (под названием TOMMORROW), призванную проверить идеи Роузеса на деле. TOMMORROW должна оценить риски развития БА в зависимости от возраста пациента и вариантов APOE и TOMM40. Для запуска программы будут отобраны около 6000 здоровых пожилых людей, и исследования будут продолжаться около 5 лет.
Программа будет также исследовать возможность того, что пиоглитазон — препарат для лечения пациентов с сахарным диабетом 2 типа, — в малых дозах будет задерживать развитие БА у лиц, отнесенных к группе высокого риска развития болезни Альцгеймера. Проверка этой идеи вызвана тем, что опубликованы результаты опытов на животных и даже на людях, которые говорят о способности пиоглитазона предотвращать или уменьшить патологию и симптомы, связанные с болезнью Альцгеймера [11]. Роузес думает, возможный механизм этого — стимуляция деления митохондрий.
Даже если получить мощное лекарство против болезни Альцгеймера так и не удастся, толк в этих испытаниях все равно будет: научившись задерживать развитие БА хотя бы на два года, можно уменьшить число больных в США через 50 лет на 2 млн. человек, что очень и очень неплохо [12]. Кроме того, результаты этих испытаний заставят исследователей всего мира по-новому взглянуть на деменцию. Такое сложное расстройство, как болезнь Альцгеймера, нельзя изучать только с одной стороны, — пусть и включающей ApoE4 или еще что-нибудь. По-видимому, нейрофизиологи близки к тому, чтобы признать ограниченность своих прежних взглядов и частично пересмотреть их, направив исследования по новым дорожкам, в конце которых будет разгадка проблемы, лишающей нас ума.
По материалам рубрики News Feature в Nature [13].
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№03 2010
Эпигенетика: 8% генома человека состоит из привнесенных вирусов №03 2010
Кафедра психиатрии ФУВ РГМУ, Москва
Моя предыдущая статья была написана около года назад, и в ней лишь вскользь упоминается об эпигенетике, а между тем эта молодая наука уже сейчас сулит нам поистине революционные изменения в нашем представлении о природе психических заболеваний и шизофрении в частности.
Не так давно был фактически открыт необычный вирусный код внутри ДНК человека.
Калифорнийские ученые группы Pacific Biosciences представили новую технологию расшифровки так называемой эпигенетической информации – «скрытого слоя» наследственности. Это данные, которые не определяются традиционными методиками, однако оказывают очень существенное влияние на то, как записанные в геноме инструкции будут реализованы.
Небольшой экскурс в историю: наука эпигенетика начала активно развиваться в конце XX века, когда ученые пришли к пониманию того, что наследственная информация заложена не только в самой последовательности ДНК, но и в определенных модификациях отдельных кодирующих «букв алфавита» – нуклеотидов.
Так, например, простое добавление метильной группы (CH3) часто приводит к инактивации модифицированного участка ДНК. Проблема до сих пор была в отсутствии у исследователей хоть сколько-нибудь потокового метода работы с эпигеномом – модифицированные нуклеотиды искали практически «с лупой».
Эпигенетическим наследованием называют наследуемые изменения в фенотипе или экспрессии генов, вызываемые другими механизмами, чем изменение последовательности ДНК (приставка эпи- означает «в дополнение»). Такие изменения могут оставаться видимыми в течение нескольких клеточных поколений или даже нескольких поколений живых существ.
В случае эпигенетического наследования не происходит изменения последовательности ДНК, но другие генетические факторы регулируют активность генов. Лучшим примером эпигенетических изменений для эукариот является процесс дифференцировки клеток. В течение морфогенеза тотипотентные стволовые клетки становятся плюрипотентными линиями клеток, которые в тканях эмбриона затем превращаются в полностью дифференцированные клетки. Единственная клетка – зигота (оплодотворенная яйцеклетка) дифференцируется в различные типы клеток: нейроны, мышечные клетки, эпителиальные клетки, клетки кровеносных сосудов и многие другие. В процессе дифференцировки активируются одни гены и инактивируются другие.
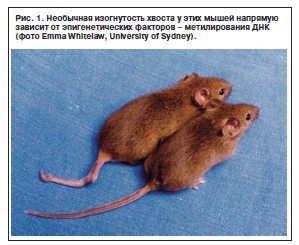
К известным эпигенетическим механизмам, помимо прионизации белков, относятся метилирование ДНК (рис. 1), ремоделирование хроматина, регуляция на уровне РНК, в частности РНК-интерференция, инактивация X-хромосомы.
Поскольку фенотип клетки или организма в целом зависит от того, какие гены транскрибируются, наследование транскрипционного статуса генов может приводить к эпигенетическим эффектам. Есть несколько уровней регуляции экспрессии генов, первый из которых – ремоделирование хроматина – комплекса ДНК и ассоциированных белков-гистонов. Ремоделирование хроматина может инициироваться посттрансляционной модификацией аминокислот гистонов, например их метилированием и химической модификацией азотистых оснований, например метилированием цитозина.
Я вспоминаю посещение лаборатории Тимоти Кроу (T.Crow) в 1984 г. в Лондоне. Т.Кроу показал мне 2 семьи макак-мармозеток (они быстро размножаются), контрольную и основную, которой ввели спинно-мозговую жидкость от 4 больных ядерной шизофренией. Ученые-приматологи фиксировали изменения поведения у потомков обезьян с помощью специальной компьютеризированной методики. Т.Кроу пришел к выводу, что у «шизофренической» линии макак движения ограничены, их жизнь выглядит беднее, они более вялые, что позволяет предположить, что болезнь проявляется таким образом, наподобие простой формы шизофрении, и эти данные были опубликованы. В частной беседе проф. Т.Кроу обратил мое внимание на раннее поседение у потомков зараженных обезьянок, что могло бы быть объяснено, и на то, что у макак, предкам которых ввели ликвор больных шизофренией, стали. завиваться хвосты. Тогда мы посмотрели на это с очевидной самоиронией, однако в свете данных последних лет мы можем думать о метилировании ДНК.
Наследственный код у людей, а также у целого ряда других млекопитающих содержит фрагменты генетической последовательности специфичного вируса, который мог сыграть важную роль в изменчивости видов как с положительным, так и с отрицательным знаком. Об этом сообщили группа ученых из Японии и США, возглавляемых Кэидзо Томонагой (Keizo Tomonaga) из университета Осаки (Япония).
По данным последних исследований, целых 8% человеческого генома происходит не от наших предков-животных, а от вирусов. Однако до сих пор в наследственном коде людей обнаруживались вставки только от различных ретровирусов.
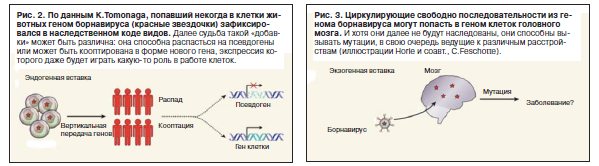
Теперь же Томонага и его коллеги открыли первый пример наследования (эндогенизации) у млекопитающих генетического кода от вируса, не принадлежащего данному семейству. И это оказался борнавирус (Bornavirus) – РНК-вирус, интересный тем, что его репликация происходит в ядре клетки (рис. 2).
Японские исследователи проанализировали 234 генома из тех видов, что ранее были секвенированы полностью. В результате нуклеотидные последовательности, гомологичные генам борнавируса (endogenous Borna-like nucleoprotein elements – EBLN), обнаружены в геномах человека, некоторых нечеловекообразных приматов, нескольких грызунов и слонов. Причем в ряде случаев в EBLN оказались нетронутыми открытые рамки считывания и происходила экспрессия генов с синтезом мРНК.
Интересно также, что анализ показал: добавление кода от борнавируса в код всех этих существ происходило независимо и в разные этапы эволюции. Так, у сусликов данная «обнова» в геноме появилась совсем недавно, а у приматов – 40 млн лет назад. Все это натолкнуло японских и американских генетиков на мысль о важной роли данного вируса в механизме генетической изменчивости видов.
Открытие международной группы ученых прокомментировал и развил Седрик Фешотт из Техасского университета (США). Как и в случае с ассимиляцией кода других вирусов, «новая» последовательность интегрируется в хромосомы половых клеток и далее передается от родителей к детям. И это важно, поскольку ранее борнавирус сам по себе биологи лишь связывали с неврологическим заболеванием Борны (Borna disease) и было известно, что поражает этот вирус только нейроны.
Однако получается, что подобные инфекции наших очень отдаленных предков оставили след в геноме нашего вида. Как это происходит, японцы показали на опыте, заразив борнавирусом культивированные человеческие клетки и тут же обнаружив свежие примеры формирования в геноме этих клеток новых последовательностей EBLN.
С.Фешотт рассуждает, что такие случаи заражения популяций с последующим наследованием части генома вируса могут служить источником мутаций в мозге, приводящих к самым различным (по знаку) последствиям для вида в целом (рис. 3). В частности, С.Фешотт предполагает, что имеется связь между древним «подарком» от борнавируса людям и таким заболеванием, как шизофрения. Очевидно, что на тернистом пути поисков этиологии психических заболеваний уже в ближайшем будущем следует ожидать новых открытий.
Эпигенетика: теоретические аспекты и практическое значение
В данной статье освещаются современные представления о эпигенетике как новой науке, механизмах эпигенетической регуляции и ее нарушениях, приводящих к развитию заболеваний.
This article highlights the modern views on epigenetics as a new science, the mechanisms of epigenetic regulation and their disorders, leading to the development of diseases.
Эпигенетика — сравнительно недавнее направление биологической науки и пока не так широко известно, как генетика. Под ней понимают раздел генетики, который изучает наследуемые изменения активности генов во время развития организма или деления клеток.
Эпигенетические изменения не сопровождаются перестановкой последовательности нуклеотидов в дезоксирибонуклеиновой кислоте (ДНК).
В организме существуют различные регуляторные элементы в самом геноме, которые контролируют работу генов, в том числе в зависимости от внутренних и внешних факторов. Долгое время эпигенетику не признавали, т. к. было мало информации о природе эпигенетических сигналов и механизмах их реализации.
Структура генома человека
В 2002 г. в результате многолетних усилий большого числа ученых разных стран закончена расшифровка строения наследственного аппарата человека, который заключен в главной молекуле ДНК. Это одно из выдающихся достижений биологии начала ХХI века.
ДНК, в которой находится вся наследственная информация о данном организме, называется геномом. Гены — это отдельные участки, занимающие очень небольшую часть генома, но при этом составляют его основу. Каждый ген отвечает за передачу в организме человека данных о строении рибонуклеиновой кислоты (РНК) и белка. Структуры, которые передают наследственную информацию, называют кодирующими последовательностями. В результате проекта «Геном» были получены данные, согласно которым геном человека оценивался в более чем 30 000 генов. В настоящее время, в связи с появлением новых результатов масс-спектрометрии, геном предположительно насчитывает около 19 000 генов [1].
Генетическая информация каждого человека содержится в ядре клетки и расположена в особых структурах, получивших название хромосомы. Каждая соматическая клетка содержит два полных набора (диплоидный) хромосом. В каждом единичном наборе (гаплоидном) присутствует 23 хромосомы — 22 обычные (аутосомы) и по одной половой хромосоме — Х или Y.
Молекулы ДНК, содержащиеся во всех хромосомах каждой клетки человека, представляют собой две полимерные цепи, закрученные в правильную двойную спираль.
Обе цепи удерживают друг друга четырьмя основаниями: аденин (А), цитозин (Ц), гуанин (Г) и тиамин (Т). Причем основание А на одной цепочке может соединиться только с основанием Т на другой цепочке и аналогично основание Г может соединяться с основанием Ц. Это называется принципом спаривания оснований. При других вариантах спаривание нарушает всю целостность ДНК.
ДНК существует в виде тесного комплекса со специализированными белками, и вместе они составляют хроматин.
Гистоны — это нуклеопротеины, основная составляющая хроматина. Им свойственно образование новых веществ путем присоединения двух структурных элементов в комплекс (димер), что является особенностью для последующей эпигенетической модификации и регуляции.
ДНК, хранящая генетическую информацию, при каждом клеточном делении самовоспроизводится (удваивается), т. е. снимает с самой себя точные копии (репликация). Во время клеточного деления связи между двумя цепями двойной спирали ДНК разрушаются и нити спирали разделяются. Затем на каждой из них строится дочерняя цепь ДНК. В результате молекула ДНК удваивается, образуются дочерние клетки.
ДНК служит матрицей, на которой происходит синтез разных РНК (транскрипция). Этот процесс (репликация и транскрипция) осуществляется в ядрах клеток, а начинается он с области гена, называемой промотором, на котором связываются белковые комплексы, копирующие ДНК для формирования матричной РНК (мРНК).
В свою очередь последняя служит не только носителем ДНК-информации, но и переносчиком этой информации для синтеза белковых молекул на рибосомах (процесс трансляции).
В настоящее время известно, что зоны гена человека, кодирующие белки (экзоны), занимают лишь 1,5% генома [2]. Большая часть генома не имеет отношения к генам и инертна в плане передачи информации. Выявленные зоны гена, не кодирующие белки, называются интронами.
Первая копия мРНК, полученная с ДНК, содержит в себе весь набор экзонов и интронов. После этого специализированные белковые комплексы удаляют все последовательности интронов и соединяют друг с другом экзоны. Этот процесс редактирования называется сплайсингом.
Эпигенетика объясняет один из механизмов, с помощью которого клетка способна контролировать синтез производимого ею белка, определяя в первую очередь, сколько копий мРНК можно получить с ДНК.
Итак, геном — это не застывшая часть ДНК, а динамическая структура, хранилище информации, которую нельзя свести к одним генам.
Развитие и функционирование отдельных клеток и организма в целом не запрограммированы автоматически в одном геноме, но зависят от множества различных внутренних и внешних факторов. По мере накопления знаний выясняется, что в самом геноме существуют множественные регуляторные элементы, которые контролируют работу генов. Сейчас это находит подтверждение во множестве экспериментальных исследований на животных [3].
При делении во время митоза дочерние клетки могут наследовать от родительских не только прямую генетическую информацию в виде новой копии всех генов, но и определенный уровень их активности. Такой тип наследования генетической информации получил название эпигенетического наследования.
Эпигенетические механизмы регуляции генов
Предметом эпигенетики является изучение наследования активности генов, не связанной с изменением первичной структуры входящей в их состав ДНК. Эпигенетические изменения направлены на адаптацию организма к изменяющимся условиям его существования.
Впервые термин «эпигенетика» предложил английский генетик Waddington в 1942 г. Разница между генетическими и эпигенетическими механизмами наследования заключается в стабильности и воспроизводимости эффектов [4].
Генетические признаки фиксируются неограниченное число, пока в гене не возникает мутация. Эпигенетические модификации обычно отображаются в клетках в пределах жизни одного поколения организма. Когда данные изменения передаются следующим поколениям, то они могут воспроизводиться в 3–4 генерациях, а затем, если стимулирующий фактор пропадает, эти преобразования исчезают.
Молекулярная основа эпигенетики характеризуется модификацией генетического аппарата, т. е. активации и репрессии генов, не затрагивающих первичную последовательность нуклеотидов ДНК.
Эпигенетическая регуляция генов осуществляется на уровне траскрипции (время и характер транскрипции гена), при отборе зрелых мРНК для транспорта их в цитоплазму, при селекции мРНК в цитоплазме для трансляции на рибосомах, дестабилизации определенных типов мРНК в цитоплазме, избирательной активации, инактивации молекул белков после их синтеза.
Совокупность эпигенетических маркеров представляет собой эпигеном. Эпигенетические преобразования могут влиять на фенотип.
Эпигенетика играет важную роль в функционировании здоровых клеток, обеспечивая активацию и репрессию генов, в контроле транспозонов, т. е. участков ДНК, способных перемещаться внутри генома, а также в обмене генетического материала в хромосомах [5].
Эпигенетические механизмы участвуют в геномном импритинге (отпечаток) — процессе, при котором экспрессия определенных генов осуществляется в зависимости от того, от какого родителя поступили аллели. Импритинг реализуется через процесс метилирования ДНК в промоторах, в результате чего транскрипция гена блокируется.
Эпигенетические механизмы обеспечивают запуск процессов в хроматине через модификации гистонов и метилирование ДНК. За последние два десятилетия существенно изменились представления о механизмах регуляции транскрипции эукариот. Классическая модель предполагала, что уровень экспрессии определяется транскрипционными факторами, связывающимися с регуляторными областями гена, которые инициируют синтез матричной РНК. Гистонам и негистоновым белкам отводилась роль пассивной упаковочной структуры для обеспечения компактной укладки ДНК в ядре.
В последующих исследованиях была показана роль гистонов в регуляции трансляции. Был обнаружен так называемый гистоновый код, т. е. модификация гистонов, неодинаковая в разных районах генома. Видоизмененные гистоновые коды могут приводить к активизации и репрессии генов [6].
Модификациям подвергаются различные части структуры генома. К концевым остаткам могут присоединяться метильные, ацетильные, фосфатные группы и более крупные белковые молекулы.
Все модификации являются обратимыми и для каждой существуют ферменты, которые ее устанавливают или удаляют.
Метилирование ДНК
У млекопитающих метилирование ДНК (эпигенетический механизм) было изучено раньше других. Показано, что он коррелирует с репрессией генов. Экспериментальные данные показывают, что метилирование ДНК является защитным механизмом, подавляющим значительную часть генома чужеродной природы (вирусы и др.).
Метилирование ДНК в клетке контролирует все генетические процессы: репликацию, репарацию, рекомбинацию, транскрипцию, инактивацию Х-хромосомы. Метильные группы нарушают ДНК-белковое взаимодействие, препятствуя связыванию транскрипционных факторов. Метилирование ДНК влияет на структуру хроматина, блокирует транскрипционные репрессоры [7].
Действительно, повышение уровня метилирования ДНК коррелирует с относительным увеличением содержания некодирующей и повторяющейся ДНК в геномах высших эукариот. Экспериментальные данные показывают, что это происходит потому, что метилирование ДНК служит главным образом как защитный механизм, чтобы подавлять значительную часть генома чужеродного происхождения (реплицированные перемещающиеся элементы, вирусные последовательности, другие повторяющиеся последовательности).
Профиль метилирования — активирование или угнетение — меняется в зависимости от средовых факторов. Влияние метилирования ДНК на структуру хроматина имеет большое значение для развития и функционирования здорового организма, чтобы подавлять значительную часть генома чужеродного происхождения, т. е. реплицированные перемещающиеся элементы, вирусные и другие повторяющиеся последовательности.
Метилирование ДНК происходит путем обратимой химической реакции азотистого основания — цитозина, в результате чего метильная группа СН3 присоединяется к углероду с образованием метилцитозина. Этот процесс катализируется ферментами ДНК-метилтрансферазами. Для метилирования цитозина необходим гуанин, в результате образуется два нуклеотида, разделенные фосфатом (СрG).
Скопление неактивных последовательностей СрG называется островками СрG. Последние представлены в геноме неравномерно [8]. Большинство из них выявляются в промоторах генов. Метилирование ДНК происходит в промоторах генов, в транскрибируемых участках, а также в межгенных пространствах.
Гиперметилированные островки вызывают инактивацию гена, что нарушает взаимодействие регуляторных белков с промоторами.
Метилирование ДНК оказывает огромное влияние на экспрессию генов и, в конечном счете, на функцию клеток, тканей и организма в целом. Установлена прямая зависимость между высоким уровнем метилирования ДНК и количеством репрессированных генов.
Удаление метильных групп из ДНК в результате отсутствия метилазной активности (пассивное деметилирование) реализуется после репликации ДНК. При активном деметилировании участвует ферментативная система, превращающая 5-метилцитозин в цитозин независимо от репликации. Профиль метилирования меняется в зависимости от средовых факторов, в которых находится клетка.
Утрата способности поддерживать метилирование ДНК может приводить к иммунодефициту, злокачественным опухолям и другим заболеваниям [9].
Долгое время механизм и ферменты, вовлеченные в процесс активного деметилирования ДНК, оставались неизвестными.
Ацетилирование гистонов
Существует большое число посттрансляционных модификаций гистонов, которые формируют хроматин. В 1960-е годы Винсент Олфри идентифицировал ацетилирование и фосфорилирование гистонов из многих эукариот [8].
Ферменты ацетилирования и деацетилирования (ацетилтрансферазы) гистонов играют роль в ходе транскрипции. Эти ферменты катализируют ацетилирование локальных гистонов. Деацетилазы гистонов репрессируют транскрипцию.
Эффект ацетилирования это ослабление связи между ДНК и гистонами из-за изменения заряда, в результате чего хроматин становится доступным для факторов транскрипции.
Ацетилирование представляет собой присоединение химической ацетил-группы (аминокислоты лизин) на свободный участок гистона. Как и метилирование ДНК, ацетилирование лизина представляет собой эпигенетический механизм для изменения экспрессии генов, не влияющих на исходную последовательность генов. Шаблон, по которому происходят модификации ядерных белков, стали называть гистоновым кодом.
Гистоновые модификации принципиально отличаются от метилирования ДНК. Метилирование ДНК представляет собой очень стабильное эпигенетическое вмешательство, которое чаще закрепляется в большинстве случаев.
Подавляющее большинство гистоновых модификаций более вариативно. Они влияют на регуляцию экспрессии генов, поддержание структуры хроматина, дифференциацию клеток, канцерогенез, развитие генетических заболеваний, старение, репарацию ДНК, репликацию, трансляцию. Если гистоновые модификации идут на пользу клетки, то они могут продолжаться довольно долго [8].
Одним из механизмов взаимодействия между цитоплазмой и ядром является фосфорилирование и/или дефосфорилирование транскрипционных факторов. Гистоны были одними из первых белков, фосфорилирование которых было обнаружено. Это осуществляется с помощью протеинкиназ.
Под контролем фосфорилируемых транскрипционных факторов находятся гены, в том числе гены, регулирующие пролиферацию клеток. При подобных модификациях в молекулах хромосомных белков происходят структурные изменения, которые приводят к функциональным изменениям хроматина.
Помимо описанных выше посттрансляционных модификаций гистонов имеются более крупные белки, такие как убиквитин, SUMO и др., которые могут присоединяться с помощью ковалентной связи к боковым аминогруппам белка-мишени, оказывая воздействие на их активность.
Эпигенетические изменения могут передаваться по наследству (трансгенеративная эпигенетическая наследственность). Однако в отличие от генетической информации, эпигенетические изменения могут воспроизводиться в 3–4 поколениях, а при отсутствии фактора, стимулирующего эти изменения, исчезают. Передача эпигенетической информации происходит в процессе мейоза (деления ядра клетки с уменьшением числа хромосом вдвое) или митоза (деления клеток).
Модификации гистонов играют фундаментальную роль в нормальных процессах и при заболеваниях.
Регуляторные РНК
Молекулы РНК выполняют в клетке множество функций. Одной из них является регуляция экспрессии генов. За эту функцию отвечают регуляторные РНК, к которым относятся антисмысловые РНК (aRNA), микроРНК (miRNA) и малые интерферирующие РНК (siRNA)
Механизм действия разных регуляторных РНК схож и заключается в подавлении экспрессии генов, реализующейся путем комплементарного присоединения регуляторной РНК к мРНК, с образованием двухцепочечной молекулы (дцРНК). Само по себе образование дцРНК приводит к нарушению связывания мРНК с рибосомой или другими регуляторными факторами, подавляя трансляцию. Также после образования дуплекса возможно проявление феномена РНК-интерференции — фермент Dicer, обнаружив в клетке двухцепочечную РНК, «разрезает» ее на фрагменты. Одна из цепей такого фрагмента (siRNA) связывается комплексом белков RISC (RNA-induced silencing complex) [10].
В результате деятельности RISC одноцепочечный фрагмент РНК соединяется с комплементарной последовательностью молекулы мРНК и вызывает разрезание мРНК белком семейства Argonaute. Данные события приводят к подавлению экспрессии соответствующего гена.
Физиологические функции регуляторных РНК разнообразны — они выступают основными небелковыми регуляторами онтогенеза, дополняют «классическую» схему регуляции генов.
Геномный импритинг
Человек обладает двумя копиями каждого гена, один из которых унаследован от матери, другой от отца. Обе копии каждого гена имеют возможность быть активной в любой клетке. Геномный импритинг это эпигенетически избирательная экспрессия только одного из аллельных генов, наследуемых от родителей. Геномный импритинг затрагивает и мужское и женское потомство. Так, импритингованный ген, активный на материнской хромосоме, будет активным на материнской хромосоме и «молчащим» на отцовской у всех детей мужского и женского пола. Гены, подверженные геномному импритингу, в основном кодируют факторы, регулирующие эмбриональный и неонатальный рост [11].
Импритинг представляет сложную систему, которая может ломаться. Импритинг наблюдается у многих больных с хромосомными делециями (утраты части хромосом). Известны заболевания, которые у человека возникают в связи с нарушением функционирования механизма импритинга.
Прионы
В последние десятилетие внимание привлечено к прионам, белкам, которые могут вызывать наследуемые фенотипические изменения, не изменяя нуклеотидной последовательности ДНК. У млекопитающих прионный белок расположен на поверхности клеток. При определенных условиях нормальная форма прионов может изменяться, что модулирует активность этого белка.
Викнер выразил уверенность в том, что этот класс белков является одним из многих, которые составляют новую группу эпигенетических механизмов, требующих дальнейшего изучения. Он может находиться в нормальном состоянии, а в измененном состоянии прионные белки могут распространяться, т. е. стать инфекционными [12].
Первоначально прионы были открыты как инфекционные агенты нового типа, но сейчас считают, что они представляют собой феномен общебиологический и являются носителями информации нового типа, хранимой в конформации белка. Феномен прионов лежит в основе эпигенетической наследственности и регуляции экспрессии генов на посттрансляционном уровне.
Эпигенетика в практической медицине
Эпигенетические модификации контролируют все стадии развития и функциональную активность клеток. Нарушение механизмов эпигенетической регуляции напрямую или косвенно связано с множеством заболеваний.
К заболеваниям с эпигенетической этиологией относят болезни импринтинга, которые в свою очередь делятся на генные и хромосомные, всего в настоящее время насчитывают 24 нозологии.
При болезнях генного импринтинга наблюдается моноаллельная экспрессия в локусах хромосом одного из родителей. Причиной являются точечные мутации в генах, дифференцированно экспрессирующихся в зависимости от материнского и отцовского происхождения и приводящих к специфическому метилированию цитозиновых оснований в молекуле ДНК. К ним относят: синдром Прадера–Вилли (делеция в отцовской хромосоме 15) — проявляется черепно-лицевым дисморфизмом, низким ростом, ожирением, мышечной гипотонией, гипогонадизмом, гипопигментацией и задержкой умственного развития; синдром Ангельмана (делеция критического района, находящегося в 15-й материнской хромосоме), основными признаками которого являются микробрахицефалия, увеличенная нижняя челюсть, выступающий язык, макростомия, редкие зубы, гипопигментация; синдром Беквитта–Видемана (нарушение метилирования в коротком плече 11-й хромосомы), проявляющийся классической триадой, включающей макросомию, омфалоцеле макроглоссию и др. [13].
К числу важнейших факторов, влияющих на эпигеном, относятся питание, физическая активность, токсины, вирусы, ионизирующая радиация и др. Особенно чувствительным периодом к изменению эпигенома является внутриутробный период (особенно охватывающий два месяца после зачатия) и первые три месяца после рождения. В период раннего эмбриогенеза геном удаляет большую часть эпигенетических модификаций, полученных от предыдущих поколений. Но процесс репрограммирования продолжается в течение всей жизни [14].
К заболеваниям, где нарушение генной регуляции является частью патогенеза, можно отнести некоторые виды опухолей, сахарный диабет, ожирение, бронхиальную астму, различные дегенеративные и другие болезни [15, 16].
Эпигоном при раке характеризуется глобальными изменениями в метилировании ДНК, модификации гистонов, а также изменением профиля экспрессии хроматин-модифицирующих ферментов.
Опухолевые процессы характеризуются инактивацией посредством гиперметилирования ключевых генов-супрессоров и посредством гипометилирования активацией целого ряда онкогенов, факторов роста (IGF2, TGF) и мобильных повторяющихся элементов, расположенных в районах гетерохроматина [17].
Так, в 19% случаев гипернефроидные опухоли почки ДНК островков СрG была гиперметилированной, а при раке груди и немелкоклеточной карциноме легких выявлена взаимосвязь между уровнями гистонового ацетилирования и экспрессией супрессора новообразований — чем ниже уровни ацетилирования, тем слабее экспрессия гена.
В настоящее время уже разработаны и внедрены в практику противоопухолевые лекарственные препараты, основанные на подавлении активности ДНК-метилтрансфераз, что приводит к снижению метилирования ДНК, активации генов-супрессоров опухолевого роста и замедлению пролиферации опухолевых клеток. Так, для лечения миелодиспластического синдрома в комплексной терапии применяют препараты децитабин (Decitabine) и азацитидин (Azacitidine) [18]. С 2015 г. для лечения множественной миеломы в сочетании с классической химиотерапией применяют панобиностат (Panibinostat), являющийся ингибитором гистоновой деацитилазы [19]. Данные препараты по данным клинических исследований оказывают выраженный положительный эффект на уровень выживаемости и качество жизни пациентов.
Изменения экспрессии тех или иных генов могут происходить и в результате действия на клетку факторов внешней среды. В развитии сахарного диабета 2-го типа и ожирения играет роль так называемая «гипотеза экономного фенотипа», согласно которой недостаток питательных веществ в процессе эмбрионального развития приводит к развитию патологического фенотипа [20]. На моделях животных был выявлен участок ДНК (локус Pdx1), в котором под влиянием недостаточности питания снижался уровень ацетилирования гистонов, при этом наблюдались замедление деления и нарушения дифференцировки B-клеток островков Лангерганса и развития состояния, схожего с сахарным диабетом 2-го типа [21].
Активно развиваются и диагностические возможности эпигенетики. Появляются новые технологии, способные анализировать эпигенетические изменения (уровень метилирования ДНК, экспрессию микроРНК, посттрансляционные модификации гистонов и др.), такие как иммунопреципитация хроматина (CHIP), проточная цитометрия и лазерное сканирование, что дает основания полагать, что в ближайшее время будут выявлены биомаркеры для изучения нейродегенеративных заболеваний, редких, многофакторных болезней и злокачественных новообразований и внедрены в качестве методов лабораторной диагностики [22].
Итак, в настоящее время эпигенетика бурно развивается. С ней связывают прогресс в биологии и медицине.
Литература
ФГБОУ ВО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва