Углерод — основа жизни на Земле
Мы посвятили две статьи воздуху, без которого жизнь на нашей 
Углерод — простое неорганическое вещество, элемент таблицы Менделеева. Обозначается буквой «С» (Carboneum). В виде алмазов, графита и древесного угля известен человечеству с древнейших времен. Название carbone (углерод) впервые было введено в химическую науку французскими учеными. А. Лавуазье доказал, что уголь — это элементарное химическое вещество, а не носитель некоего невесомого флюида флогистона, отвечающего за горючие свойства веществ. Он же установил, что алмаз — это кристаллическая форма углерода.
Три формы углерода
Углерод — удивительное вещество, физические свойства которого и даже внешний вид описать однозначно просто невозможно. Этот элемент — рекордсмен по количеству аллотропных модификаций. Три формы углерода:
• кристаллическая: алмазы, наноалмазы, фуллерены, фуллерит, графиты, карбины, лонсдейлиты, углеродные нанотрубки и нановолокна, графен, волокна и структуры;
• аморфная: угли (древесный, в том числе активированный уголь, антрацит и др.), коксы, сажа, углеродная нанопена, стеклоуглерод, техуглерод;
• кластерная: астралены, диуглерод, углеродные наноконусы.

Вещества, относящиеся к аморфным формам, не являются чистой формой углерода, но содержат углерод в очень значительных количествах. Для аморфного углерода характерна высокая теплоемкость, свойства полупроводников, невысокая плотность, относительно невысокая термостойкость — при температуре выше 1600 °С он превращается в графит. Как правило, их основой являются разные формы мелкокристаллического графита в виде неупорядочной структуры.
Углеродные кластеры — сложные соединения с очень интересными свойствами. Им, а также другим перспективным материалам на основе углерода, мы посвятим одну из ближайших статей.
Химические свойства
С химическими свойствами немного проще. В нормальных условиях углерод практически не вступает в реакции с другими элементами и веществами, инертен к кислотам, щелочам, галогенам. При высоких температурах проявляет сильные восстановительные свойства. Наиболее химически активны аморфные виды углерода, наиболее инертны — кристаллические. Графит по химической активности занимает серединное положение. При высоких температурах углерод окисляется кислородом (горит), образует несколько видов оксидов.
Графит и аморфный углерод при высоких температурах 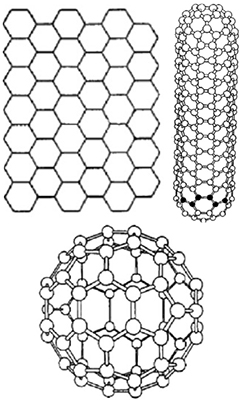
Главное свойство углерода — способность соединяться в длинные цепи, причем эти цепи могут содержать как атомы углерода, так и другие атомы. Цепи могут замыкаться, разветвляться, образовывать циклы, быть разной длины, соединяться («сшиваться») между собой в разнообразные структуры. Такие углеродно-водородные цепи — основа всей органической химии.
Следующая статья будет о содержании углерода в природе, его опасности и сферах применения.
Углерод элемент. Свойства углерода. Применение углерода
Его называют основой жизни. Он есть во всех органических соединениях. Только он способен формировать молекулы из миллионов атомов, такие, как ДНК.
Столько не наберется у всех остальных, вместе взятых элементов. Не удивительно, что один из двух разделов химии изучает исключительно соединения углерода и проходится в старших классах.
Предлагаем вспомнить школьную программу, а так же, дополнить ее новыми фактами.
Что такое углерод
В устаревшем варианте системы, углерод стоит в главной подгруппе 4-ой группы.
Обозначение элемента – буква С. Порядковый номер вещества – 6, относится к группе неметаллов.
Различия во внешности обусловлены несколькими типами строения кристаллической решетки. От нее зависят и полярные характеристики минерального углерода.
Графит, к примеру, мягок, не зря же добавляется в пишущие карандаши, а алмаз тверже всех остальных камней на Земле. Поэтому, логично рассмотреть свойства самого углерода, а не его модификаций.
Свойства углерода
Начнем со свойств, общих для всех неметаллов. Они электроотрицательны, то есть, оттягивают на себя общие электронные пары, образованные с другими элементами.
Получается, углерод может восстановить оксиды неметаллов до состояния металлов.
Однако, делает это 6-ой элемент лишь при нагреве. В обычных условиях вещество химически инертно.
На внешних электронных уровнях неметаллов больше электронов, чем у металлов.
Именно поэтому, атомы 6-го элемента стремятся достроить толику собственных орбиталей, чем отдавать свои частицы кому-то.
Металлам же, с минимумом электронов на внешних оболочках проще отдать отдаленные частицы, чем перетягивать на себя чужие.
Главная форма 6-го вещества – атом. По идее, речь должна идти о молекуле углерода. Из молекул составлено большинство неметаллов.
Однако, углерод с бором и кремнием – исключения, имеют атомную структуру. Именно за счет нее соединения элементов отличаются высокими температурами плавления.
Раз разговор зашел о формах 6-го вещества, укажем, что кристаллическая – лишь одна из.
Атомы углерода не всегда выстраиваются в кристаллическую решетку. Встречается аморфная разновидность.
Если же вещество соединено с другими, могут получиться и газы. Кристаллический углерод переходит в них при температуре в 3700 градусов.
В обычных условиях элемент газообразен, если это, к примеру, оксид углерода.
В народе его именуют угарным газом. Однако, реакция его образования активнее и быстрее, если, все же, поддать жару.
Газообразных соединений углерода с кислородом несколько. Есть еще, к примеру, монооксид.
Этот газ бесцветный и ядовитый, причем, при обычных условиях. Такая окись углерода имеет тройную связь в молекуле.
Реакция возможна и с водородом. Углерод вступит во взаимодействие, если «сыграет» один из факторов, или все вместе: температура, аллотропное состояние, дисперсность.
Под последней, подразумевается отношение площади поверхности частиц вещества к занимаемому ими объему.
Аллотропия – возможность нескольких форм одного и того же вещества, то есть, имеется в виду кристаллический, аморфный, или газообразный углерод.
Однако, как не совпадай факторы, с кислотами и щелочами элемент не реагирует вовсе. Игнорирует углерод и почти все галогены.
Чаще всего, 6-ое вещество связывается само с собой, образовывая те самые масштабные молекулы из сотен и миллионов атомов.
Сформированные молекулы, углерода реагируют с еще меньшим числом элементов и соединений.
Применение углерода
Применение элемента и его производных столь же обширно, как их число. Содержание углерода в жизни человека больше, чем может казаться.
Активированный уголь из аптеки – 6-е вещество. Бриллиант в кольце из ювелирного магазина – он же.
Графит в карандашах – тоже углерод, нужный, так же, в ядерных реакторах и контактах электрических машин.
Метановое топливо тоже в списке. Диоксид углерода нужен для производства соды и может быть сухим льдом, то есть, хладагентом.
Углекислый газ служит консервантом, заполняя овощные хранилища, а еще, нужен для получения карбонатов.
Формула углерода соответствует еще и коксу. Он пригождается металлургам.
Кокс служит восстановителем во время переплавки руды, извлечения из нее металлов.
Не задумывались, почему автомобильные шины черного цвета? Это сажа. Она придает резине прочность.
Сажа, так же, входит в крема для обуви, краски для печати, туши для ресниц. Народное название употребляется не всегда. Промышленники зовут сажу техническим углеродом.
Это твердый и прочный материал. Звучит увесисто. Но, на самом деле, аэрогель легче воздуха.
В железо углерод добавляют, чтобы получить так называемую углеродистую сталь. Она тверже обычной.
Однако, массовая доля 6-го элемента в сплаве не должна превышать пары, тройки процентов. Иначе, свойства стали идут на спад.
Список можно продолжать бесконечно. Но, где бесконечно брать углерод? Добывают его или синтезируют? На эти вопросы ответим в отдельной главе.
Добыча углерода
Газ углерод и его твердые модификации проще и дешевле добывать попутно с каменным углем.
Из земных недр этого ископаемого извлекают примерно 2 миллиарда тонн ежегодно. Хватает, чтобы обеспечить мир техническим углеродом.
Месторождения графита, напротив, горизонтальны, располагаются у поверхности.
Поэтому, добыча минерала довольно проста и не затратна. В год из недр извлекают около 500 000 тонн графита.
Чтобы получить активированный уголь, приходится нагреть каменный уголь и обработать струей водяного пара.
Ученые даже разобрались, как воссоздать белки человеческого тела. Их основа – тоже углерод. Азот и водород – аминогруппа, к нему примыкающая.
Нужен, так же, кислород. То есть, белки построены на аминокислоте. Она не у всех на слуху, но для жизни куда важнее остальных.
Популярные серная, азотная, соляная кислоты, к примеру, организму нужны куда меньше.
Так что, углерод – то, за что стоит платить. Узнаем, на сколько велик разброс цен на разные товары из 6-го элемента.
Цена углерода
Для жизни, как несложно понять, углерод бесценен. Что же касается остальных сфер бытия, ценник зависит от наименования продукции и ее качества.
Образцы аэрогеля, пока, стоят десятки долларов за несколько квадратных сантиметров.
Но, в будущем, производители обещают поставлять материал рулонами и просить недорого.
Технический углерод, то есть, сажа, реализуется по 5-7 рублей за кило. За тонну, соответственно, отдают около 5000-7000 рублей.
Однако, углеродный налог, вводимый в большинстве развитых стран, может обеспечить рост цен.
Углеродную промышленность считают причиной парникового эффекта. Предприятия обязывают платить за выбросы, в частности, CO2.
Это главный парниковый газ и, одновременно, индикатор загрязнения атмосферы. Эта информация – ложка дегтя в бочке меда.
Она позволяет понять, что у углерода, как и всего в мире, есть обратная сторона, а не только плюсы.
Углерод
Углерод встречается как:
История
Углеро́д в виде древесного угля применялся в глубокой древности для выплавки металлов. Издавна известны алмаз и графит. Элементарная природа углерода установлена А. Лавуазье в конце 1780-х годов.
Происхождение названия
Международное название происходит от латинского carbo — уголь, связанного с древним корнем kar — огонь. Этот же корень в латинском cremare — гореть, а возможно, и в русском « гарь », «жар», «угореть» (в древнерусском «угорати» — обжигать, опалять). Отсюда — и «уголь».
Содержание
Физические свойства
Углерод существует во множестве аллотропных модификаций с очень разнообразными физическими и химическими свойствами. Разнообразие модификаций обусловлено способностью углерода образовывать химические связи разного типа. Основные физические свойства собственно углерода смотри в таблице.
Изотопы углерода
Аллотропные модификации углерода
Упрощенная фазовая диаграмма углерода, заштрихованы области где аллотропные модификации могут быть метастабильны. (diamond — алмаз, graphite — графит, liquid — жидкость, vapor — газ)

Электронное строение атома углерода
Графит и алмаз
Элементарная ячейка (углерода) алмаза
При давлении свыше 60 Г Па предполагают образование весьма плотной модификации С III (плотность на 15—20 % выше плотности алмаза), имеющей металлическую проводимость. При высоких давлениях и относительно низких температурах (ок. 1 200 K) из высокоориентированного графита образуется гексагональная модификация углерода с кристаллической решеткой типа вюрцита — лонсдейлит (а = 0,252 нм, с = 0,412 нм, пространственная группа Р63/ттс), плотность 3,51 г/см³, т. е. такая же, как у алмаза. Лонсдейлит найден также в метеоритах.
Ультрадисперсные алмазы (наноалмазы)
Карбин
Фуллерены и углеродные нанотрубки
Углерод известен также в виде кластерных частиц С60, С70 и подобных (фуллерены), а также графенов и нанотрубок.
Аморфный углерод
Нахождение в природе
Содержание углерода в земной коре 0,1 % по массе. Свободный углерод находится в природе в виде алмаза и графита. Основная масса углерода в виде природных карбонатов (известняки и доломиты), горючих ископаемых — антрацит (94—97 % С), бурые угли (64—80 % С), каменные угли (76—95 % С), горючие сланцы (56—78 % С), нефть (82—87 % С), горючих природных газов (до 99 % метана), торф (53—56 % С), а также битумы и др. В атмосфере и гидросфере находится в виде диоксида углерода СО2, в воздухе 0,046 % СО2 по массе, в водах рек, морей и океанов в
60 раз больше. Углерод входит в состав растений и животных (
В парообразном состоянии и в виде соединений с азотом и водородом углерод обнаружен в атмосфере Солнца, планет, он найден в каменных и железных метеоритах.
Большинство соединений углерода, и прежде всего углеводороды, обладают ярко выраженным характером ковалентных соединений. Прочность простых, двойных и тройных связей атомов С между собой, способность образовывать устойчивые цепи и циклы из атомов С обусловливают существования огромного числа углеродсодержащих соединений, изучаемых органической химией.
Химические свойства
При обычных температурах углерод химически инертен, при достаточно высоких соединяется со многими элементами, проявляет сильные восстановительные свойства. Химическая активность разных форм углерода убывает в ряду: аморфный углерод, графит, алмаз, на воздухе они воспламеняются при температурах соответственно выше 300—500 °C, 600—700 °C и 850—1000 °C.
Степени окисления +4, −4, редко +2 (СО, карбиды металлов), +3 (C2N2, галогенцианы); сродство к электрону 1,27 эВ; энергия ионизации при последовательном переходе от С 0 к С 4+ соответственно 11,2604, 24,383, 47,871 и 64,19 эВ.
Неорганические соединения
Углерод реагирует со многими элементами с образованием карбидов.
Органические соединения
Благодаря способности углерода образовывать полимерные цепочки, существует огромный класс соединений на основе углерода, которых значительно больше, чем неорганических, и изучением которых занимается органическая химия. Среди них наиболее обширные группы: углеводороды, белки, жиры и др.
Применение
Феррит ( твердый раствор внедрения C в α-железе с объемно-центрированной кубической решеткой)
Аустенит ( твердый раствор внедрения C в γ-железе с гранецентрированной кубической решеткой)
Цементит (карбид железа; Fe3C метастабильная высокоуглеродистая фаза)
Графит стабильная высокоуглеродистая фаза
Ледебурит ( эвтектическая смесь кристаллов цементита и аустенита, превращающегося при охлаждении в перлит)
Мартенсит (сильно пересыщенный твердый раствор углерода в α-железе с объемно-центрированной терагональной решеткой)
Перлит ( эвтектоидная смесь, состоящая из тонких чередующихся пластинок феррита и цементита)
Сорбит (дисперсный перлит)
Троостит (высокодисперсный перлит)
Бейнит (устар: игольчатый троостит) — ультрадисперсная смесь кристаллов низкоуглеродистого мартенсита и карбидов железа
Конструкционная сталь (до 0,8 % C)
Инструментальная сталь (до
2 % C)
Нержавеющая сталь ( легированная хромом)
Жаростойкая сталь
Жаропрочная сталь
Высокопрочная сталь
Белый чугун (хрупкий, содержит ледебурит и не содержит графит)
Серый чугун (графит в форме пластин)
Ковкий чугун (графит в хлопьях)
Высокопрочный чугун (графит в форме сфероидов)
Половинчатый чугун (содержит и графит, и ледебурит)
Углерод играет огромную роль в жизни человека. Его применения столь же разнообразны, как сам этот многоликий элемент.
Углерод является основой всех органических веществ. Любой живой организм состоит в значительной степени из углерода. Углерод — основа жизни. Источником углерода для живых организмов обычно является СО2 из атмосферы или воды. В результате фотосинтеза он попадает в биологические пищевые цепи, в которых живые существа пожирают друг друга или останки друг друга и тем самым добывают углерод для строительства собственного тела. Биологический цикл углерода заканчивается либо окислением и возврашением в атмосферу, либо захоронением в виде угля или нефти.
Углерод в виде ископаемого топлива: угля и углеводородов (нефть, природный газ) — один из важнейших источников энергии для человечества.
Углерод в сталелитейной промышленности один из важнеших компонентов сплавов железо-углерод (производсво чугуна и стали).
Графит используется в карандашной промышленности. Также его используют в качестве смазки при особо высоких или низких температурах.
Токсическое действие
Токсическое действие 14 С, вошедшего в состав молекул белков (особенно в ДНК и РНК), определяется радиационным воздействием бета частиц и ядер отдачи азота ( 14 С (β) → 14 N) и трансмутационным эффектом — изменением химического состава молекулы в результате превращения атома С в атом N. Допустимая концентрация 14 С в воздухе рабочей зоны ДКА 1,3 Бк/л, в атмосферном воздухе ДКБ 4,4 Бк/л, в воде 3,0•10 4 Бк/л, предельно допустимое поступление через органы дыхания 3,2•10 8 Бк/год.
УГЛЕРОД
В этой книге слово «углерод» встречается довольно часто: в рассказах о зелёном листе и о железе, о пластмассах и кристаллах и ещё во многих других. Углерод — «рождающий уголь» — один из удивительнейших химических элементов. Его история — это история возникновения и развития жизни на Земле, потому что он входит в состав всего живого Земли.
А как выглядит углерод?
Сделаем несколько опытов. Возьмём сахар и нагреем его без доступа воздуха. Он сначала расплавится, станет коричневым, а потом почернеет и превратится в уголь, выделив воду. Если теперь нагреть этот уголь в присутствии КИСЛОРОДА, он сгорит без остатка и превратится в УГЛЕКИСЛЫЙ ГАЗ. Стало быть, сахар состоял из угля и воды (сахар, кстати, и называют углеводом), а «сахарный» уголь — это, видимо, и есть чистый углерод, потому что углекислый газ — это соединение углерода с кислородом. Значит, углерод — чёрный, мягкий порошок.
Возьмём серый мягкий камень графит, хорошо тебе знакомый благодаря карандашам. Если его нагреть в кислороде, он тоже сгорит без остатка, хотя и немного медленней, чем уголь, а в приборе, где он горел, останется углекислый газ. Значит, графит тоже чистый углерод? Конечно, но и это ещё не всё.
Если в том же приборе в кислороде накалить алмаз, прозрачный сверкающий драгоценный камень, самый твердый из всех минералов, он тоже сгорит, превратившись в углекислый газ. Если же нагревать алмаз без доступа кислорода, он превратится в графит, а при очень высоких давлениях и температурах можно из графита получить алмаз.
Итак, уголь, графит и алмаз — это различные формы существования одного и того же элемента — углерода.
Ещё более удивительна способность углерода «принимать участие» в огромном количестве разнообразных соединений (поэтому-то слово «углерод» так часто встречается в этой книге).
104 элемента периодической системы образуют более сорока тысяч изученных соединений. А соединений, основу которых составляет углерод, уже известно свыше миллиона!
Причина такого разнообразия заключается в том, что атомы углерода могут соединяться между собой и с другими атомами прочной связью, образуя сложные МОЛЕКУЛЫ в виде цепей, колец и других фигур. Ни один элемент в таблице МЕНДЕЛЕЕВА, кроме углерода, не способен на это.












