Фетальная печень что такое
Течение хронического гепатита (ХГ) и цирроза печени (ЦП) сопровождается развитием гипоксии различной степени выраженности [3]. Известно, что формирование хронической гипоксии характеризуется стойкими нарушениями окислительных процессов в тканях с последующим прогрессированием дистрофических процессов в различных тканях и органах и декомпенсацией функции жизненно важных органов, в том числе печени [1].
Изучение молекулярных механизмов гипоксии показало, что развитие в организме патологических процессов, сопровождающихся перестройкой интенсивности кроветворения и оксигенации тканей, характеризуется ростом гетерогенности гемоглобина [1, 6, 7]. Среди всех типов гемоглобина особый интерес представляет фетальный гемоглобин (HbF), который при одном и том же парциальном давлении более активно поглощает кислород и с большей готовностью отдает углекислоту, чем гемоглобин взрослого [1, 2, 6, 7]. В процессе эмбриогенеза содержание HbF в крови постепенно уменьшается параллельно увеличению количества взрослого гемоглобина (HbA1) и к моменту рождения составляет, по данным разных авторов, 50-80 % [1, 2, 6, 9]. После рождения ребенка HbF продолжает убывать и к 2-3 году жизни составляет всего 1-1,5 %, как и у взрослого. Количество HbF, превышающее 1,5 %, считается патологическим для взрослого человека и для детей старше 3 лет [6, 7, 8, 9].
Учитывая особенности данной фракции гемоглобина и его высокое сродство к кислороду, в последние годы активизировались работы, посвященные изучению роли HbF при хронических заболеваниях, протекающих с гипоксией [1, 2, 4, 5, 8]. В значительной степени это продиктовано усовершенствованием методов исследования HbF, преимущество среди которых отдается иммунохимическим тестам в связи с их высокой специфичностью и чувствитель- ностью [6, 7]. При этом клинико-патогенетическое значение HbF у больных ХДЗП мало изучено, в связи с чем проведение подобного исследования является актуальным.
Цель: установить диагностическую значимость определения уровня HbF у больных ХГ и ЦП с учетом степени выраженности патологического процесса в печени и степени ее функциональной недостаточности.
Материалы и методы исследования
HbF определялся по методике, разработанной на кафедре биохимии ГБОУ ВПО АГМА. Для количественного анализа HbF применялся способ ракетного электрофореза в агаровом геле с додецилсульфатом натрия (патент №2310204 от 10.11.2007) [7]. Авторами использовались чистые препараты HbF и моноспецифические антисыворотки к HbF, полученные самостоятельно и прошедшие строгий контроль чистоты и специфичности [1, 6, 7]. Описываемый способ был успешно апробирован в научной лаборатории кафедры биохимии с курсом клинической лабораторной диагностики Астраханской государственной медицинской академии в течение 2005-2009 гг.
Забор крови для исследования на HbF производили на 2-е сутки после поступления в стационар.
Проводя настоящее исследование, нельзя было не учесть осложнения ЦП. В связи с этим больные были разделены по группам с наличием осложнений (варикозно расширенные вены пищевода (ВРВП), асцит, гиперспленизм) и без них. Результаты исследования представлены в табл. 2.
Таблица 2. Показатели HbF в зависимости от наличия осложнений цирроза печени
Группа больных циррозом печени (n = 146)
Ультразвуковые исследования печени в педиатрии
Введение
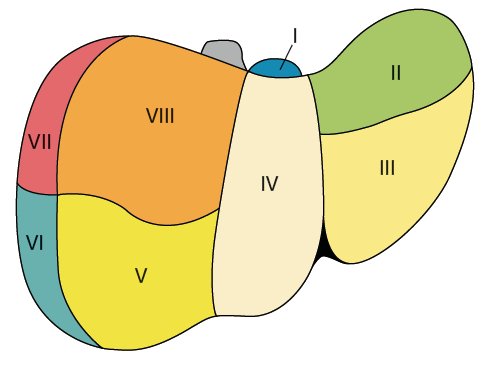
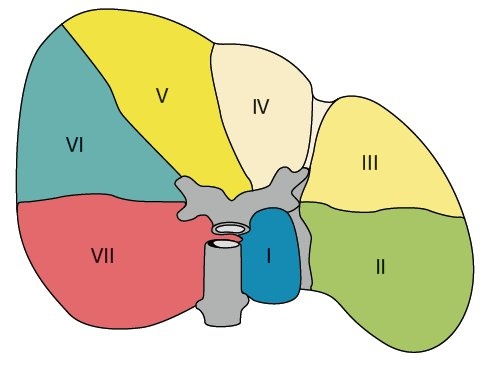
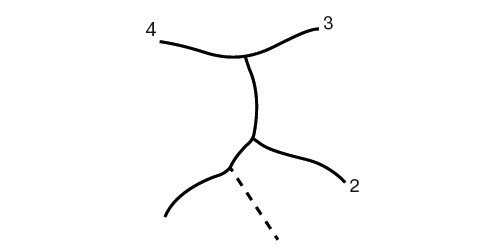
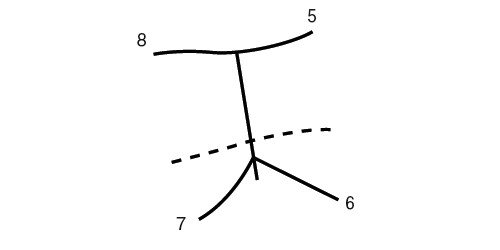
Клиническая анатомия печени
Известно высказывание, сравнивающее ультразвуковые исследования (УЗИ) с волшебным фонариком, позволяющим заглянуть в темную комнату и рассмотреть ее содержимое. УЗИ представляют нам «живую анатомию» органа, позволяя поставить топический диагноз при очаговом поражении печени или объективно охарактеризовать динамику диффузного процесса.
а) Вид с диафрагмальной поверхности.
б) Вид с абдоминальной поверхности.
а) Левая доля печени.
б) Правая доля печени.
Полноценное УЗИ подразумевает неукоснительную визуализацию ветвей воротной вены, их сегментарных ветвей, печеночных вен. Это позволяет диагностировать не только очаговые поражения печени, но и обнаружить тромбозы, сдавление сосудов объемным образованием или прорастанием опухоли в сосуд. Допплеровское исследование завершает диагностическую процедуру, определяя наличие и направление кровотока в сосудах. Рядом с сосудистым пучком (печеночная артерия и воротные вены) располагаются желчные ходы. Они становятся видны при блокаде оттока желчи [2].
Клинические проблемы
Желтухи новорожденных могут быть результатом паренхиматозных процессов (гепатоцеллюлярные) обструктивного характера, гемолитического и септического происхождения.
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Трансплантация фетальных стволовых клеток
Общая информация
Краткое описание
Трансплантация фетальных стволовых клеток – это уникальная операция, введения в организм больного фетальных клеток, которые представляют собой, клеточную фракцию криоконсервированных фетальных тканей плода, полученных из абортированного материала (фетуса) 16-21 недельной беременности.
Процедура трансплантации фетальных стволовых клеток проводится 6-10 кратно с интервалом в 3-6 и более месяцев, в зависимости от нозологии, степени тяжести заболевание и функциональных нарушений органов или тканей после предоставления информированного согласия пациентом [1,20,33].
Название протокола: Трансплантация фетальных стволовых клеток
Код протокола:
Код(ы) МКБ-10:
Е 03 – Другие формы гипотиреоза
Е 10 – Сахарный диабет 1 тип
Е 11 – Сахарный диабет 2 тип
G 11.2 – Поздняя мозжечковая атаксия
G 11.8 – Другая наследственная атаксия
G 12.2 – Болезнь двигательного неврона
G 35 – Рассеянный склероз
G 37.8 – Рассеянный энцефаломиелит
G 95.0 – Сирингомиелия и сирингобульбия
I 69.1 – Последствия внутричерепного кровоизлияния
I 69.3 – Последствия инфаркта мозга
K74. – Фиброз и цирроз печени
K74.3 – Первичный билиарный цирроз печени
K74.6 – Другой и неуточненный цирроз печени
М05 – Серопозитивный ревматоидный артрит
М06 – Другие ревматоидные артриты
М05.3 – Ревматоидный артрит с вовлечением других органов и систем
М06.0 – Серонегативный ревматоидный артрит
М87 – Остеонекроз
N03 – Хронический нефритический синдром
N04 – Нефротический синдром
N 11.9 – Хронический тубулоинтерстициальный нефрит неуточненный
N 18 – Хроническая почечная недостаточность
N 18.9 – Хроническая почечная недостаточность неуточненная
T 91.3 – Последствия травмы спинного мозга.
Сокращения, используемые в протоколе:
CKD-EPI – Chronic Kidney Desease Epidemiology Collaboration
СТР – Сhild-Turcotte Pugh
CD – cluster of differentiation
СА – Cancer Antigen
CYFRA – фрагмент цитокератина 19
EDSS – Expanded Disability Status Scale
IgA – иммуноглобулин А
IgG – иммуноглобулин G
IgM – иммуноглобулин M
MDRD – Modification of Diet in Renal Disease Study
MELD – Model End-Stage Liver Disease
RW – реакция Вассермана
SpO2 – сатурация гемоглобина кислородом
Scripps шкала – шкала неврологического статуса
АД – артериальное давление
АлТ – аланинаминотрансфераза
АРА – Американская ревматологическая ассоциация
АсТ – аспартатаминотрансфераза
АФП – альфа-фетопротеин
АЧТВ – активированное частичное тромбопластиновое время
БДН – болезнь двигательного неврона
БПГН – быстропрогрессирующий гломерулонефрит
ХГН – хронический гломерулонефрит
ХБП – хронический болезнь почек
ВАШ – визуальная аналоговая шкала
ВИЧ – вирус иммунодефицита человека
ВМ – врожденные миопатии
ГКС – глюкокортикостероиды
ДНА – другая наследственная атаксия
ИМТ – индекс массы тела
ИФА – иммуноферментный анализ
КТ – компьютерная томография
МД – мышечная дистрофия
МНО – международное нормализованное отношение
МРТ – магнитно-резонансная томография
МФФ – микофенолат мофетил
ОАК – общий анализ крови
ОГБК – остеонекроз головки бедренной кости
ПВ – протромбиновое время
ПВК – последствия внутричерепного кровоизлияния
ПИМ – последствия инфаркта мозга
ПМА – поздняя мозжечковая атаксия
ПСА – простатический специфический антиген
ПТСМ – последствия травмы спинного мозга
ПЦР – полимеразная цепная реакция
РА – ревматоидный артрит
РС – рассеянный склероз
РФ – ревматоидный фактор
РЭА – раковый эмбриональный антиген
СД1 – сахарный диабет 1 тип
СД2 – сахарный диабет 2 тип
СКФ – скорость клубочковой фильтрации
СОЭ – скорость оседания эритороцитов
СПИД – синдром приобретенного иммунодефицита
СРБ – С-реактивный белок
ТФСГ – трансплантация фетальных стволовых гепатоцитов
ТФСК – трансплантация фетальных стволовых клеток
ТФСКПЖ – трансплантация фетальных стволовых клеток поджелудочной железы
ТФСН – трансплантация фетальных стволовых нейроцитов
ТФСНф – трансплантация фетальных стволовых нефроцитов
ТФСТ – трансплантация фетальных стволовых тиреоцитов
ТФСХ – трансплантация фетальных стволовых хондроцитов
УЗДГ – ультразвуковая допплерография
УЗИ – ультразвуковое исследование
ФГЧ – фетальные гепатоциты человека
ФКПЖ – фетальные клетки поджелудочной железы
ФКЧ – фетальные клетки человека
ФНфЧ – фетальные нефроциты человека
ФНЧ – фетальные нейроциты человека
ФП – фиброз печени
ФТЧ – фетальные тиреоциты человека
ХПН – хроническая почечная недостаточность
ХТИН – хронический тубулоинтерстициальный нефрит
ЦВБ – цереброваскулярные болезни
ЦНС – центральная нервная система
ЦП – цирроз печени
ЦсА – циклоспорин А
ЦФ – циклофосфан
ЧБС – частота болевых суставов
ЧПС – частота пораженных суставов
ЧСС – частота сердечных сокращений
ЭГДС – эзофагогастродуоденоскопия
ЭКГ – электрокардиограмма
ЭХО ЭКГ – эхоэлектрокардиограмма
Дата разработки протокола: 2015 год.
Категория пациентов: пациенты, страдающие аутоиммунными и/или дегенеративными заболеваниями с нарушением гемопоэза, нуждающиеся в трансплантации фетальных клеток для регенерации органов и тканей.
Пользователи протокола: гастроэнтерологи, ревматологи, невропатологи, нефрологи, эндокринологи, терапевты, хирурги, анестезиологи-реаниматологии и врачи общей практики.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Диагностика
Цель проведения процедуры/вмешательства:
Управление прогрессирующими хроническими заболеваниями путем регенерации и восстановления утраченных функций органов и тканей для увеличения продолжительности жизни и улучшения качества жизни [23,33].
Показания и противопоказания для проведения трансплантации фетальных стволовых нефроцитов:
Показания к трансплантации фетальных стволовых гепатоцитов [22,24,42]:
· Цирроз печени, класс «А» по Сhild-Turcotte Pugh
Критерии: асцит отсутствует, энцефалопатия отсутствует, билирубин менее 35 мкмоль/л; альбумин >3,5 г/дл, ПВ
Лечение
Методика проведения процедуры:
Процедура ТФСК проводится в условиях операционного блока (ТФСН и ТФСХ) или отделения реанимации и интенсивной терапии медицинских организаций, оказывающих высокоспециализированную и специализированную помощь населению.
К работе допускаются лица не моложе 18 лет, имеющих высшее медицинское образование с квалификационной характеристикой врача хирурга, ортопеда-травматолога или трансплантолога.
В помещении для проведения ТФСК обеспечивается соблюдение санитарно-противоэпидемического режима, соответствующего операционному блоку, с соблюдением правил асептики, антисептики, стерилизации.
Эндолюмбальная трансплантация фетальных стволовых нейроцитов
Процедура состоит из 4 этапов:
· процедуры подготовки клеточного материала;
· определение дозы и кратности введения клеточного материала;
· эндолюмбальное введение фетальных нейроцитов;
· оценка качества проведенной ТФСН.
Процедуры подготовки клеточного материала:
Разморозку криоконсервированных фетальных нейроцитов производят на водяной бане, снабженной нагревательным элементом, регулятором температуры. Ампулы объемом 10,0 мл размораживают при температуре 37 0 С в течение 5,0 мин. При размораживании ампул соблюдать меры предосторожности.
После размораживания определяют концентрацию сохранившихся клеток, для чего в суспензию добавляли равный объем 0,2%-ного трипанового синего, окрашивающего мертвые клетки в синий цвет. Окрашенную суспензию заправляли в счетную камеру Горяева. Общий процент жизнеспособных клеток после разморозки должен составлять не менее 70% от общего количества клеток.
Определение дозы и кратности введения клеточного материала:
ТФСН назначают однократно в виде суспензии по 3,0мл барботажное введение в спинномозговое пространство.
Оценка качества проведенной трансплантации фетальных медиаторов:
Возможные побочные явления: пациент может почувствовать небольшую боль в местах пункций во время введения пункционной иглы. После проведения ТФСН возможны головная боль, тошнота, рвота, повышение температуры тела.
Возможные осложнения в области пункции, такие как воспалительный процесс тканей и спинного мозга. Накладывается давящая повязка и наблюдение в динамике в течение суток. В случае отсутствия осложнений пациент переводится в отделение.
После проведения трансплантации осуществляется динамическое наблюдение, контроль АД, ЧСС, температуры тела и ОАК в первые сутки после ТФСН [27,31,40].
Трансплантация фетальных стволовых хондроцитов в тазобедренный сустав (Z-дуга рентгенологическая):
Процедура состоит из 4 этапов:
· процедуры подготовки клеточного материала;
· определение дозы и кратности введения клеточного материала;
· внутрисуставное введение фетальных хондроцитов в тазобедренный сустав по рентгенологическим контролем;
· оценка качества проведенной ТФСХ.
Процедуры подготовки клеточного материала:
Разморозку криоконсервированных фетальных хондроцитов производят на водяной бане, снабженной нагревательным элементом, регулятором температуры. Ампулы объемом 10,0 мл размораживают при температуре 37 0 С в течение 5,0 мин. При размораживании ампул соблюдать меры предосторожности.
После размораживания определяют концентрацию сохранившихся клеток, для чего в суспензию добавляли равный объем 0,2%-ного трипанового синего, окрашивающего мертвые клетки в синий цвет. Окрашенную суспензию заправляли в счетную камеру Горяева. Общий процент жизнеспособных клеток после разморозки должен составлять не менее 70% от общего количества клеток.
Определение дозы и кратности введения клеточного материала:
ТФСХ назначают однократно внутрь в головку бедренной кости, в крышку вертлужной впадины, субхондрально и в полость тазобедренного сустава в виде суспензии 5,0мл.
Внутрисуставное введение фетальных хондроцитов в тазобедренный сустав:
Положение пациента на операционном столе в горизонтальном положении на спине. Обработка операционного поля, трижды спиртовым раствором 96°-20,0 мл. Внутривенная анестезия до введения фетальных стволовых хондроцитов одного тазобедренного сустава проводится или перидуральная анестезия до выполнения ТФСХ в оба тазобедренных суставов. Под рентгенологическим контролем (Z-дуга) (рис.1), производится пункция тазобедренного сустава спицей Киршнера. По методу Сельдингера, через пункционную иглу в косо- параллельных направлениях в головку бедренной кости, по ходу спицы Киршнера в крышу вертлужной впадины субхондрально (в зоны остеопороза) и отдельно в полость тазобедренного сустава вводится взвесь фетальных хондроцитов в объеме 5мл соответствующей группы крови и резус фактора (рис.2). Проводится фотодокументация трансплантации фетальных стволовых хондроцитов. Накладывается асептическая и давящая повязка.
Оценка качества проведенной ТФСХ в тазобедренный сустав:
Возможные побочные явления: пациент может почувствовать небольшую боль в местах пункций во время введения пункционной иглы. После проведения ТФСХ возможны головная боль, тошнота, рвота, повышение температуры тела.
Возможные осложнения в области пункции, такие как воспалительный процесс тканей и спинного мозга. Накладывается давящая повязка и наблюдение в динамике в течение суток. В случае отсутствия осложнений пациент переводится в отделение.
После проведения трансплантации осуществляется динамическое наблюдение, контроль АД, ЧСС, температуры тела и ОАК в первые сутки после ТФСХ [3,13].
Трансплантация фетальных стволовых хондроцитов в коленный сустав (артроскопия):
Процедура состоит из 4 этапов:
· процедуры подготовки клеточного материала;
· определение дозы и кратности введения клеточного материала;
· внутрисуставное артроскопическое введение фетальных хондроцитов в коленный сустав;
· оценка качества проведенной ТФСХ.
Процедуры подготовки клеточного материала:
Разморозку криоконсервированных фетальных хондроцитов производят на водяной бане, снабженной нагревательным элементом, регулятором температуры. Ампулы объемом 10,0 мл размораживают при температуре 37 0 С в течение 5,0 мин. При размораживании ампул соблюдать меры предосторожности.
После размораживания определяют концентрацию сохранившихся клеток, для чего в суспензию добавляли равный объем 0,2%-ного трипанового синего, окрашивающего мертвые клетки в синий цвет. Окрашенную суспензию заправляли в счетную камеру Горяева. Общий процент жизнеспособных клеток после разморозки должен составлять не менее 70% от общего количества клеток.
Определение дозы и кратности введения клеточного материала:
ТФСХ назначают однократно внутрь туннелей бедренной и большеберцовой костей, вблизи дефекта и в полость коленного сустава в виде суспензии 5,0мл.
Внутрисуставное артроскопопическое введение фетальных хондроцитов в коленный сустав:
Положение пациента на операционном столе на спине горизонтальное. Обработка операционного поля трижды 96°-20,0мл спиртом. Перидуральная анестезия. Двумя базовыми доступами в полость коленного сустава вводятся артроскоп и инструменты. Ревизия полости сустава, обильно промывается полость физиологическим раствором. На мыщелке бедренной и большеберцовой кости, вблизи дефекта, пункционной иглой проводится туннелизация. В каналы и в полость коленного сустава вводится взвесь фетальных стволовых хондроцитов в объеме 5мл соответствующей группы крови и резус фактора (рис.3). Накладываются послойные швы на операционные раны, асептическая давящая повязка.
Оценка качества проведенной ТФСХ в коленный сустав:
Возможные побочные явления: пациент может почувствовать небольшую боль в местах пункций во время введения пункционной иглы. После проведения ТФСХ возможны головная боль, тошнота, рвота, повышение температуры тела.
Возможные осложнения в области пункции, такие как воспалительный процесс тканей и спинного мозга. Накладывается давящая повязка и наблюдение в динамике в течение суток. В случае отсутствия осложнений пациент переводится в отделение.
После проведения трансплантации осуществляется динамическое наблюдение, контроль АД, ЧСС, температуры тела и ОАК в первые сутки после ТФСХ [3,13].

Трансплантация фетальных стволовых хондроцитов пункционным методом внутрь сустава:
Процедура состоит из 4 этапов:
· процедуры подготовки клеточного материала;
· определение дозы и кратности введения клеточного материала;
· внутрисуставное пункционное введение фетальных хондроцитов;
· оценка качества проведенной ТФСХ.
Процедуры подготовки клеточного материала:
Разморозку криоконсервированных фетальных хондроцитов производят на водяной бане, снабженной нагревательным элементом, регулятором температуры. Ампулы объемом 10,0 мл размораживают при температуре 37 0 С в течение 5,0 мин. При размораживании ампул соблюдать меры предосторожности.
После размораживания определяют концентрацию сохранившихся клеток, для чего в суспензию добавляли равный объем 0,2%-ного трипанового синего, окрашивающего мертвые клетки в синий цвет. Окрашенную суспензию заправляли в счетную камеру Горяева. Общий процент жизнеспособных клеток после разморозки должен составлять не менее 70% от общего количества клеток.
Определение дозы и кратности введения клеточного материала
ТФСХ назначают однократно внутрь коленного сустава в виде суспензии 5,0мл.
Внутрисуставное пункционное введение фетальных хондроцитов внутрь сустава:
Положение больного горизонтальное на спине. Обработка операционного поля трижды 96°-20,0мл спиртом.
Местная инфильтрационная анестезия. Местная анестезия раствором лидокаина 2%-2,0 мл. Длина иглы 5-6 см. Кожу в точке вкола сдвигают в сторону. Этим достигают искривления раневого канала, сделанного иглой. После извлечения иглы кожа возвращается на место. Такой прием препятствует проникновению инфекции в полость сустава с поверхности тела и вытеканию содержимого сустава. Вводится игла перпендикулярно поверхности кожи и за надколенник в горизонтальной плоскости. Глубина вкола иглы не более 1,5-2,5 см. Внутрисуставно в полость коленного сустава вводится взвесь соответствующей группы крови и резус фактора фетальных хондроцитов в объеме 5мл. Накладывается асептическая давящая повязка
Оценка качества проведенной ТФСХ в тазобедренный сустав:
Возможные побочные явления: пациент может почувствовать небольшую боль в местах пункций во время введения пункционной иглы. После проведения ТФСХ возможны головная боль, тошнота, рвота, повышение температуры тела.
Возможные осложнения в области пункции, такие как воспалительный процесс тканей и спинного мозга. Накладывается давящая повязка и наблюдение в динамике в течение суток. В случае отсутствия осложнений пациент переводится в отделение.
После проведения трансплантации осуществляется динамическое наблюдение, контроль АД, ЧСС, температуры тела и ОАК в первые сутки после ТФСХ [3,13].
Трансплантация фетальных стволовых гепатоцитов, нефроцитов или клеток поджелудочной железы.
Процедура состоит из 4 этапов:
· процедуры подготовки клеточного материала;
· определение дозы и кратности введения клеточного материала;
· внутривенное введение фетальных стволовых гепатоцитов, нефроцитов или клеток поджелудочной железы;
· оценка качества проведенной ТФСГ, ТФСНф или ТФСКПЖ.
Процедуры подготовки клеточного материала:
Разморозку криоконсервированных фетальных стволовых гепатоцитов, нефроцитов или клеток поджелудочной железы производят на водяной бане, снабженной нагревательным элементом, регулятором температуры. Ампулы объемом 10,0 мл размораживают при температуре 37 0 С в течение 5,0 мин. При размораживании ампул соблюдать меры предосторожности.
После размораживания определяют концентрацию сохранившихся клеток, для чего в суспензию добавляли равный объем 0,2%-ного трипанового синего, окрашивающего мертвые клетки в синий цвет. Окрашенную суспензию заправляли в счетную камеру Горяева. Общий процент жизнеспособных клеток после разморозки должен составлять не менее 70% от общего количества клеток.
Определение дозы и кратности введения клеточного материала:
ТФСГ, ТФСНф или ТФСКПЖ назначают однократно внутривенно коленного сустава в виде суспензии 5,0мл разведенной в 20,0 мл 0,9% раствора натрия хлорид.
Внутривенное введение фетальных стволовых гепатоцитов, нефроцитов или клеток поджелудочной железы:
Положение больного горизонтальное на спине. Обработка операционного поля трижды 96°-20,0мл спиртом. Установка внутривенного периферического катетера. Инфузия фетальных клеток человека соответствующей группы крови и резус фактора со скоростью 40-50 капель в минуту. Время трансфузии клеток в среднем составляет 30-40 мин.
Оценка качества проведенной ТФСГ, ТФСНф или ТФСКПЖ:
Возможные побочные явления: пациент может почувствовать небольшую боль в местах пункций во время введения пункционной иглы. После проведения ТФСГ, ТФСНф или ТФСКПЖ возможны головная боль, тошнота, рвота, повышение температуры тела.
Возможные осложнения в области пункции, такие как воспалительный процесс тканей и спинного мозга. Накладывается давящая повязка и наблюдение в динамике в течение суток. В случае отсутствия осложнений пациент переводится в отделение.
После проведения трансплантации осуществляется динамическое наблюдение, контроль АД, ЧСС, температуры тела и ОАК в первые сутки после ТФСГ, ТФСНф или ТФСКПЖ [1,20,21,22,24,28,29,42].
Трансплантация фетальных стволовых тиреоцитов:
Процедура состоит из 5 этапов:
· процедуры подготовки клеточного материала;
· исследование положения и размера щитовидной железы;
· определение дозы и кратности введения клеточного материала;
· селективное введение фетальных стволовых тиреоцитов;
· оценка качества проведенной ТФСТ.
Процедуры подготовки клеточного материала:
Разморозку криоконсервированных фетальных тиреоцитов производят на водяной бане, снабженной нагревательным элементом, регулятором температуры. Ампулы объемом 10,0 мл размораживают при температуре 37 0 С в течение 5,0 мин. При размораживании ампул соблюдать меры предосторожности.
После размораживания определяют концентрацию сохранившихся клеток, для чего в суспензию добавляли равный объем 0,2%-ного трипанового синего, окрашивающего мертвые клетки в синий цвет. Окрашенную суспензию заправляли в счетную камеру Горяева. Общий процент жизнеспособных клеток после разморозки должен составлять не менее 70% от общего количества клеток.
Исследование положения и размера щитовидной железы:
Положение больного горизонтальное на спине. Производится ультразвуковое сканирование щитовидной железы или её культи, определяется форма, размеры и объем железы, расстояние от передней поверхности шеи до железы, а также положение общей сонной артерии (рис.4). Определяется точка пункции на коже передней поверхности шеи.
Определение дозы и кратности введения клеточного материала:
ТФСТ назначают однократно внутрь паренхимы обеих долей щитовидной железы или в культи в виде суспензии по 0,5 мл.
Селективное введение фетальных стволовых тиреоцитов:
Область прокола обрабатывается трижды 96°-20,0мл спиртом. Без применения анестезии производится пункция иглой от одноразового 5,0мл шприца. Игла продвигается под контролем датчика УЗИ – аппарата строго перпендикулярно передней поверхности шеи до капсулы щитовидной железы или её культи. Пункция щитовидной железы или ее культи в переднезаднем направлении, под ультразвуковой визуализацией. После достижения кончика иглы капсулы железы, покрывающей её заднюю поверхность, дробно болюсно вводится взвесь фетальных тиреоцитов, по мере продвижения иглы в обратном направлении, в объеме 0,5-1,0 мл.
Оценка качества проведенной ТФСТ:
Возможные побочные явления: пациент может почувствовать небольшую боль в месте пункции во время введения пункционной иглы. После проведения ТФСТ возможны головная боль, тошнота, рвота, повышение температуры тела.
Возможные осложнения в виде воспалительного отека в области пункции, потеря речи. Накладывается давящая повязка, лед на область раны, противовоспалительная терапия и наблюдение в динамике в течение суток. В случае отсутствия осложнений пациент переводится в отделение.
После проведения трансплантации осуществляется динамическое наблюдение, контроль АД, ЧСС, температуры тела и ОАК в первые сутки после ТФСТ [1,20].

Индикаторы эффективности:
Трансплантации фетальных стволовых гепатоцитов [20,42,50]:
Долгосрочные критерии эффективности ТФСГ:
Уменьшение на один класс степени тяжести цирроза печени с использованием суммы баллов по данным шкалы Сhild-Turcotte Pugh для оценки степени печеночно-клеточной недостаточности:
а) Снижение степени тяжести цирроза печени с класса В на класс А по системе Сhild-Turcotte Pugh в течении 1-3 лет по критериям: асцита и энцефалопатии нет, билирубин 3,5г/дл и ПВ 130 градусов;
· функция коленных суставов оценивается по критериям И. Инсалл, тазобедренных суставов по критериям Харриса;
· рентгенологически: подсчитывается число суставов с эрозиями. Индекс Ларсена-Дейла вычисляется отдельно для крупных суставов – коленных, локтевых, тазобедренных (общий счет 0-30) и мелких суставов кистей и стоп (общий счет 0-200); определяется модифицированный индекс Шарпа, отражающий число эрозий и выраженность сужений межс
уставных щелей в суставах кистей и стоп.
Препараты (действующие вещества), применяющиеся при лечении
Информация
Источники и литература
Информация
Список разработчиков:
1) Туганбекова Салтанат Кенесовна – доктор медицинских наук, профессор, заместитель генерального директора по научной работе АО «Национальный научный медицинский центр», главный внештатный нефролог МЗСР РК.
2) Исмаилова Гульзия Нуртазаевна – кандидат медицинских наук, руководитель отдела научного менеджмента и доказательной медицины АО «Национальный научный медицинский центр».
3) Аскаров Манарбек Бапович – доктор медицинских наук, руководитель Центра клеточных технологий и трансплантации АО «Национальный научный медицинский центр».
4) Сапарбаев Самат Сагатович – кандидат медицинских наук, руководитель отдела трансплантации фетальных клеток АО «Национальный научный медицинский центр».
5) Идрисова Сахипжамал Шакировна – невропатолог, руководитель отдела нейро-трансплантации АО «Национальный научный медицинский центр».
6) Рахметова Венера Саметовна – доктор медицинских наук, руководитель научного отдела гепатологии АО «Национальный научный медицинский центр».
7) Кузембаева Карлыгаш Уразалиновна – кандидат медицинских наук, ведущий научный сотрудник отдела гепатологии АО «Национальный научный медицинский центр».
8) Криворучко Наталья Алексеевна – ревматолог, руководитель научного отдела ревматологии и нефрологии АО «Национальный научный медицинский центр».
9) Зарипова Лина Ниязовна – старший научный сотрудник отдела ревматологии и нефрологии АО «Национальный научный медицинский центр».
10) Таубалдиева Жаннат Сатыбаевна – кандидат медицинских наук, руководитель отдела эндокринных нарушений АО «Национальный научный медицинский центр».
11) Ульянова Ольга Владимировна – кандидат медицинских наук, ведущий научный сотрудник отдела эндокринных нарушений АО «Национальный научный медицинский центр».
12) Туребеков Зайырхан Темирханович – научный сотрудник отдела ревматологии и нефрологии АО «Национальный научный медицинский центр».
Указание на отсутствие конфликта интересов: отсутствует.
Рецензенты:
1. Туребеков Думан Кажибаевич – доктор медицинских наук, доцент главный внештатный нефролог по городу Астана, заведующий отделением нефрологии ГКП на ПХВ «Городская больница №1» Управления здравоохранения города Астаны;
2. Жариков Серик Нагашыбаевич – доктор медицинских наук, главный внештатный трансплантолог МЗСР РК, заместитель директора учреждения «Республиканский координационный центр по трансплантации»;
Указания условий пересмотра протокола: пересмотр протокола через 3 года после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.