как называется внеклеточная форма существования вирусной частицы
Что мы знаем о вирусах и методах защиты от них?
Что такое вирус?
Как устроен вирус?
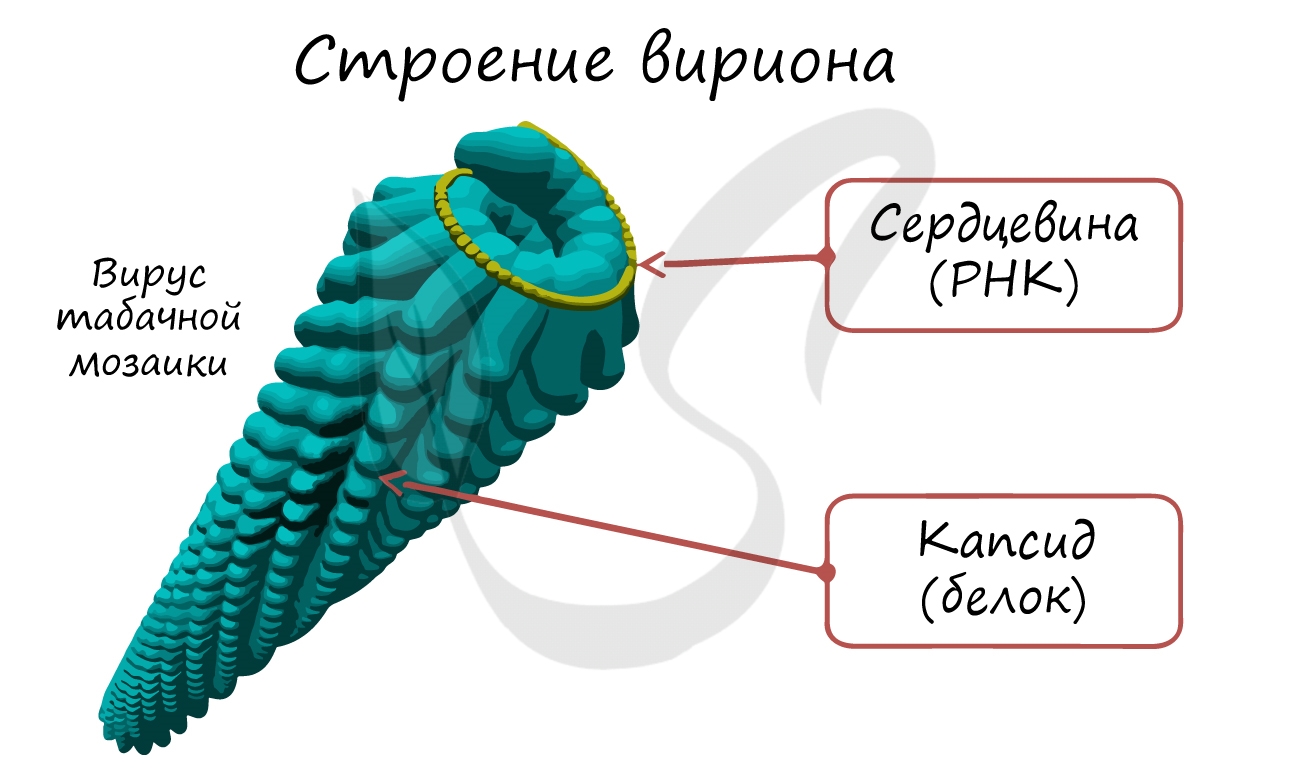
В центре агента находится генетический материал РНК или ДНК, вокруг которого располагается белковая структура — капсид.
Капсид служит для защиты вируса и помогает при захвате клетки. Некоторые вирусы дополнительно покрыты липидной оболочкой, т.е. жировой структурой, которая защищает их от изменений окружающей среды.
Вирусолог Дэвид Балтимор объединил все вирусы в 8 групп, из которых некоторые группы вирусов содержат 1-2 цепочки ДНК. Другие же содержат 1 цепочку РНК, которая может удваиваться или достраивать на своей матрице ДНК. При этом каждая группа вирусов производит себя в различных органеллах зараженной клетки.
Вирусы имеют определенный диапазон хозяев, т.е. он может быть опасен для одних видов и абсолютно безвреден для других. Например, оспой болеет только человек, а чумкой только некоторые виды плотоядных. Вирус не способен выжить сам по себе, поэтому активируется только в хозяйской клетке, используя ее ресурсы и питательные вещества. Цель вируса — создание множества копий себя, чтобы инфицировать другие клетки!
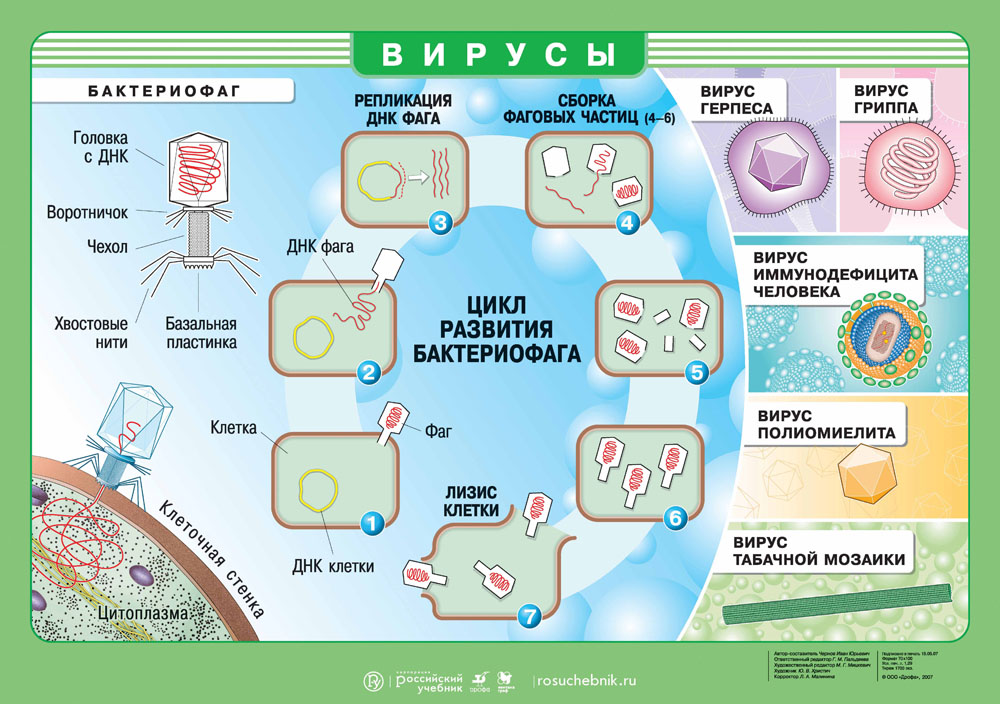
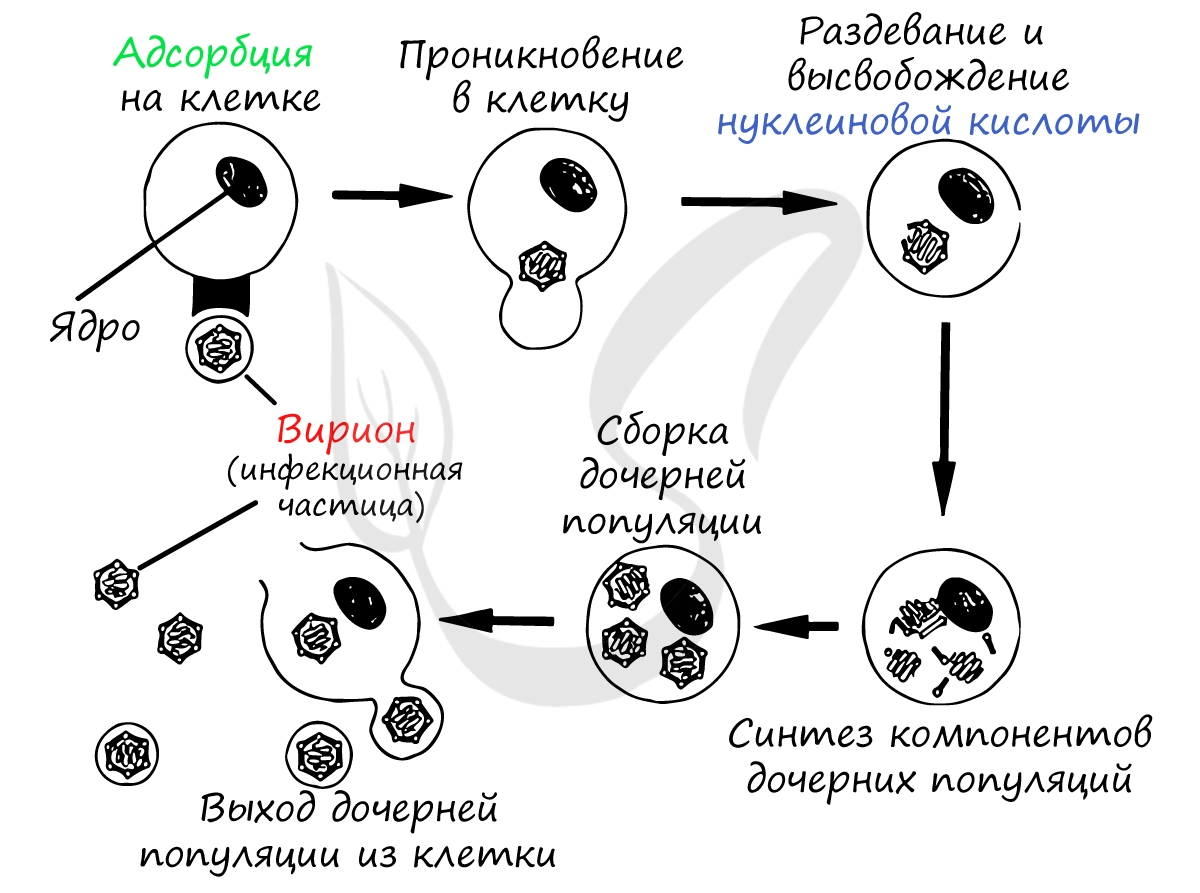
Вирусы. Цикл развития бактериофага. Скачать наглядное пособие в большом разрешении можно здесь.
Как вирус попадает в организм?
Геном вируса встраивается в одну из органелл или цитоплазму и превращает клетку в настоящий вирусный завод. Естественные процессы в клетке нарушаются, и она начинает заниматься производством и сбором белка вируса. Этот процесс называется репликацией. И его основная цель — это захват территории. Во время репликации генетический материал вируса смешивается с генами клетки хозяина — это приводит к активной мутации самого вируса, а также повышает его выживаемость. Когда процесс репликации налажен, вирусная частица отпочковывается и заражает уже новые клетки, в то время как инфицированная ранее клетка продолжает производство.
«Для проникновения в клетку белки поверхности вируса связываются со специфическими поверхностными белками клетки. Прикрепление, или адсорбция, происходит между вирусной частицей и клеточной мембраной. В мембране образуется дырка, и вирусная частица или только генетический материал попадают внутрь клетки, где будет происходить размножение вируса. Сегодня ученые всего мира сделали важное открытие о том, что заражение коронавирусом людей преклонного возраста объясняется тем, что у пожилых людей накапливается специфический белок, который помогает COVID-19 проникать внутрь клетки эпителия».
Выход вируса
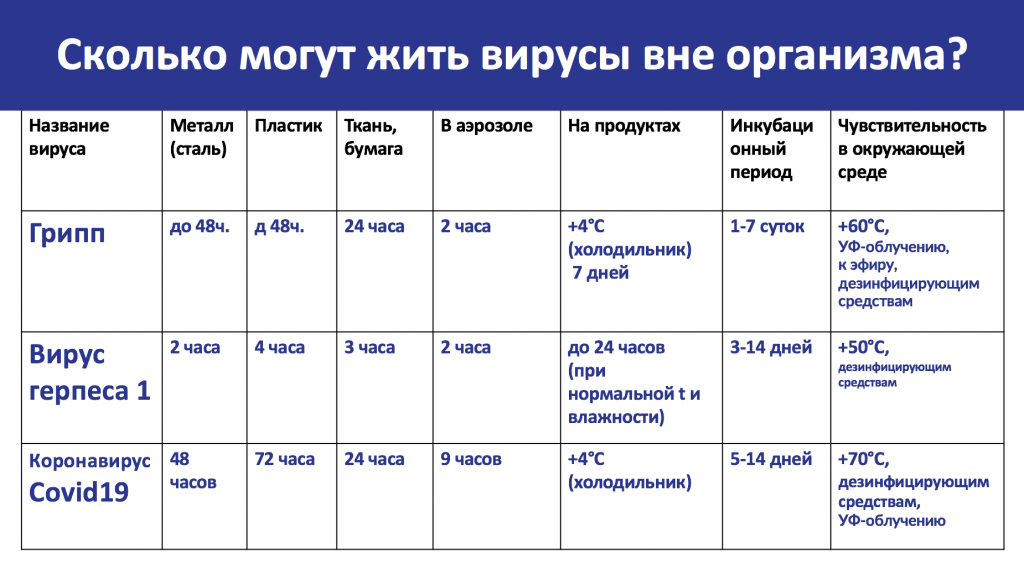
Скорость распространения вирусной инфекции
Вирусная латентность
Как вирус распространяется?
Почему с вирусами так тяжело бороться?
Сегодня людям уже удалось победить некоторые вирусы, а некоторые взять под жесткий контроль. Например, Оспа (она же черная оспа). Болезнь вызывается вирусом натуральной оспы, передается от человека к человеку воздушно-капельным путем. Больные покрываются сыпью, переходящей в язвы, как на коже, так и на слизистых внутренних органов. Смертность, в зависимости от штамма вируса, составляет от 10 до 40 (иногда даже 70%), На сегодняшний день вирус полностью истреблен человечеством.
Кроме того, взяты под контроль такие заболевания, как бешенство, корь и полиомиелит. Но помимо этих вирусов существует масса других, которые требуют разработок или открытия новых вакцин.
Коронавирус
К наиболее распространенным симптомам COVID-19 относятся повышение температуры тела, сухой кашель и утомляемость. К более редким симптомам относятся боли в суставах и мышцах, заложенность носа, головная боль, конъюнктивит, боль в горле, диарея, потеря вкусовых ощущений или обоняния, сыпь и изменение цвета кожи на пальцах рук и ног. Как правило, эти симптомы развиваются постепенно и носят слабо выраженный характер. У некоторых инфицированных лиц болезнь сопровождается очень легкими симптомами.
Поскольку пока не изобретено вакцины от COVID-19, в целях защиты от инфекции самым важным для нас является соблюдение гигиены.
Гигиена — раздел медицины, изучающий влияние жизни и труда на здоровье человека и разрабатывающая меры (санитарные нормы и правила), направленные на предупреждение заболеваний, обеспечение оптимальных условий существования, укрепление здоровья и продление жизни.
Сегодня следует соблюдать определенные правила гигиены:
«Мы пытались рассказать Вам не только о существующих научных фактах о вирусах, но и показать, что определенные знания помогают нам в нынешней практической ситуации сохранить свое здоровье и здоровье своих близких. Мы понимаем, что сегодня коронавирус может находиться практически везде: на поверхностях любых предметов, в окружающей среде и т.д. Поэтому самоизоляция – это один из важнейших способов защиты от инфекции. Находясь дома, вы защищаете не только свое здоровье, но и помогаете медикам и ученым, которые сражаются с этим вирусов и день и ночь. Ведь, чем меньше шансов у нас с вами заболеть, тем больше шансов появляется у них, чтобы победить коронавирус. Пожалуйста, оставайтесь дома и соблюдайте режим самоизоляции и нормы гигиены».
Убить невидимого убийцу. Все о вирусах и методах борьбы с ними
Алевтина Боголюбова-Кузнецова СПИД.ЦЕНТР
Вирусы у всех на слуху. С одними мы неизбежно сталкиваемся лично, например, с вирусами гриппа или теми, что вызывают простуду. Другие будоражат медицинское сообщество, наводняют новости и становятся зловещими прообразами для популярной литературы и кино.
И это неудивительно хотя бы потому, что вирусы — штука довольно непонятная. Неясно даже, считать их живыми или нет. С одной стороны, это просто хрупкий набор молекул, который не может существовать автономно, без живой клетки. Он не производит и не накапливает энергии, а также не поддерживает постоянства внутренней среды — ее попросту нет. Но когда вирус попадает в клетку, он проходит жизненный цикл, копирует себя и эволюционирует. Невидимое глазу нечто существует в огромном количестве, постоянно меняется, переходит от одних хозяев к другим и причиняет страдания разной степени тяжести всему человечеству.
Как устроены вирусы?
Вирусная частица, или вирион, — это нуклеиновая кислота (ДНК или РНК) в обертке из белков. В некоторых случаях она покрыта дополнительным слоем липидов, «украденных» у клетки-хозяина. У вирусов есть своя классификация: царства, семейства и прочие таксоны (группы), за списком которых следит Международный комитет по таксономии вирусов. Самый большой таксон — реалм. Сейчас ученые выделяют четыре реалма, из которых три — ДНК-содержащие вирусы. К ним относятся, например, вирусы оспы, герпеса и папилломавирусы.
РНК-содержащие вирусы можно разделить на собственно РНК-вирусы и ретровирусы. Первые — это вирусы гриппа, бешенства, гепатита С, а также коронавирусы и вирус Эбола. Они содержат РНК и используют для размножения РНК-зависимую РНК-полимеразу, с ее помощью на исходной молекуле РНК сразу синтезируется новая. А к ретровирусам относится, например, ВИЧ. Он содержит РНК, но в ходе жизненного цикла она превращается в ДНК и встраивается в геном клетки-хозяина. После чего новая РНК синтезируется уже на основе молекулы ДНК — то есть так же, как у нас.
Как с ними бороться?
Можно выделить три стратегии борьбы с вирусами. Первая — «пожар проще предотвратить, чем потушить». Защититься от заражения можно по-разному, например, избегать незащищенного секса или контакта с зараженной кровью. Более изощренный способ — контроль природных резервуаров вируса: осушение болот (чтобы предотвратить вспышки желтой лихорадки), карантин, вакцинация или отстрел животных.
Еще одна стратегия — активная и пассивная иммунопрофилактика. Активная — это простая и всем знакомая вакцинация. Человеку вводят неактивную форму вируса или его кусочек, в организме срабатывает иммунный ответ и синтезируются антитела, которые защитят человека в будущем, если он когда-нибудь встретится с настоящим живым вирусом. Но вакцину не всегда можно создать, да и уже существующие порой не работают на все сто. Так, вакцина от гриппа защищает только от нескольких — самых распространенных в текущем сезоне — штаммов (видов) вируса. Пассивная иммунопрофилактика — это введение готовых антител тем, кто уже встретился с вирусом или с большой вероятностью сделает это. Такие лекарства существуют для респираторно-синцитиального вируса (рекомендованы недоношенным младенцам) и ветряной оспы (для людей с подавленным иммунитетом).
И, наконец, последняя стратегия на случай, если ничто не помогло и человек заболел, — антивирусные препараты. Их развитие подстегивали научный прогресс и насущные проблемы. Чтобы придумать противовирусный препарат, нужно сначала изучить вирус и его жизненный цикл и выбрать возможные мишени для атаки. Причем такие, чтобы они как можно сильнее отличались от человеческих аналогов. Иначе лекарство будет бороться и с вирусами, и с невинными человеческими клетками, вызывая сильные побочные эффекты.
Первые клеточные культуры, в которых можно было имитировать взаимодействие вируса с хозяином, появились в 1950-х годах. До этого удобных моделей in vitro (в пробирке) не существовало, и изучение вирусов было затруднено. Уже в 1963 году появился первый антивирусный препарат — идоксуридин. Это был нуклеозидный аналог дезоксиуридина — одного из четырех «кирпичиков» молекулы ДНК. Препарат до сих пор используется при лечении герпеса.
В 80-е произошло другое громкое открытие — вирус иммунодефицита человека. Это породило шквал научных работ, посвященных разработке новых противовирусных лекарств. К тому времени связанный с ним СПИД уже распространился по миру, а в США началась эпидемия.
Какие бывают антивирусные препараты?
Их можно разделить на 13 групп, причем к шести относятся различные лекарства против ВИЧ. Это ингибиторы входа вируса в клетку, вирусных ферментов интегразы и протеазы, а также три вида ингибиторов вирусного фермента обратной транскриптазы, или ревертазы. Все они действуют на разные этапы жизненного цикла вируса:
1. Проникновение в клетку
Это первое, что должен сделать вирус, попав в организм. То, какую клетку он поразит, определяется рецептором на ее поверхности. У ВИЧ это рецептор CD4, который есть у Т-хелперов, макрофагов, а также некоторых других видов клеток. Кроме него в связывании вируса и его проникновении участвуют: рецепторы CXCR4 и CCR5 со стороны клетки и поверхностные гликопротеины gp120 и gp41 — со стороны вируса.
Сейчас FDA (американское Управление по санитарному надзору за качеством пищевых продуктов и медикаментов) одобряет четыре лекарства, работающие на этой стадии. Каждый связывается с каким-то из участников процесса и мешает его работе. Например, к этой группе принадлежит самый новый препарат против ВИЧ — фостемсавир, его одобрили в США в июле 2020 года. В организме он превращается в активную форму темсавир, соединяется с вирусным гликопротеином gp120 и мешает ему связаться с клеточным рецептором CD4. Другой препарат — ибализумаб — связывается с самим CD4, причем так, что рецептор не может участвовать в проникновении вируса, но выполняет свою нормальную иммунную функцию — связывает и узнает антигены на поверхности антигенпрезентирующих клеток.
Подобные препараты также используются для лечения респираторно-синцитиального вируса, вирусов ветряной оспы и простого герпеса. Они тоже действуют на вирусные гликопротеины и их связывание с клеточными рецепторами. К этой же группе можно отнести препараты для пассивной иммунопрофилактики антителами.
2. Подготовка к размножению, часть 1
Когда вирус попал в клетку, он должен в ней размножиться, то есть создать копии себя, используя ресурсы самой клетки. Так как ВИЧ — ретровирус, его генетический материал — РНК, которая должна достроиться до двухцепочечной ДНК и встроиться в ДНК клетки. Процесс достраивания называется обратной транскрипцией, и для него необходим вирусный фермент обратная транскриптаза, ее еще называют ревертазой. Это самая популярная мишень препаратов против ВИЧ, которые делятся на две группы: нуклеозидные и ненуклеозидные.
3. Подготовка к размножению, часть 2
Чтобы наконец размножиться, ВИЧ, уже в виде молекулы ДНК, необходимо встроиться в геном клетки-хозяина. В этом участвует другой вирусный фермент — интеграза. Ее ингибируют несколько одобренных лекарств, причем они часто используются вместе с другим препаратом — кобицистатом. Он никак не действует на вирус, но ингибирует некоторые ферменты печени и увеличивает биодоступность самих антивирусных препаратов.
Попав в геном, вирус может запустить транскрипцию и синтезировать новые РНК и белки. А может и «заснуть». Именно поэтому ВИЧ почти нельзя вылечить: всегда останутся клетки со «спящим» вирусом, который себя не проявляет, а значит, не может быть мишенью для атаки. Активация вируса связана с активацией клетки. Так как ВИЧ инфицирует в основном иммунные клетки, именно те из них, что борются с инфекцией, и становятся его жертвой.
4. Созревание
Белки ВИЧ синтезируются в виде длинных полипротеинов, которые нужно «нарезать», чтобы получить зрелые формы. Для этого необходим вирусный фермент протеаза. Это — вторая по популярности мишень антивирусных препаратов. Большинство из них — белковые аналоги вирусного полипептида. Они ингибируют работу фермента, и зрелые вирусные белки и новые вирусные частицы не образуются. Подобно ингибиторам обратной транскриптазы, к препаратам из этой группы тоже очень быстро развивается резистентность. И, как и с ингибиторами вирусной интегразы, с ними часто используется кобицистат.
Препараты ингибирования вирусной протеазы также существуют для лечения вируса гепатита С. Несмотря на большие отличия в структуре и способе репликации, белки этого вируса тоже синтезируются в незрелой форме, которую нужно «нарезать».
Другие препараты
Есть три группы антивирусных препаратов, которые мы еще не упоминали. Во-первых, это ингибиторы белков NS5A и NS5B вируса гепатита С, которые играют важную роль в репликации РНК вируса. Во-вторых, лекарства против вируса гриппа: три ингибитора вирусного белка нейраминидазы и один ингибитор РНК-полимеразы вируса. И, наконец, сборная солянка препаратов, которые не действуют прицельно на вирусные компоненты. Это интерфероны, а также иммуностимуляторы и ингибиторы митоза клеток.
Первые заслуживают особого внимания из-за обилия отечественных лекарств против гриппа и простуды на их основе. FDA одобряет инъекции (!) интерферонов только для лечения гепатита B и С, причем на практике они используются очень осторожно из-за серьезных побочных эффектов. Отечественные противовирусные препараты с интерферонами, которые выпускаются в форме мазей, спреев и суппозиториев, вряд ли работают. И слава богу. Иммуностимуляторы и ингибиторы митоза клеток выпускаются в виде мазей и используются для лечения генитальных бородавок, то есть папилломавируса человека.
Наука не стоит на месте, и разработка противовирусных препаратов продолжается, подстегиваемая новыми вирусами, эпидемиями, а также развитием резистентности к существующим лекарствам. Но по-прежнему самыми изученными и многочисленными препаратами остаются ингибиторы вирусных обратной транскриптазы или ДНК-полимеразы и протеазы. Для разработки других стратегий борьбы ученым еще предстоит изучить детали работы вирусов — как давно известных, так и совершенно новых.
Да, вирусы остаются источником зловещих идей в популярной культуре. Но существующих препаратов и методов уже достаточно, чтобы мы могли избежать заражения, быстро вылечиться или свести негативные последствия болезни к нулю.
Вирусы
Вирусы способны размножаться только внутри живых клеток, до проникновения в них вирусы не имеют признаков жизни: пассивно перемещаются во внешней среде, ожидая встречи с клеткой-мишенью.
В 1892 году Ивановский Д.И. в ходе изучения мозаичной болезни табака обнаружил, что болезнь вызывается мельчайшими субстанциями, которые проходят через бактериальный фильтр, то есть были меньше бактерий. Вирусы впервые увидели в электронный микроскоп в 1939 году (спустя 19 лет со смерти Ивановского), однако считается, что именно Ивановский положил начало вирусологии как науке.
У вирусов отсутствует обмен веществ с внешней средой (метаболизм).
Не имеют клеточной мембраны, ограничивающих их от внешней среды, и, соответственно, клеточного строения.
У вирусов отсутствует половое размножение и деление. Попав в живую клетку, вирус встраивает свою нуклеиновую кислоту (РНК/ДНК) в наследственный материал клетки-мишени. В результате клетка начинает синтезировать вирусные белки (новые вирусы): так увеличивается численность вирусов.
Носителем наследственной информации у вирусов может быть ДНК, РНК. В связи с этим все вирусы подразделяются на ДНК- и РНК-содержащие.
Взаимодействие вируса с клеткой
Найдя клетку, на поверхности которой есть подходящий рецептор, вирус взаимодействует с ним и прикрепляется к мембране клетки. Путем эндоцитоза (образование вакуоли) вирус проникает внутрь клетки, выходит из вакуоли в цитоплазму. Наследственный материал (ДНК/РНК) вируса реализуется по схеме: ДНК ↔ РНК → белок.
Образовавшиеся белки объединяются в вирусные частицы, которые могут выходить из клетки разными путями. Вирионы вирусов гепатита C выходят из клетки путем почкования (экзоцитозом), при таком варианте клетка долгое время остается живой и служит для продукции новых вирионов.
Известен и другой механизм выхода вирионов из клетки: взрывной, при котором оболочка клетки разрывается, и тысячи вирионов отправляются инфицировать новые клетки. Такой способ характерен для аденовирусов, ротавирусов.
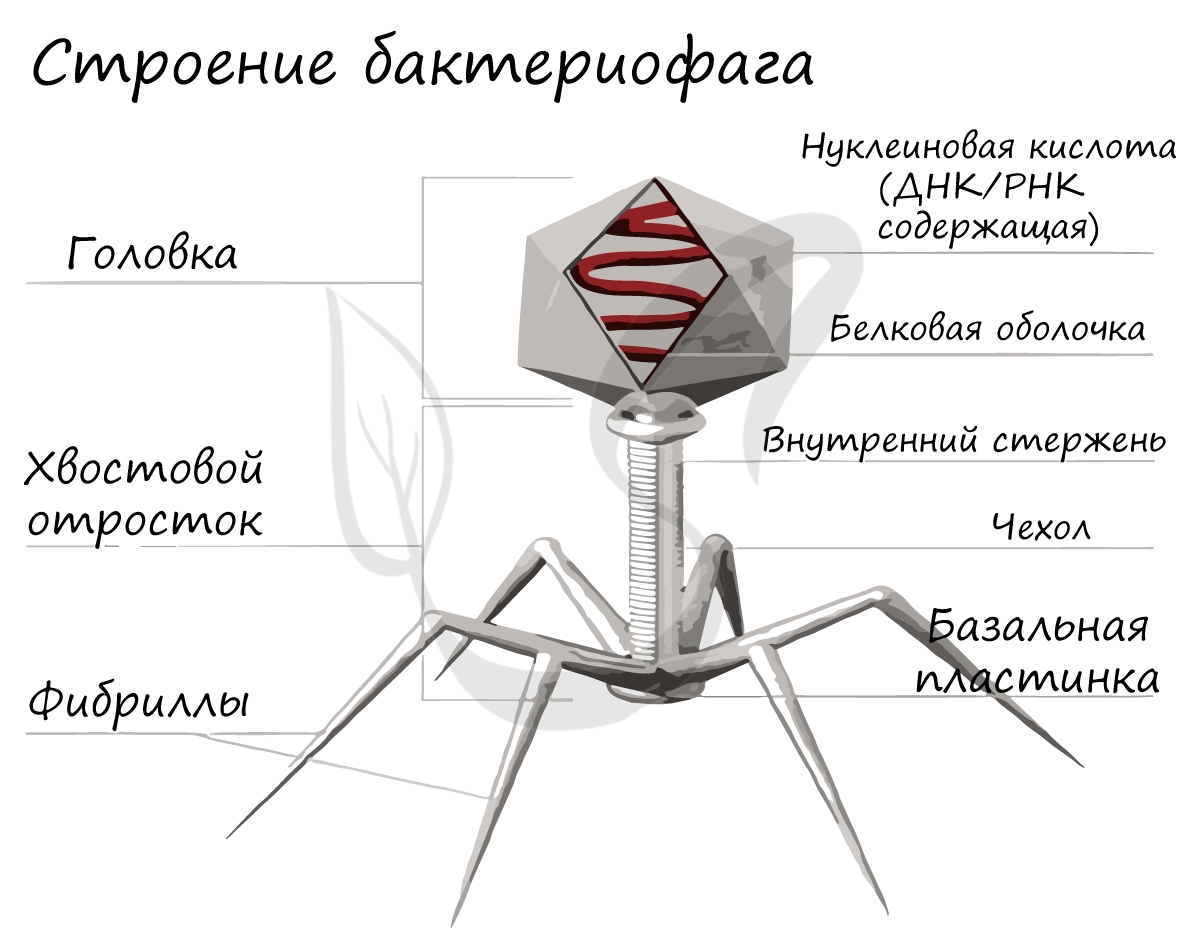
Бактериофаги («бактерия» + греч. phag(os) — пожирающий)
Ниже вы можете видеть типичное строение бактериофага. Бактериофаг напоминает шприц, который протыкает стенку бактерии и впрыскивает внутрь нее свою нуклеиновую кислоту.
Бактериофаги успешно применяются в медицине для лечения многих заболеваний. Это высокоэффективные, дорогостоящие препараты, которые помогают, например, нормализовать микрофлору кишечника при бактериальных инфекциях.
Вирусные инфекции
Вирусы вызывают множество заболеваний человека и животных. Некоторые из них неизлечимы даже на современном этапе развития медицины, например бешенство. К вирусным инфекциям относятся грипп, корь, свинка, СПИД (вызванный ВИЧ), полиомиелит, желтая лихорадка, онковирусы.
Такая группа, как онковирусы, потенцируют развитие опухолей в организме. К ВИЧ и онкогенным вирусам не существует специфических антител, что затрудняет процесс создания вакцины. В то же время против ряда вирусных инфекций: корь, ветряная оспа созданы вакцины, создающие стойкий пожизненный иммунитет.
Риск заражения ВИЧ присутствует при гемотрансфузии (переливании крови), половом акте. Инфекция также может быть передана от ВИЧ инфицированной матери к плоду.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Как называется внеклеточная форма существования вирусной частицы
В журнале Nature опубликован очень подробный обзор, характеризующих особенности строения и жизненный цикл SARS-CoV2, механизмы инфицирования и избегания своевременного иммунного ответа, обозначены потенциальные мишени для создания противовирусных препаратов. Также представлены результаты компьютерного моделирования строения вируса и механизмов проникновения в клетку.
Особенностью данного вируса является наличие очень большого количества гликанов на поверхности спайк-протеина, маскирующих его от иммунной системы человека. Поэтому на первом этапе заболевания вирус подобен «волку в овечьей шкуре» и остается невидим для иммунной системы. В дальнейшем, когда вирус уже размножился, иммунный ответ может развиться даже избыточно, что, по-видимому, лежит в основе тяжелого течения заболевания.
В S2- субъединице спайк-протеина есть три участка, делающих «ножку» спайк-протеина гибкой, что позволяет ей «искать» рецепторы на клетках хозяина более эффективно. Такая структура довольно редка для вирусов, обычно аналогичные «шипики» на поверхности вириона ригидны (такова, например, ситуация у вируса гриппа).
Важной частью спайк-протеина является RBD-домен, функцией которого является связь с рецептором ACE2 на поверхности клетки-хозяина. У SARS-CoV2 эта связь в 2-4 раза сильнее, чем у вируса SARS. Во время взаимодействия с рецептором этот домен «выдвигается» из-за двух маскирующих его молекул гликанов. Исследования in vitro показали, что мутации в этих двух гликанах могут полностью нарушать процессы проникновения вируса в клетку. Для эффективного взаимодействия RDB и ACE2 предпочтительна более «высокая» позиция этого домена на остальными структурами. У альфа варианта вируса найдено 10 дополнительных мутаций, приводящих RBD – домен в более «высокое» положение, а у дельта вируса – еще 3 мутации.
Попав в клетку, вирус подавляет экспрессию генов клетки-хозяина, в том числе – образование интерферонов, сигнализирующих о вирусной инфекции. Для ковидной инфекции типична очень низкая концентрация интерферонов в крови.
В дальнейшем может происходить формирование синцитиев из клеток легочной ткани. Считается, что синцитии позволяют дольше и эффективнее вырабатывать вирусные белки. Такой тип агрессии типичен для персистирующих вирусов – например, ВИЧ. SARS-CoV2 индуцирует даже формирование синцитиев клеток респираторного эпителия с лимфоцитами, что мешает нормальному иммунному ответу. Такой тип «маскировки» от иммунитета типичен для опухолей, а не вирусов.
В дальнейшем перестраивается эндоплазматический ретикулум с формированием шарообразных двухмембранных структур, в которых происходит активный синтез белков вируса. Выход вирионов наружу осуществляется в лизосомах, формирующихся в комлексе Гольджи, путем экзоцитоза. Считается, что молекулярные механизмы, ответственные за описанные процессы, могут быть мишенями для противовирусной терапии.
В месте соединения S1 и S2 субъединиц спайк-протеина есть зона, которая способна связывать и быть расщепленной фурином – протеазой клетки-хозяина, содержащейся в лизосомах. Такое предварительное расщепление значительно упрощает в дальнейшем взаимодействие с трансмембранной протеазой TMPRSS2 и значительно увеличивает проникновение вирусной частицы в следующую клетку. Для вируса SARS показано, что порядка 10% вирусных частиц на выходе из клетки – хозяина связано с фурином. У вируса SARS-CoV2 в соответствующем локусе, отвечающем за связь с фурином, идентифицированы мутации. Как следствие, до 50% вирионов альфа-разновидности SARS-CoV2, выходящих из клетки-хозяина, связаны с фурином, а в случае дельта-вируса – до 90%, что, по-видимому, и объясняет более агрессивное распространение этого варианта вируса. Есть данные, что у пациентов с дельта-формой в тканях легких и носоглотки содержание вирионов достоверно выше, чем у носителей альфа-формы.
По материалам: Megan Scudellari. How the coronavirus infects cells — and why Delta is so dangerous. Nature 595, 640-644 (2021). doi:
Как называется внеклеточная форма существования вирусной частицы
Репетитор по Химии и Биологии
Главная • Биология • Химия • Резюме • Цены • Контакты
Биология  | ||
Программа  | Конспекты  | Контрольные работы  |
Репетитор по Биологии
Конспекты
На этой странице Вы можете найти конспект на тему «Вирусы и фаги».
Эволюционное происхождение вирусов
Жизненный цикл вируса начинается с проникновения внутрь клетки. Для этого он связывается со специфическими рецепторами на ее поверхности и:
а) либо вводит свою нуклеиновую кислоту внутрь клетки, оставляя белки вириона на ее поверхности,
б) либо проникает целиком в результате эндоцитоза. В последнем случае после проникновения вируса внутрь клетки следует его «раздевание» — освобождение геномных нуклеиновых кислот от белков оболочки.
В результате вирусный геном становится доступным для ферментных систем клетки, обеспечивающих экспрессию генов вируса. Именно после проникновения вирусной геномной нуклеиновой кислоты в клетку заключенная в ней генетическая информация расшифровывается генетическими системами хозяина и используется для синтеза компонентов вирусных частиц.
По сравнению с геномами других организмов вирусный геном относительно мал и кодирует лишь ограниченное число белков, в основном белки капсида и один или несколько белков, участвующих в репликации и экспрессии вирусного генома. Необходимые метаболиты и энергия поставляются хозяйской клеткой.
Строение и классификация вирусов
Вирусы нельзя увидеть в оптический микроскоп, так как их размеры меньше длины световой волны. Разглядеть их можно лишь с помощью электронного микроскопа.
Вирусы состоят из следующих основных компонентов:
Капсиды и дополнительная оболочка несут защитные функции, как бы оберегая нуклеиновую кислоту. Кроме того, они способствуют проникновению вируса в клетку. Полностью сформированный вирус называется вирионом.
Схематичное строение РНК- содержащего вируса со спиральным типом симметрии и дополнительной липопротеидной оболочкой приведено слева на рисунке 2, справа показан его увеличенный поперечный разрез.
Взаимодействие вируса с клеткой
Вирусы способны жить и размножаться только в клетках других организмов. Вне клеток организмов они не проявляют никаких признаков жизни. В связи с этим вирусы представляют собой либо внеклеточную покоящуюся форму ( варион ),
Взаимодействии вируса с клеткой последовательно проходят несколько стадий:
2. Вторая стадия состоит в проникновении целого вариона или его нуклеиновой кислоты внутрь клетки-хозяина.
4. В ходе четвертой стадии на основе вирусной нуклеиновой кислоты происходит синтез необходимых для вируса соединений.
6. В ходе шестой стадии из синтезированных ранее многочисленных копий нуклеиновой кислоты и белков формируются новые вирионы путем самосборки
Бактериофаги, образующие в зараженных клетках новое поколение фаговых частиц, что приводит к лизису(разрушению) бактериальной клетки, называются вирулентными фагами.
ДНК-содержащие вирусы несут в качестве генетического материала либо одно-, либо двухцепочечную ДНК, которая может быть как линейной, так и кольцевой. В ДНК закодирована информация о всех белках вируса. Вирусы классифицируют в зависимости от того, одно или двухцепочечная у них ДНК, и про- или эукариотической является клетка-хозяин. Вирусы заражающие бактерии называются бактериофагами.
Первая группа — вирусы с двуцепочечной ДНК:
— они получили название ретроидные вирусы.
— п редставителями этой группы вирусов являются вирус гепатита В и вирус мозаики цветной капусты.
1. Репликация ДНК-генома этих вирусов осуществляется при посредстве промежуточных молекул РНК:
2. Молекулы РНК образуются в результате транскрипции вирусных ДНК в клеточном ядре хозяйским ферментом ДНК-зависимой РНК-полимеразой.
3. Транскрибируется только одна из нитей вирусной ДНК.
4. Синтез ДНК на РНК-матрице происходит в результате реакции, катализируемой обратной транскриптазой; сначала синтезируется (-) нить ДНК,
5. а затем на вновь синтезированной (-) нити ДНК тот же фермент строит (+) нить.
Вторая группа — вирусы с двуцепочечной ДНК,
— с генома этих вирусов в зараженной клетке ДНК-зависимая РНК-полимераза транскрибирует молекулы мРНК (т.е. (+) РНК),
— мРНК (т.е. (+) РНК) принимает участие в синтезе вирусных белков,
— размножение вирусного генома осуществляет фермент ДНК-зависимая ДНК-полимераза: 
Третья группа — вирусы с одноцепочечной ДНК, либо с негативной, либо с позитивной полярностью.
— Попав в клетку, вирусный геном сначала превращается в двуцепочечную форму,

Транскрипция и репликация на последующих этапах происходит так же, как и для вирусов, с (±) ДНК-геномом.
— обычно встречаются у нитевидных вирусов.
— образуются путем самосборки асимметричных белковых субъединиц ( капсомеров ), объединяющихся в трубчатую структуру со спиральной симметрией ( например у Pf 1).
— Субъединицы в большинстве случаев гомогенны, так, что поверхность вириона состоит из множества копий одного и того же белка, хотя под наружним капсидом могут находиться и другие белки.
— ДНК в таких вирусах либо вытянута, либо может быть туго скручена в комплексе со специальными связывающими белками.
— свойственны большинству сферических ДНК-содержащих вирусов
— икосаэдр – это многогранник с двадцатью треугольными гранями, имеющий кубическую симметрию и приблизительно сферическую форму.
— Вершины треугольников соединяясь образуют двенадцать вершин икосаэдра;
— в местах соединения располагаются обычно пентамерные белковые структуры – пентоны ; там же могут находится участки, на которых формируются белковые нити, нередко ассоциированные с вершинами ( например у ф Х174).
— ДНК обычно плотно свернута внутри капсида ;
— иногда она связана с белками или полипептидами, способными стабилизировать ее структуру.
Сложные капсиды без оболочки
— типичны для бактериофагов:
— они состоят из частей с разными типами симметрии.
— У бактериофага Т2, например, ДНК находится в икосаэдрической головке, а для «узнавания» бактерии и введения в нее ДНК служат трубчатые и фибриллярные структуры (в узнавании участвует также лизоцим, расположенный на дистальном конце хвостового отростка).
Выделяют 5 морфологических типов бактериофагов:
Жизненный цикл бактериофага 5 типа:
Сложные капсиды с оболочкой
— есть только у вирусов эукариотических клеток.
— В них ДНК-белковые комплексы окружены одним или несколькими белковыми слоями и наружней мембраной, почти все белковые компоненты которой являются вирусными по своему происхождению, а липидные структуры – клеточными.
Инфицирование – процесс, посредством которого вирус внедряется в клетку-хозяина и «настраивает» ее метаболический аппарат на воспроизведение вирионов.
— зараженные вирусом клетки либо остаются живыми (тогда говорят, что вирус невирулентен ),
— либо подвергаются лизису, приводящему к высвобождению вирусных частиц.
— Неизменным итогом заражения клеток ДНК-содержащими бактериофагами является лизис.
— ДНК-содержащие вирусы животных вызывают лизис редко; однако клетки могут погибнуть из-за возникших при заражении хромосомных повреждений, вследствии иммунологической реакцииорганизма или просто в результате нарушения вирусом нормальных клеточных функций.
Размножение вируса – четко очерченный цикл, приводящий в конечном счете, после синтеза новых молекул вирусных белков и большого числа копий вирусной ДНК, к формированию зрелых вирусных частиц. У вирусов бактерий весь цикл может завершаться менее чем за час, тогда как у многих вирусов животных он занимает не один день.
Адсорбция вируса на клетке-хозяине – первый этап инфицирования. Она происходит на специфических рецепторных участках (белковых или липидных) клеточной поверхности, которые узнаются особыми выступающими частями вириона и к которым он прочно прикрепляется. У вирусов без оболочки такими частями могут быть белковые отростки (например, у аденовируса и бактериофага Т2), а у вирусов с оболочкой это, как правило белки, погруженные в вирусную мембрану. В процессе адсорбции осуществляются, в частности, такие белок-белковые взаимодействия, результатом которых является инициация стадии проникновения ДНК в клетку.
Проникновение вирусной ДНК в клетку-хозяина у разных вирусов происходит по-разному. ДНК многих бактериофагов, например, бактериофага Т2: белковый стержень сплющивается, подобно телескопической конструкции, и ДНК «впрыскивается» в бактерию. Из вирусов животных ДНК обычно переходит в клетку в результате как бы слияния наружнего слоя вириона с клеточной мембраной. В отличие от ДНК большинства бактериофагов ДНК вирусов животных всегда входят в клетку вместе с непосредственно прилегающими к ней белками; последующее освобождение ДНК от этих белков осуществляется с помощью ферментов.
ДНК-содержащие опухолеродные вирусы разделяются на следующие 5 классов.
1. Полиомавирусы – обезьяний вирус SV40, вирус полиомы мышей и вирусы человека ВК и JC.
2. Папилломавирусы – 16 вирусов папилломы человека и множество папилломовирусов животных.
3. Аденовирусы – 37 вирусов человека, множество аденовирусов животных (например, 24 вируса обезьян и 9 вирусов крупного рогатого скота).
4. Герповирусы – вирусы простого герпеса человека, цитомегаловирус человека, вирус Эпштейна– Барр и онкогенные вирусы приматов, лошадей, кур, кроликов, лягушек.
5. Вирусы, подобные вирусу гепатита В, – вирус гепатита В человека, гепатита североамериканского сурка, гепатита земляных белок и гепатита уток.