Жидкий кислород
Жидкий кислород – это агрегатное состояние кислорода, в котором он представляет собой бледно-синюю жидкость. Он относится к категории веществ, которые одними из первых стали использоваться в разных областях промышленности. Жидкий О2 используется с двумя целями: для усиления процессов горения и для окисления химических процессов. Именно необходимость решения этих задач стала причиной популярности воздухоразделительного оборудования.
Физические свойства жидкого кислорода
В жидком состоянии кислород имеет бледно-голубой оттенок. При переливании из одной емкости в другую жидкий кислород выделяет водяные пары, поглощая тепло из окружающего воздуха. При этом температура воздуха резко снижается, что приводит к образованию тумана.
Этот вид кислорода способен закипать при температуре 183°С. Если в это время поместить его в среду, в которой температура воздуха составляет около 30-40°С, то кипение лишь усилится. При комнатной температуре жидкость быстро испаряется.
Для того чтобы снизить скорость испарения кислорода жидкого, его помещают в специальные баллоны. Баллон для хранения О2 представляет собой двухслойный сосуд. Внутренняя стенка баллона покрыта слоем серебра, а между ней и внешней стенкой полностью выкачан весь воздух. Слой серебра необходим для того, чтобы отражать тепло. В таком баллоне кислород может храниться на протяжении нескольких суток.
К другим физическим свойствам жидкого кислорода можно отнести следующие:
Как получают жидкий кислород?
После этого проводят ректификацию, то есть отделение азота от кислорода. Этого добиваются путем многократного нагревания жидкости, в ходе которого первым делом испаряется азот, а оставшаяся жидкость обогащается О2.
В каких областях используют жидкий кислород?
В настоящее время жидкому кислороду находится применение в разных областях промышленности:
Жидкий О2 служит в качестве сырья для получения других химических соединений, вроде двуокиси титана или окиси этилена. С его помощью также можно повысить производительность большинства окислительных процессов.
В стекольной промышленности кислород применяется для интенсификации процессов горения, необходимых для поддержания работы стеклоплавильных печей. Помимо этого, он помогает снизить выбросы оксида азота и увеличить эффективность стекольного производства.
С этой же целью жидкий О2 используется в металлургии, где он обогащает воздух и повышает эффективность процесса горения.
С жидким кислородом связано ускорение процессов роста клеток, поэтому в фармацевтике его добавляют в ферментеры и биореакторы.
В целлюлозно-бумажной отрасли промышленности с помощью этого вида кислорода осуществляется окислительное экстрагирование, обработка сточных вод и делигнификация (процесс получения целлюлозы).
Помимо этого, кислородом жидким пользуются в автомобилестроении и машиностроении, где он применяется в качестве вспомогательного газа во время лазерной резки. Его также добавляют в состав защитных газовых смесей.
Техника безопасности при работе с жидким кислородом
При работе с жидким кислородом нет угрозы отравления, но все же некоторые требования безопасности необходимо строго соблюдать:
Преимущества сотрудничества с НПК «Грасис»
Научно-производственная компания «Грасис» осуществляет поставки оборудования, которое позволит вам самостоятельно получать газообразный кислород из атмосферного воздуха.
Наша компания более 10 лет занимается разработкой и производством газо- и воздухоразделительного оборудования, а также инжинирингом, проектированием и выполнением комплексных работ «под ключ». Мы поможем вам решить любые задачи, связанные с газо- и воздухоразделением, утилизацией попутного нефтяного газа и подготовкой природного газа.
В процессе производства оборудования мы используем нанотехнологии и высококачественные комплектующие, благодаря которым улучшаются технико-эксплуатационные свойства продукции. Свяжитесь с представителями компании «Грасис», чтобы получить развернутую информацию о заинтересовавшей вас установке!
Вакуум. Жидкий воздух
В Лабораториях вакуум («пустота»), при котором столкновения молекул между собой уже сравнительно редки, соответствует давлению примерно в 0,13 Па. Даже с помощью самых совершенных методов современной техники не удается достигнуть вакуума, при котором в кубическом сантиметре газа оставалось бы менее 1000 частиц.
Масса литра воздуха при нормальных условиях (1,293 г), а его средняя молярная масса воздуха равна 22,4·1,293 = 29 г/моль.
При достаточном охлаждении воздух переходит в жидкое состояние. Жидкий воздух можно довольно долго сохранять в сосудах с двойными стенками, из пространства между которыми для уменьшения теплопередачи выкачан воздух. Подобные сосуды используются, например, в термосах.
Трудно сжижаемые газы научились сжижать используя их свойства охлаждаться при расширении, если газ многократно сжимать и выпускать его в большой сосуд, то он будет охлаждаться и когда его температура достигнет критической он начнет сжижаться.
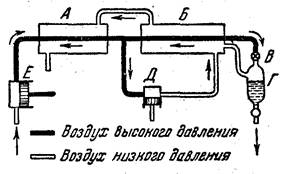
Далее воздух, омыв два теплообменника и тем самым охладив второй поток, идущий навстречу, выходит наружу и собирается в термосе. –
В 1938 г. П. Л. Капицей был разработан метод получения жидкого воздуха при низком давлении — всего 5-6 атм. Основной особенностью этого метода является замена поршневых механизмов компрессора и детандера турбинными.
Применение
Сжатый воздух хранят в стальных баллонах, рассчитанных на давление 150 атм. По действующим техническим условиям баллоны эти должны иметь черную окраску с белой надписью: «Воздух сжатый».
Химические реакции при температуре жидкого воздуха вообще очень сильно замедляются. Однако благодаря большой концентрации в нём кислорода (концентрацией называется количество вещества в единице объёма или массы), смешанные с жидким воздухом горючие вещества горят гораздо энергичнее, чем в обычных условиях. Например, смоченная жидким воздухом вата сгорает со вспышкой подобно бездымному пороху.
Кислород – рождающий кислоты
Содержание
Кислород при нормальных условиях (температуре и давлении) представляет собой прозрачный газ без запаха, вкуса и цвета. Не относится к горючим газам, но способен активно поддерживать горение.
По химической активности среди неметаллов он занимает второе место после фтора.
Все элементы, кроме благородных металлов (платина, золото, серебро, родий, палладий и др.) и инертных газов (гелий, аргон, ксенон, криптон и неон), вступают в реакцию окисления и образовывают оксиды. Процесс окисления элементов, как правило, носит экзотермический (с выделением теплоты) характер. Также необходимо учитывать тот факт, что при повышении температуры, давления или использовании катализаторов – скорость реакции окисления резко возрастает.
История открытия кислорода
Открытие кислорода приписывают Джозефу Пристли (Joseph Priestley). У него была лаборатория, оборудованная приборами для собирания газов. Он испытывал его физиологическое действие на себе и на мышах. Пристли установил, что после вдыхания газа некоторое время ощущается приятная легкость. Мыши в герметически закрытой банке с воздухом задыхаются быстрей, чем в банке с O2. Поскольку Пристли был приверженцем флогистонной теории он так и не узнал, что оказалось у него в руках. Он только описал этот газ, даже не догадываясь, что он описал. А вот лавры открытия кислорода принадлежат Антуан Лоран Лавуазье (Antoine Laurent de Lavoisier), который и дал ему имя.
Лавуазье, поставил свой знаменитый опыт, продолжавшийся 12 дней. Он нагревал ртуть в реторте. При кипении образовывалась ее красная окись. Когда реторту охладили, оказалось, что воздуха в ней убыло почти на 1/6 его объема, а остаток ртути весил меньше, чем перед нагревом. Но когда разложили окись ртути сильным прокаливанием, все вернулось: и недостача ртути, и «исчезнувший» кислород.
Впоследствии Лавуазье установил, что этот газ входит в состав азотной, серной, фосфорной кислот. Он ошибочно полагал, что O2 обязательно входит в состав кислот, и поэтому назвал его «оксигениум», что значит «рождающий кислоты». Теперь хорошо известны кислоты, лишенные «оксигениума» (например: соляная, сероводородная, синильная и др.).
Способы получения кислорода
В основном кислород получают тремя способами:
Из атмосферного воздуха его получают методом глубокого охлаждения, как побочный продукт при получении азота.
Также O2 добывают путем пропускания электрического тока через воду (электролиз воды) с попутным получением водорода.
Химические способ получения малопроизводителен, а, следовательно, и неэкономичен, он не нашел широкого применения и используются в лабораторной практике.
Наверно многие помнят химический опыт, когда в колбе нагревают марганцовку (перманганат калия KMnO4), а потом выделяющийся в процессе нагрева газ собирают в другую колбу?
Применение кислорода
Помимо того, что все живые существам в природе, за исключением немногих микроорганизмов, при дыхании потребляют кислород, он широко применяется во многих отраслях промышленности: металлургической, химической, машиностроении, авиации, ракетостроении и даже в медицине.
В химической промышленности его применяет:
В металлургии его используют:
В медицинских целях больным, у которых нарушена нормальная деятельность органов дыхания или кровообращения, искусственно увеличивают содержание O2 в воздухе или дают дышать непродолжительное время чистым O2. Медицинский кислород, выпускаемый ГОСТ 5583, особенно тщательно очищают от всех примесей.
Применение кислорода в сварке
Сам по себе O2 является негорючим газом, но из-за свойства активно поддерживать горение и увеличения интенсивности (интенсификации) горения газов и жидкого топлива его используют в ракетных энергетических установках и во всех процессах газопламенной обработки. В таких процессах газопламенной обработки, как газовая сварка, поверхностная закалка высокая температура пламени достигается путем сжигания горючих газов в O2, а при газовой резке благодаря ему происходит окисление и сгорание разрезаемого металла.
При полуавтоматической сварке (MIG/MAG) кислород O2 используют как компонент защитных газовых смесей с аргоном (Ar) или углекислым газом (CO2).
Кислород добавляют в аргон при полуавтоматической сварке легированных сталей для обеспечения устойчивости горения дуги и струйного переноса расплавленного металла в сварочную ванну. Дело в том, что как поверхностно активный элемент он уменьшает поверхностное натяжение жидкого металла, способствуя образованию на конце электрода более мелких капель.
При сварке низколегированных и низкоуглеродистых сталей полуавтоматом O2 добавляют в углекислый газ для обеспечения глубокого проплавления и хорошего формирования сварного шва, а также для уменьшения разбрызгивания.
Чаще всего кислород используют в газообразном виде, а в виде жидкости используют только при его хранении и транспортировке от завода-изготовителя до потребителей.
Вредность и опасность кислорода
За внешней безобидностью скрывается очень опасный газ, но об этом на нашем сайте опубликована статья про маслоопасность и взрывоопасность кислорода и мы не будем здесь дублировать информацию.
Хранение и транспортировка кислорода
Кислород газообразный технический и медицинский выпускают по ГОСТ 5583.
Хранят и транспортируют его в стальных баллонах ГОСТ 949 под давлением 15 МПа. Кислородные баллоны окрашены в синий цвет с надписью черными буквами «КИСЛОРОД».

Жидкий кислород выпускается по ГОСТ 6331. O2 находится в жидком состоянии только при получении, хранении и транспортировке. Для газовой сварки или газовой резки его необходимо снова превратить в газообразное состояние.
Характеристики кислорода
Характеристики O2 представлены в таблицах ниже:
Коэффициент перевода объема и массы O2 при Т=15°С и Р=0,1 МПа
| Масса, кг | Объем | |
|---|---|---|
| Газ, м 3 | Жидкость, л | |
| 1,337 | 1 | 1,172 |
| 1,141 | 0,853 | 1 |
| 1 | 0,748 | 0,876 |
Коэффициенты перевода объема и массы O2 при Т=0°С и Р=0,1 МПа
| Масса, кг | Объем | |
|---|---|---|
| Газ, м 3 | Жидкость, л | |
| 1,429 | 1 | 1,252 |
| 1,141 | 0,799 | 1 |
| 1 | 0,700 | 0,876 |
Кислород в баллоне
| Наименование | Объем баллона, л | Масса газа в баллоне, кг | Объем газа (м 3 ) при Т=15°С, Р=0,1 МПа |
|---|---|---|---|
| O2 | 40 | 8,42 | 6,3 |
Благодаря этой таблице теперь можно легко дать ответы на вопросы, которые очень часто задают сварщики:
Криогенная технология
Криогенная технология-разделения воздуха с помощью криогенных температур на основные газовые компоненты
ИА Neftegaz.RU. Технология разделения воздуха с помощью криогенных температур на основные газовые компоненты известна очень давно.
Повторяя подобный процесс многократно на ректификационных тарелках воздухоразделительных колонн, получают жидкие кислород, азот и аргон нужной чистоты.
При относительно высокой стоимости криогенные блоки очень надежны, просты в эксплуатации, обладают высокими техническими характеристиками и позволяют получать газы высокой чистоты в очень больших объемах, например, газообразный азот сверхвысокой чистоты (до 1 ppb), который не может быть получен в адсорбционных и мембранных системах.
В то же время криогенные блоки являются экономически эффективными при долгосрочной эксплуатации за счет низкого удельного энергопотребления и низких эксплуатационных затрат.
Широкое применение нержавеющей стали, особенно для трубопроводов и клапанов, позволяет использовать простые и надежные сварные соединения, а также обеспечивает противокоррозионную стойкость. Кроме этого, само по себе сварные соединения нержавеющих трубопроводов как внутри холодного блока, так и в не его, обеспечивают долговечную плотность и не допускают протечек.
Основными техническими преимуществами криогенного способа являются гарантированная высокая чистота продукта при неизменном расходе, а также низкое удельное энергопотребление в течение всего срока эксплуатации.
Минимизация вращающихся и движущихся механизмов обеспечивает долгий ресурс работы криогенных установок.
При соблюдении проектных условий эксплуатации блока комплексной очистки (БКО) не требуется замена адсорбентов в течение всего срока службы установки.
Процесс генерации жидкого азота
Расплескалась синева: первое получение жидкого кислорода
История сжижения кислорода под конец превратилась в соперничество. Но кто возьмет верх: инженер, всю жизнь проработавший на металлургическом заводе, или специалист по физике низких температур в Женевском университете? Лед или пламень, теория или практика, Эйфелева башня или Суэцкий канал одержат победу? Об этом читайте в рубрике «История науки».
Жидкий кислород, налитый в химический стакан, а не в сосуд Дьюара, удивит вас красивым голубым цветом. Этот цвет в прямом смысле небесной лазури – ведь этот газ составляет 21% воздуха. Но первым человеком, получившим его, был вполне приземленный инженер и владелец завода, не привыкший мечтами парить в небесах.
Луи-Поль Кайете родился в Бургундии, в живописной коммуне Шатийон-сюр-Сен. Школьное образование он начал получать там же, продолжил в Париже, а затем поступил в Горный институт вместе с братом Камилем. Там, в химической лаборатории, Луи познакомился со множеством будущих знаменитостей французского научного мира. Окончив институт, братья совершили несколько поездок в Англию, Австрию и Германию, тоже с образовательными целями: там они увидели самые современные доменные печи и прокатные станы, знакомились с самым передовым оборудованием. Но заниматься всю жизнь одной наукой не получилось: отец и дед молодых людей состарились, и дома, в Бургундии, нужна была помощь в работе на металлургическом заводе.
Myrabella / Wikimedia Commons / CC BY-SA 4.0
Но и там Луи не прекратил научных изысканий. Сначала он занялся исследованием процессов горения древесины в печах, показав, что этот процесс приводит к выделению углекислого газа. Была у него слабость и к ботанике: свободное время он уделял своей небольшой оранжерее, где выращивал редкие орхидеи и бегонии, в результате даже опубликовав несколько статей по физиологии растений.
После того, как его брат умер от туберкулеза, а отец и дед – от старости в 1860-х годах, Луи-Поль Кайете остался единственным владельцем завода. Но это только подстегнуло его исследования. Он занялся изучением выплавки чугуна и участием в ней разных газов. Для понимания процессов в плавильных печах ученому нужно было измерить температуру и давление. Однако существующие приборы не работали в большом диапазоне температур и давлений, и Кайете посвятил полтора десятка лет своей жизни усовершенствованию манометров и термометров, а также изучению зависимости объема газов от давления и температуры, описанной законом Бойля-Мариотта.
В 1870 году на первом этаже оранжереи он построил себе лабораторию, оборудованную мощным гидравлическим насосом, чтобы изучать химические вещества при высоком давлении и температуре. Итогом его работы стал манометр, способный измерить давление до 400 атмосфер. В 1891 году он даже установил свой манометр на Эйфелевой башне.
Тогда Кайете и заинтересовался сжатием газов и решил получить их в жидком виде. В ноябре 1877 года он проводил опыты по сжижению ацетилена и диоксида азота, сначала сжимая их под большим давлением, а потом охлаждая их другими сжиженными газами. Кайете использовал эффект Джоуля-Томпсона, зная, что если замораживать газ при сильном давлении, а затем позволить ему резко расшириться, температура газа упадет еще больше.
Аппарат Кайете для сжижения газов
Popular Science Monthly Volume 12/Wikipedia
Этим ученым был физик из Женевы Рауль Пикте. Он был третьим из пяти отпрысков старинного швейцарского рода. Получив образование в Париже, Пикте к тому времени уже семь лет возглавлял кафедру в Женевском университете, занимаясь физикой низких температур. До этого он успел поработать в Египте во время строительства Суэцкого канала, реорганизовав образовательные учреждения в этой стране.
В отличие от своего французского соперника, он сам не занимался инженерным делом и прикладной наукой, хотя и верил в важность образования в обеих областях. Несмотря на это, у него, несомненно, был изобретательский талант: уже в 23 года он сконструировал холодильную установку, которая производила 15 килограммов льда в час. Идея Пикте о том, что в холодильных установках должна быть смесь двух веществ, была развита в дальнейшем и использована на практике при создании холодильников и криогенного оборудования.
Лаборатория Рауля Пикте
Ch. Baude/L’Illustration, du 19 janvier 1878, vol. LXXI, p. 45, et L’Exposition de Paris, journal hebdomadaire, du 28 mai 1878, N°4, p. 28
Разрешить спор помог Анри Девиль – французский физикохимик, разработавший промышленный способ производства алюминия и преподаватель Сорбонны. Также он ввел теорию диссоциации – разложения вещества при нагревании – и изготовил эталоны метра и килограмма из сплава платины и иридия для Международной комиссии мер и весов в 1872 году. К такому влиятельному ученому нельзя было не прислушаться. Так на чьей же он был стороне? Оказалось, Девиль, друг Кайете, получил от него письмо, датированное 2 декабря, с точным и полным описанием опыта по получению кислорода. При возникновении разногласий Анри Девиль тут же доставил доказательства секретарю Академии наук. Так Луи-Поль Кайете и стал известен как первый ученый, получивший кислород в жидком виде.