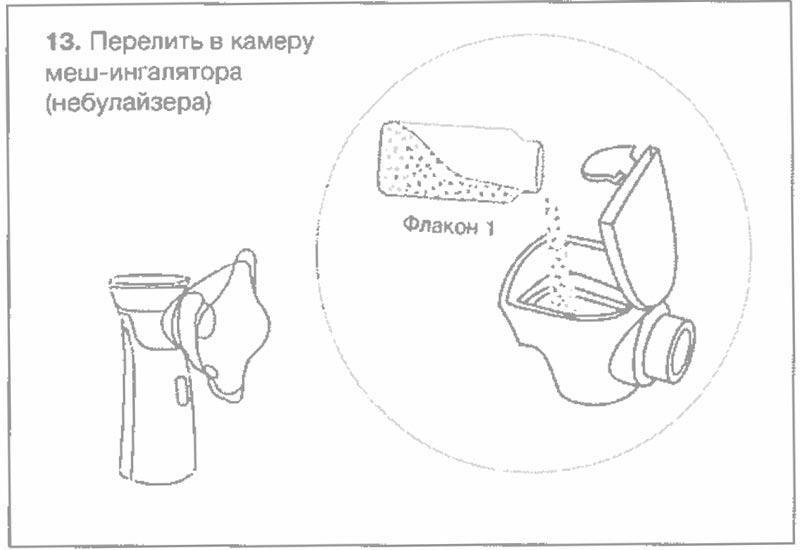
Физиологический раствор с фосфатным буфером
| Соль | Концентрация (ммоль / л) | Концентрация (г / л) |
|---|---|---|
| NaCl | 137 | 8.0 |
| KCl | 2,7 | 0,2 |
| Na 2 HPO 4 | 10 | 1,42 |
| КН 2 ПО 4 | 1,8 | 0,24 |
| реагент | МВт | масса (г) 10 × | [M] 10 × | масса (г) 5 × | [M] 5 × | масса (г) 1 × | [M] 1 × |
|---|---|---|---|---|---|---|---|
| Na 2 HPO 4 | 141,95897 | 14.1960 | 0,1000 | 7,0980 | 0,0500 | 1,41960 | 0,0100 |
| КН 2 ПО 4 | 136.08569 | 2.4496 | 0,0180 | 1,2248 | 0,0090 | 0,24496 | 0,0018 |
| NaCl | 58,44300 | 80,0669 | 1,3700 | 40,0335 | 0,6850 | 8,00669 | 0,1370 |
| KCl | 74,55150 | 2,0129 | 0,0270 | 1,0064 | 0,0135 | 0.20129 | 0,0027 |
| pH = 7,4 |
7,4. При приготовлении буферных растворов рекомендуется всегда измерять pH напрямую с помощью pH-метра. При необходимости pH можно отрегулировать с помощью соляной кислоты или гидроксида натрия.
PBS также можно получить с использованием коммерческих таблеток или пакетов с буфером PBS. [4]
Данный лекарственный препарат зарегистрирован по процедуре регистрации препаратов, предназначенных для применения в условиях угрозы возникновения, возникновения и ликвидации чрезвычайных ситуаций. Инструкция подготовлена на основании ограниченного объема клинических данных по применению препарата и будет дополняться по мере поступления новых данных. Применение препарата возможно только в условиях стационарной медицинской помощи.
Регистрационный номер:
Торговое наименование
Международное непатентованное или группировочное наименование
Синтетическая малая интерферирующая рибонуклеиновая кислота (миРНК) [двуцепочечная]
Лекарственная форма
Лиофилизат для приготовления раствора для ингаляций
Состав
1 упаковка содержит:
Действующее вещество:
Синтетическая малая интерферирующая РНК siRk-12 (миРНК) – 0,088 мг.
Вспомогательное вещество:
Пептид КК-46 – 1,762 мг.
Растворитель:
Фосфатно-солевой буферный раствор – 2,5 мл.
Лекарственный препарат выпускается в комплекте с растворителем – фосфатно-солевой буферный раствор.
Состав растворителя (на 1 мл): натрия хлорид – 8 мг, натрий фосфорнокислый 2-замещенный 12-водный – 3,58 мг, калий фосфорнокислый однозамещенный – 0,24 мг, калий хлористый – 0,2 мг, вода для инъекций – до 1 мл.
Описание
Флакон-1: действующее вещество – синтетическая малая интерферирующая-РНК siRk-12 (миРНК) – белый аморфный порошок или пленка на флаконе.
Восстановленный раствор представляет собой прозрачный, бесцветный раствор.
Флакон-2: растворитель для лиофилизата – фосфатно-солевой буферный раствор – прозрачный, бесцветный раствор
Флакон-3: вспомогательное вещество пептид КК-46 – белый или желтоватый аморфный порошок или пористая масса в виде таблетки.
Восстановленный раствор представляет собой прозрачный, бесцветный раствор.
Флакон-4: растворитель для лиофилизата – фосфатно-солевой буферный раствор – прозрачный, бесцветный раствор.
Фармакотерапевтическая группа
Противовирусные средства системного действия; противовирусные средства прямого действия; другие противовирусные средства.
Код АТХ:
Фармакологические свойства
Фармакодинамика
Действующим веществом является синтетическая малая интерферирующая РНК siRk-12 (миРНК) – короткие двуцепочечные молекулы, обладающие сродством к геному вируса. Молекулы миРНК имеют размер 22 пары нуклеотидов и несут следующие модификации: LNA-модификацию в 5-ти позициях и DNA-модификацию в 2-х позициях. Указанные модификации увеличивают резистентность молекулы миРНК к ферментам деградации организма (РНКазам) более чем в 3 раза, что в итоге позволяет оказывать более длительный биологический эффект.
Молекулы миРНК данного препарата направлены против консервативного участка генома SARS-CoV-2, кодирующего жизненно важный фермер репликации вируса – РНК-зависимую РНК-полимеразу (RdRp). Данный участок генома консервативен не только у SARS-CoV-2, но и у близкородственных видов семейства Coronaviridae (например, SARS-CoV), вызывающих атипичную пневмонию.
Свой биологический антивирусный эффект молекулы миРНК проявляют в цитоплазме инфицированной клетки, где вирус лишается своего капсида, происходит репликация его генома, транскрипция мРНК и трансляция вирусных белков с последующим образованием новых вирионов, способных инфицировать новые незаряженные клетки. В момент репликации в цитоплазме клетки геном SARS-CoV-2 наиболее «уязвим» для действия молекул миРНК. Молекулы миРНК, после проникновения в цитоплазму клетки к месту действия, встраиваются в белковый комплекс RISC (РНК-индуцированный сайленсинговый комплекс), который предсуществует внутри клетки. Блок AGO этого комплекса за счет хеликазной активности расплетает двуцепочечную молекулу миРНК, после чего в комплексе RISC остается одна антисмысловая цепь, в то время как смысловая антипараллельная цепь деградирует. Далее за счет антисмысловой цепи комплекс RISC по принципу комплементарности «нацеливается» на геном SARS-CoV-2 и его мРНК-транскрипты и за счет экзонуклезной активности катализирует их разрезание, что в итоге приводит к уменьшению репликации вируса и числа копий его генома в клетке.
Молекулы миРНК самопроизвольно не способны проникать к месту своего действия – в цитоплазму клеток. Для этого в составе препарата используется пептид, выполняющий функцию носителя для миРНК. За счет своей разветвленной структуры и высокой плотности положительного заряда пептид в водном растворе электростатически взаимодействует с отрицательно заряженными молекулами миРНК, формируя наноструктуры. Данные наноструктуры по механизму эндоцитоза приникают в цитоплазму клетки – к месту репликации вируса. Исследования в культуре клеток показали, что препарат в концентрации 84 мкг/мл в течение 2 суток уменьшал число копий генома SARS-CoV-2 до 10 000 раз. Учитывая, что целевой участок генома SARS-CoV-2 отличается от генома человека, то молекулы миРНК препарата не оказывают «ложного нацеливания» на мРНК генов человека.
В экспериментах на сирийских хомячках, зараженных SARS-CoV-2 продемонстрировано, что ежедневные ингаляции препаратом в дозе 0,35 мг/кг/сут снижают вирусную нагрузку в легких в 50 раз на вторые сутки после инфекции и в 25 раз на 6-е сутки после инфекции. Такое снижение репликации вируса приводит к уменьшению патологических нарушений ткани легких.
Фармакокинетика
Были проведены исследования фармакокинетики препарата МИР 19 ® на крысах и кроликах при внутривенном и ингаляционном введениях. Для проведения данных исследований в состав компонентов препарата (миРНК siRk-12 и пептид КК-16) были введены флуоресцентные метки. Была доказана линейность зависимости Сmax, AU0-t и AUC0-∞ от введенной дозы по каждому компоненту в диапазоне от 0,35 мг/кг до 3,5 мг/кг на крысах при ингаляционном введении.
В результате исследования было показано, что при ингаляционном введении период полувыведения из системного кровотока животных для миРНК в среднем составил 21,53 мин, а для пептида – 23,22 мин. Из этого следует, что полное выведение препарата можно ожидать примерно через 2 часа. Если дозирование препарату при терапевтическом использовании будет с интервалом более 2 часов, то можно утверждать, что накопление и кумуляции препарата в организме наблюдаться не будут.
При изучении распределения препарата по органам крыс было показано, что препарат не обнаруживается в органах иммунной системы (тимусе и селезенке), репродуктивной системы (семенники) и системе ЦНС (головной мозг). Самое большое количество препарата при ингаляционном введении было обнаружено в легких, как месте введения (время достижения максимальной концентрации 3 минуты) а также в печени и почках, как органах выведения (время достижения максимальной концентрации 15 минут).
Основным путем метаболизма компонентов препарата МИР 19 ® является немикросомальный гидролиз. При ингаляционном введении неактивные метаболиты препарата всасываются в системный кровоток.
Исследования фармакокинетики препарата в клинических исследованиях с участием добровольцев не проводилось в связи с отсутствием методов детектирования действующего вещества в биологических объектах без использования меток.
Показания к применению
Лечение новой коронавирусной инфекции (COVID-19) у взрослых в возрасте от 18 до 65 лет.
Противопоказания
Повышенная чувствительность к действующему веществу и любому другому компоненту препарата.
Пациенты с тяжелым течением коронавирусной инфекции (COVID-19).
Возраст младше 18 и старше 65 лет.
Беременность и период грудного вскармливания.
Пациенты, которые на постоянной основе применяют системные глюкокортикостероиды.
С осторожностью
Применять препарат МИР 19 ® с осторожностью при хронических заболеваниях печени и почек, эндокринных заболеваниях (выраженных нарушениях функции щитовидной железы и сахарном диабете в стадии декомпенсации), тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваниях ЦНС, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах, первичных и вторичных иммунодефицитах, аутоиммунных заболеваниях, у пациентов с аллергическими реакциями.
Вследствие недостатка информации прием препарата может представлять риск для следующих групп пациентов:
Принятие решения о приеме препарата должно основываться на оценке соотношения пользы и риска в каждой конкретной ситуации.
Применение при беременности и в период грудного вскармливания
Препарат противопоказан при беременности. При необходимости применения препарата в период лактации следует прекратить грудное вскармливание.
Способ применения и дозы
Препарат применяется ингаляционно с помощью меш-ингалятора (небулайзера). Препарат назначается в условиях стационара.
Препарат принимать 2 раза в день. Перерыв между ингаляциями должен составлять 7-8 часов. Разовая доза составляет 1,85 мг. Суточная – 3,7 мг/сут. Курс лечения составляет 14 дней (28 ингаляций). При необходимости, перед проведением процедуры ингаляции следует устранить заложенность носа путем промывки солевым раствором или путем закапывания сосудосуживающих препаратов.
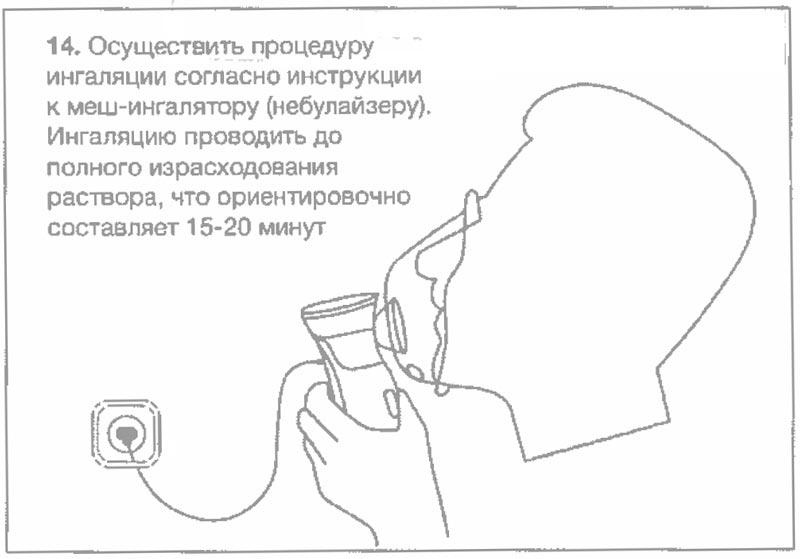
Во время ингаляции пациент должен находиться в положении сидя, не разговаривать и держать меш-ингалятор (небулайзер) вертикально, а дыхание осуществлять через маску, которая должна прилегать ко рту и к носу одновременно.
Приготовление раствора для ингаляций
После растворения молекул миРНК в растворителе образуется прозрачный раствор. После растворения пептида в растворителе образуется прозрачный раствор. После смешивания раствора миРНК и раствора пептида образуется опалесцирующий раствор от бесцветного до светло-желтого цвета.
Важно: перед медицинским применением необходимо ознакомиться с правилами эксплуатации используемого меш-ингалятора (небулайзера).
Использование небулайзеров других типов кроме меш-ингалятора (небулайзера) не допускается!
Схематический рисунок по процедуре приготовления препарата
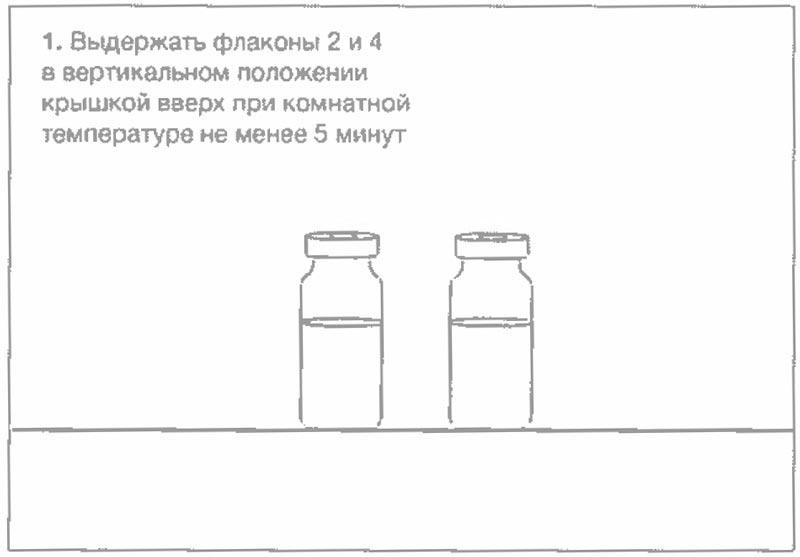
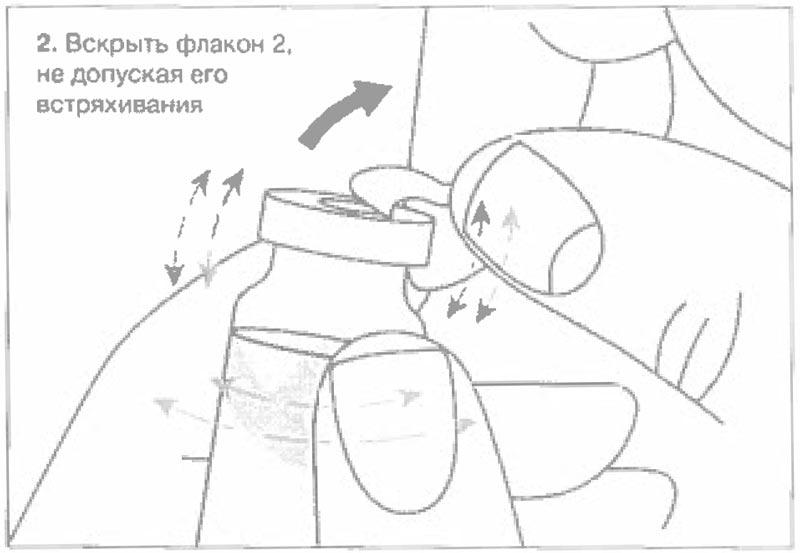
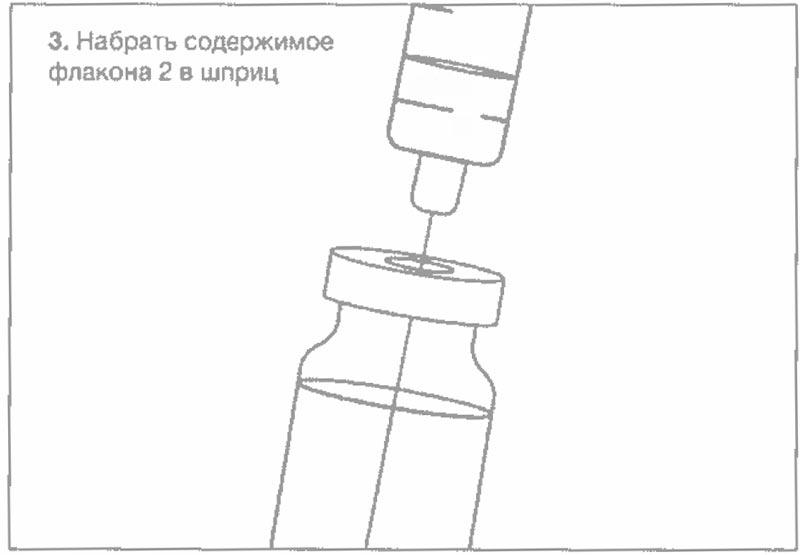
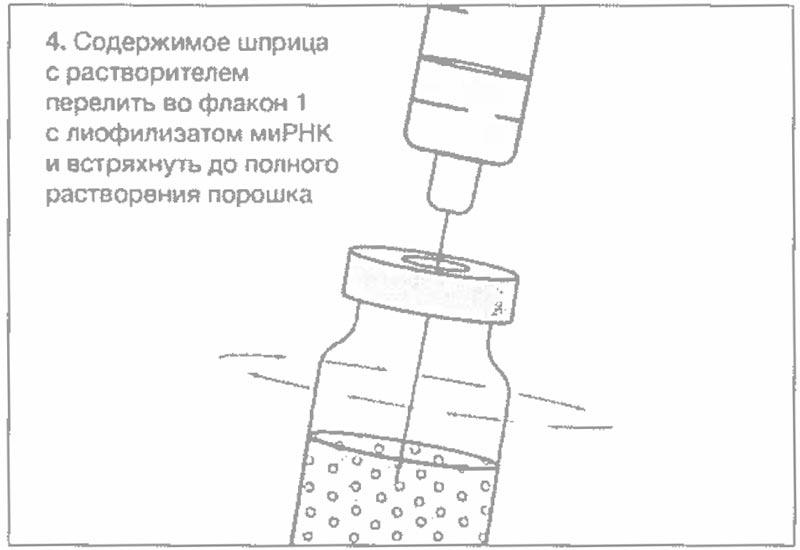
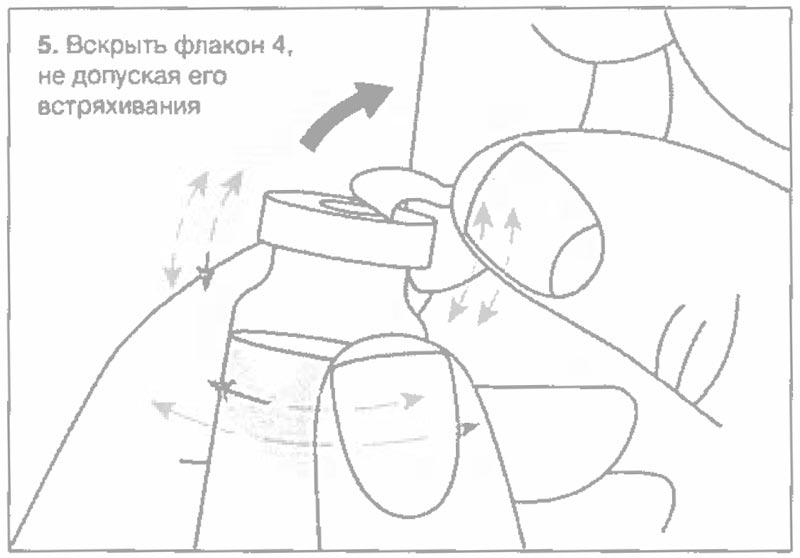
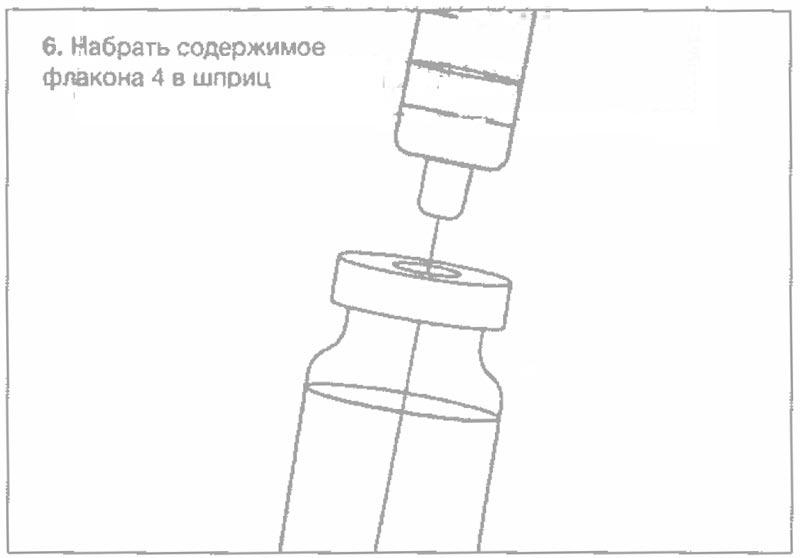
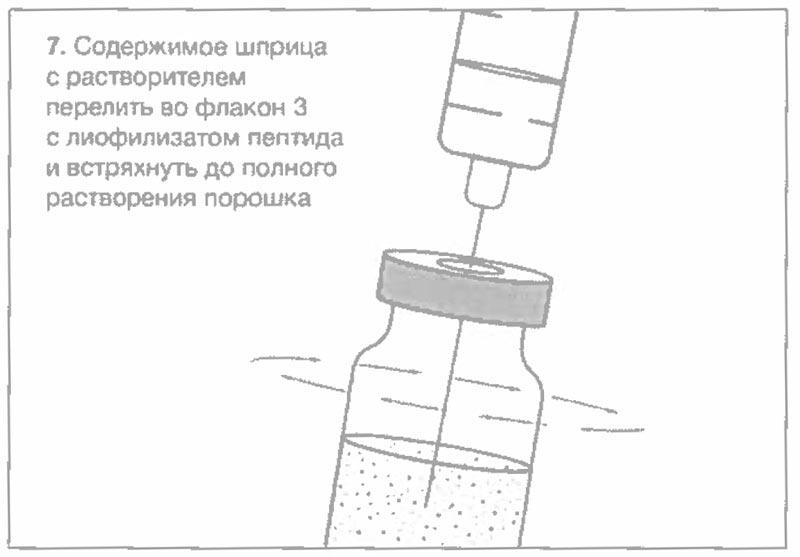
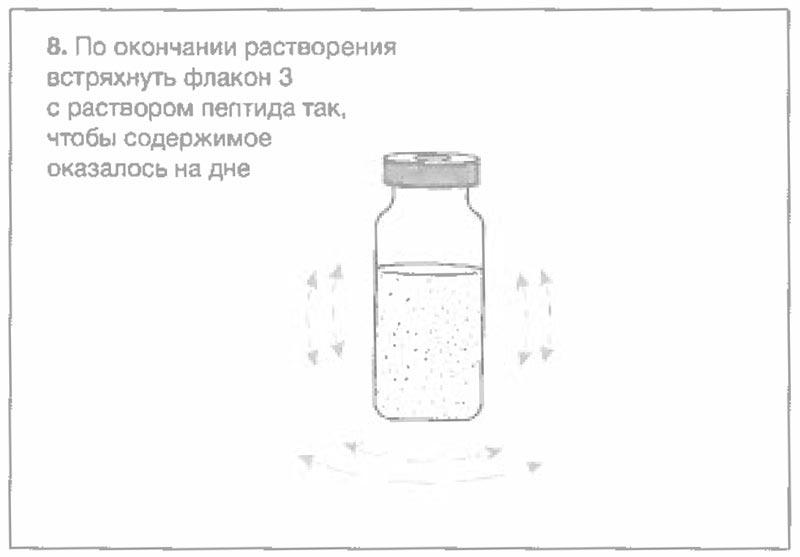
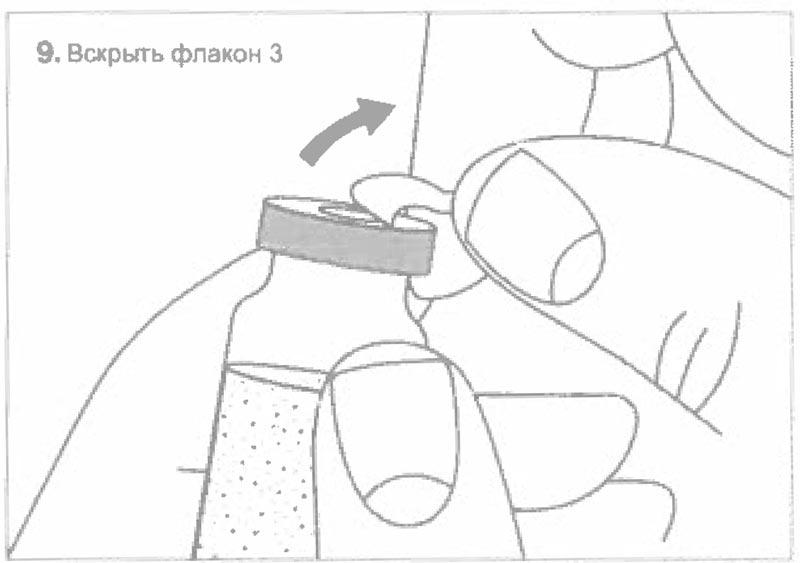
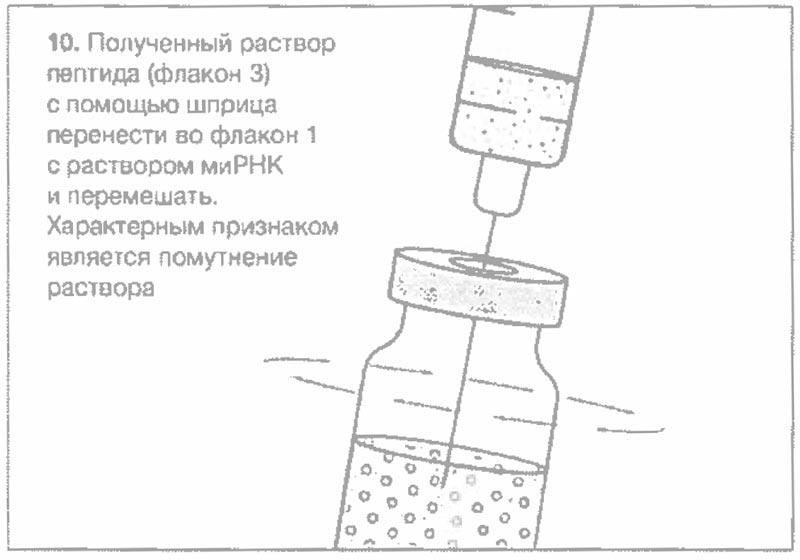

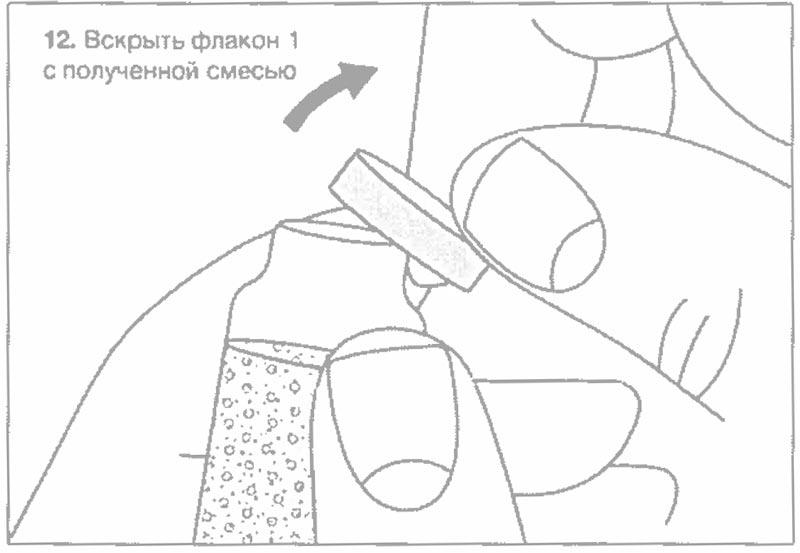
Рекомендованные характеристики меш-ингалятора (небулайзера)
Препарат применяется ингаляционно с помощью меш-ингалятора (небулайзера) со следующими характеристиками:
| Минимальный размер частиц | 3 мкм |
| Максимальный размер частиц | 5 мкм |
| Макс. скорость распыления | 0.2 мл/мин |
| Объем емкости для лекарств | не менее 7 мл |
Побочное действие
Частота развития побочных реакций представлена в соответствии с классификацией ВОЗ НЛР на основании результатов проведенных клинических исследований.
Частота встречаемости определяется на основании следующих критериев: очень часто (≥1/10), часто (≥1/100 и ® не зарегистрировано.
Взаимодействие с другими лекарственными средствами.
Нельзя добавлять никакие другие лекарственные средства в меш-ингалятор (небулайзер) для совместного применения с препаратом МИР 19 ® во избежание фармацевтической несовместимости.
Особые указания
Применение препарата возможно только в условиях стационарной медицинской помощи. При развитии побочного действия необходимо сообщать об этом в установленном порядке для осуществления мероприятий по фармаконадзору.
Влияние на способность управлять транспортными средствами, механизмами
Следует соблюдать осторожность, так как данных по влиянию препарата на способность управлять транспортными средствами и механизмами нет.
Форма выпуска
Лиофилизат для приготовления раствора для ингаляций, 0,088 мг.
Флакон-1: по 0,088 мг миРНК siRk-12 во флакон из прозрачного стекла.
Флакон-3: по 1,762 мг пептида КК-46 во флакон из прозрачного стекла.
Флакон-2 и флакон-4: по 2,5 мл фосфатно-солевого буферного раствора во флаконы из прозрачного стекла.
На каждый флакон наклеивают этикетку самоклеящуюся.
По 4 флакона (флакон-1 с миРНК siRk-12, флакон-2 с фосфатно-солевым буферным раствором, флакон-3 с пептидом КК-46, флакон-4 с фосфатно-солевым буферным раствором) в контурной ячейковой упаковке из картона упаковочного.
По 1 контурной ячейковой упаковке в пачку из картона для потребительской тары, вместе с инструкцией по применению.
Условия хранения
Хранить при температуре от 2 до 8 °С. Не замораживать.
Хранить в недоступном для детей месте.
Условия транспортирования
При температуре от 2 до 8 °С. Не замораживать.
Срок годности
1 год.
Не применять по истечении срока годности.
Условия отпуска
Отпуск только для лечебно-профилактических учреждений.
Владелец регистрационного удостоверения
Федеральное государственное бюджетное учреждение «Государственный научный центр «Институт иммунологии» Федерального медико-биологического агентства (ФГБУ «ГНЦ Институт иммунологии» ФМБА России).
Россия, 115522, г. Москва, Каширское ш., д. 24
Производитель
Федеральное государственное унитарное предприятие «Санкт-Петербургский научно-исследовательский институт вакцин и сывороток и предприятие по производству бактерийных препаратов» Федерального медико-биологического агентства (ФГУП СПбНИИВС ФМБА России).
Россия, 198320, Санкт-Петербург, г. Красное Село, ул. Свободы, д. 52, лит. А, Б, Д.
Организация, принимающая претензии от потребителей
ООО «ЗМ Веритас».
Россия, 614107, Пермский край, г. Пермь, ул. Анри Барбюса, 54, оф. 004-006, 008.
Фосфатный буфер (PBS): обоснование, приготовление и использование
Содержание:
В фосфатный буфер, BPS или фосфатный буферный растворпредставляет собой буферный и изотонический раствор, функция которого заключается в поддержании pH и осмотического давления, максимально приближенных к естественной биологической среде (физиологическому). Аббревиатура PBS означает физиологический раствор с фосфатным буфером.
Между тем, контроль осмолярности очень важен, особенно при работе с живыми клетками, поскольку плазматические мембраны клеток реагируют в соответствии с концентрацией растворенных веществ, в которых они находятся.
Если клетки переносятся в гипертоническую среду, они становятся обезвоженными, поскольку водный градиент переносится в сторону, где концентрация растворенных веществ выше. Если, с другой стороны, клетки помещают в гипотоническую среду, клетки будут поглощать жидкость до тех пор, пока они не будут лизированы.
Вот почему буфер PBS используется для лабораторных протоколов, требующих обслуживания клеток. in vitro, таким образом клетки не будут повреждены.
PBS состоит из комбинации солей, таких как хлорид натрия, фосфат натрия, хлорид калия и фосфат калия. Состав PBS может варьироваться в зависимости от протокола.
Основа
В основном функция фосфатного буфера заключается в поддержании постоянного физиологического pH вместе с концентрацией электролита, аналогичной той, которая обнаруживается внутри тела.
В этой среде клетки могут оставаться стабильными, так как физиологические условия максимально имитируются.
При необходимости к исходному составу PBS могут быть добавлены другие соединения, например добавление EDTA к буферу полезно для промывания эритроцитов в тесте на перекрестную несовместимость.
EDTA предотвращает расщепление и лизирование фракции комплемента C1, присутствующей в сыворотке, в эритроциты, то есть позволяет избежать ложных результатов несовместимости. Кроме того, ЭДТА помогает диссоциировать клетки.
Подготовка
Количество солей, которое необходимо взвесить для приготовления физиологического раствора с фосфатным буфером, будет зависеть от количества, которое необходимо приготовить:
-Фосфатно-солевой буферный раствор (10X PBS)
На один литр раствора:
Техника подготовки
Поместите тяжелые соли в стакан, добавьте достаточное количество воды (80%) и перемешайте на перемешивающей пластине с помощью магнитной планки, пока соли не растворятся.
Фильтр для удаления нерастворенных частиц. Используйте фильтры с размером пор 0,45 мкм. Автоклав и асептическое распределение в колпаке с ламинарным потоком в стеклянных банках с крышками.
10-кратный раствор (концентрированный) не регулирует pH. Регулировку проводят после разбавления до концентрации буфера 1X PBS (разведение 1:10).
-Буферный фосфатный солевой раствор (1X PBS)
1X PBS можно приготовить непосредственно, взвесив соответствующее количество каждой соли, или его можно приготовить путем разбавления исходного раствора (1:10) стерильной дистиллированной водой.
-Чтобы приготовить один литр физиологического раствора с фосфатным буфером 1X PBS, взвесьте:
Техника подготовки
Действуйте, как описано в концентрированном растворе. Впоследствии необходимо отрегулировать pH. Для этого измерьте pH и, в зависимости от результата, используйте кислоту (HCl) или основание (NaOH), чтобы понизить или повысить pH, соответственно, до 7,4.
Кислота или основание добавляются по каплям, а значение pH раствора контролируется с помощью pH-метра. Отфильтруйте, автоклавируйте и асептически разложите по коническим пробиркам или сосудам по мере необходимости.
-Чтобы приготовить 1X PBS из 10X исходного раствора:
Сделайте раствор 1:10. Например, чтобы приготовить 1 литр 1X PBS, отмерьте 100 мл исходного раствора и добавьте 700 мл стерильной дистиллированной воды. Отрегулируйте pH и залейте количество воды до 1000 мл.
Приготовленный буфер PBS бесцветный и прозрачный.
Растворы для регулирования pH
HCl
На 100 мл 1 молярной HCl (соляной кислоты).
Отмерьте 91 мл дистиллированной воды и поместите его в стакан на 250 мл.
Отмерьте 8,62 мл концентрированной HCl и медленно добавьте ее в стакан с водой (никогда не делайте наоборот). При работе с сильными кислотами (высококоррозионными веществами) примите соответствующие меры биологической безопасности.
Перемешивайте в течение 5 минут, предпочтительно используя пластину для перемешивания с магнитной полосой внутри стакана. Перенести в баллон 100 мл и довести до 100 мл с помощью H2Или дистиллированный.
NaOH
На 100 мл NaOH (гидроксид натрия) 10 моль.
Отмерьте 40 мл дистиллированной воды и поместите ее в стакан на 250 мл. Отмерьте 40 г NaOH и добавьте в воду. Перемешайте, используя пластину для перемешивания с магнитной полосой внутри стакана.
Перенести в мерную колбу на 100 мл и долить до метки дистиллированной водой. Соблюдайте правила биобезопасности, поскольку эта реакция является экзотермической (она выделяет энергию в виде тепла).
Если вы хотите приготовить другое количество фосфатно-солевого раствора, вы можете обратиться к следующей таблице:
Приложения
Он в основном используется в клеточной биологии, иммунологии, иммуногистохимии, бактериологии, вирусологии и исследовательских лабораториях.
Он идеально подходит для промывки клеток центрифугами (эритроцитов), промывки монослоев клеток, методов спектроскопической эллипсометрии, количественного определения бактериальных биопленок, поддержания культур клеток на вирусы, в качестве промывочного раствора в методе непрямой иммунофлуоресценции. и в методах характеристики моноклональных антител.
Он также служит для транспортировки клеток или тканей, в качестве разбавителя для подсчета клеток, приготовления клеточных ферментов (трипсина), в качестве разбавителя для метода осушения биомолекул и для приготовления других реагентов.
С другой стороны, Мартин и др. В 2006 году продемонстрировали, что PBS можно использовать в лабораториях судебной экспертизы, в частности, при извлечении сперматозоидов из вагинальных мазков или вагинальных клеток из мазков полового члена. Таким образом можно установить, были ли сексуальные отношения.
Ограничения
-Некоторые буферы PBS содержат в качестве консерванта вещество, называемое азидом натрия. Это соединение может образовывать взрывчатые вещества при контакте со свинцом или медью. По этой причине следует соблюдать особую осторожность при сливе этого реагента в канализацию. Если его выбрасывают таким образом, необходимо добавить много воды, чтобы максимально разбавить его.
-Цинк не следует добавлять в фосфатный буфер, так как он вызывает выпадение в осадок некоторых солей.
-Ванген и его коллеги в 2018 году определили, что использование PBS не подходит для отмывки первичных клеток острого миелоидного лейкоза (AML), выделенных из периферической крови, из-за того, что многие клетки теряются в результате лизиса, с большим уменьшением количества материала. белок.
Поэтому они определили, что первичные клетки AML не следует мыть PBS после хранения в жидком азоте.
Фосфатно солевой буфер для чего
Организм можно определить как физико-химическую систему, существующую в окружающей среде в стационарном состоянии. Для обеспечения стационарного состояния у всех организмов выработались разнообразные анатомические, физиологические и поведенческие приспособления, служащие одной цели – сохранению постоянства внутренней среды. Это относительное динамическое постоянство внутренней среды (крови, лимфы, тканевой жидкости) и устойчивость основных физиологических функций организма человека и животных называется гомеостазом.
Этот процесс осуществляется преимущественно деятельностью лёгких и почек за счёт дыхательной и выделительной функции. В основе гомеостаза лежит сохранение кислотно-основного баланса. Для нормальной жизнедеятельности большинства клеток необходимы достаточно узкие пределы рН (6,9 – 7,8), и организм вынужден постоянно осуществлять нейтрализацию образующихся кислот. Этот процесс выполняют буферные системы, которые связывают избыток ионов водорода и контролируют их дальнейшие перемещения в организме. Буферные системы играют очень важную роль, т.к. в результате различных метаболических процессов в организме постоянно образуются различные кислоты, которые сразу же нейтрализуются буферными системами: гидрокарбонатной, фосфатной, белковой и гемоглобиновой.
Главной буферной системой организма является гидрокарбонатный буфер, состоящий из Н2СО3 и NaHCО3. При рН около 7,4 в организме преобладает гидрокарбонат-ион, и его концентрация может в 20 раз превышать концентрацию угольной кислоты. По своей природе угольная кислота очень нестойкая и сразу же после образования расщепляется на углекислый газ и воду. Реакции образования и последующего быстрого расщепления угольной кислоты в организме настолько совершенны, что им часто не придают особого значения. Эти реакции катализируется ферментом карбоангидразой, который находится в эритроцитах и в почках. Особенность гидрокарбонатной буферной системы состоит в том, что она открыта. Избыток ионов водорода связывается с гидрокарбонат-ионом, образующийся при этом углекислый газ стимулирует дыхательный центр, вентиляция лёгких повышается, а излишки углекислого газа удаляются при дыхании. Так в организме поддерживается баланс рН. Чем больше в клетках образуется ионов водорода, тем больше расход буфера. На этом этапе метаболизма подключаются почки, которые выводят избыток ионов водорода, и количество гидрокарбоната в организме восстанавливается.
Фосфатный буфер может действовать как в составе органических молекул, так и в качестве свободных ионов. Одна его молекула способна связывать до трёх катионов водорода. Белки могут присоединять к своей полипептидной цепочке как кислотные, так и основные группы.
Буферная ёмкость белковой буферной системы может охватывать широкий диапазон рН. В зависимости от имеющейся величины рН она может связывать как гидроксильные группы, так и ионы водорода. Третья часть буферной ёмкости крови приходится на гемоглобин. Каждая молекула гемоглобина может нейтрализовать несколько ионов водорода. Когда кислород переходит из гемоглобина в ткани, способность гемоглобина связывать ионы водорода возрастает и наоборот: когда в лёгких происходит оксигенация гемоглобина, он теряет присоединённые ионы водорода. Освободившиеся ионы водорода реагируют с гидрокарбонатом, и в результате образуется углекислый газ и вода. Образовавшийся углекислый газ удаляется из лёгких при дыхании.
Буферные свойства гемоглобина обусловлены соотношением восстановленного гемоглобина (ННb) и его калиевой соли (КНb). В слабощелочных растворах, каким является кровь, гемоглобин и оксигемоглобин имеют свойства кислот и являются донорами Н+ или К+. Эта система может функционировать самостоятельно, но в организме она тесно связана с гидрокарбонатной. Когда кровь находится в тканевых капиллярах, откуда поступают кислые продукты, гемоглобин выполняет функции основания: КНb + Н2СО3 ↔ ННb + КНСО3. В легких гемоглобин, напротив, ведет себя, как кислота, предотвращая защелачивание крови после выделения углекислоты.
Таким образом, механизм регуляции кислотно-основного равновесия крови в целостном организме заключается в совместном действии внешнего дыхания, кровообращения, выделения и буферных систем.