Эритроидный росток сужен что значит
Эритроидный росток сужен что значит
На основании общеклинического анализа крови сложно дать оценку состояния гемопоэза. Более полное представление дает изучение костного мозга (цитологическое, цитохимическое и др.).
Цитологический анализ костного мозга играет большую роль в диагностике заболеваний кроветворной системы. Подсчет миелограммы дает представление о характере эритропоэза (нормобластический или мегалобластический), позволяет обнаружить клетки, характерные для различных заболеваний системы крови (множественной миеломы, острых лейкозов, хронического миелолейкоза, хронического лимфолейкоза, лейкемизированных неходжкинских лимфом, болезни Гоше, Ниманна-Пика, метастазов рака в костном мозге и др.).
Данные миелограммы необходимы для проведения дифференциального диагноза с лейкемоидными реакциями. Сопоставление данных костномозгового кроветворения с картиной периферической крови и клинической симптоматикой позволяет уточнить причину анемии.
Имеются абсолютные и относительные показания к стернальной пункции.
Абсолютные показания: все анемии (кроме типичной железодефицитной), различные цитопении (одноростковая, двуростковая, панцитопения), острые лейкозы, хронические лейкозы в начальной стадии (для подтверждения диагноза и исключения лейкемоидных реакций), выраженное изолированное увеличение СОЭ (для исключения множественной миеломы и макроглобулинемии Вальденстрема), подозрение на метастазы злокачественной опухоли в костном мозге.
Относительные показания: железодефицитные анемии, хронические лейкозы в развернутой стадии.
Аспирационная биопсия костного мозга является технически простым, безопасным и легкодоступным методом. Наиболее часто используется стернальная пункция, предложенная в 1927 г. М. И. Аринкиным и впервые выполненная на кафедре факультетской терапии Военно-медицинской академии. При необходимости можно пунктировать гребень или бугристость подвздошной кости, у детей — пяточную кость. Пункция грудины выполняется иглой И. А. Кассирского с предохранительным щитком. После взятия аспирата костного мозга производят подсчет количества миелокариоцитов, мегакариоцитов, ретикулоцитов, готовят мазки для подсчета миелограммы.
Нормальная миелограмма
| Показатели миелограммы | Среднее значение (%) | Пределы колебаний (%) |
| Ретикулярные клетки | 0,9 | 0,1-1,6 |
| Недифференцированные бласты | 0,6 | 0,1-1,1 |
| Миелобласты | 1,0 | 0,2-1,7 |
| Промиелоциты | 2,5 | 1,0-4,1 |
| Миелоциты нейтрофильные | 9,6 | 7,0-12,2 |
| Метамиелоциты нейтрофильные | 11,5 | 8,0-15,0 |
| Палочкоядерные нейтрофилы | 18,2 | 12,8-23,7 |
| Сегментоядерные нейтрофилы | 18,6 | 13,1-24,1 |
| Всего клеток нейтрофильного ряда | 60,8 | 52,7-68,9 |
| Миелоциты эозинофильные | 0,1 | 0,0-0,2 |
| Метамиелоциты эозинофильные | 0,2 | 0,1-0,4 |
| Эозинофилы | 2,8 | 0,4-5,2 |
| Всего клеток эозинофилъного ряда | 3,2 | 0,5-5,8 |
| Миелоциты базофильные | 0,1 | 0-0,3 |
| Базофилы | 0,1 | 0-0,3 |
| Всего клеток базофильного ряда | 0,2 | 0-0,5 |
| Лимфобласты | 0,1 | 0-0,2 |
| Пролимфоциты | 0,1 | 0-0,2 |
| Лимфоциты | 8,8 | 4,3-13,3 |
| Всего клеток лимфоидного ряда | 9,0 | 4,3-13,7 |
| Монобласты | 0,1 | 0-0,2 |
| Моноциты | 1,9 | 0,7-3,1 |
| Плазмобласты | 0,1 | 0-0,2 |
| Проплазмоциты | 0,1 | 0,1-0,2 |
| Плазматические клетки | 0,9 | 0,1-1,8 |
| Эритробласты | 0,6 | 0,2-1,1 |
| Нормобласты базофильные | 3,6 | 1,4-5,8 |
| Нормобласты полихроматофильные | 12,9 | 8,9-16,9 |
| Нормобласты оксифильные | 3,2 | 0,8-5,6 |
| Всего клеток эритроидного ряда | 20,5 | 14,5-26,5 |
| Мегакариоциты | 0,4 | 0,2-0,6 |
Миелокариоциты миелограммы. У здоровых людей количество миелокариоцитов (всех ядросодержащих клеток костного мозга) в камере Горяева составляет 50-250•10 9 /л.
Мегакариоциты миелограммы. Нормальное количество мегакариоцитов в камере Фукса-Розенталя составляет 0,05-0,1•10 6 /л. Необходимо также определять количество мегакариоцитов в окрашенных мазках в 250 полях зрения под малым увеличением и при подсчете миелограммы в процентах.
Следует помнить, что снижение уровня миелокариоцитов и мегакариоцитов в миелограмме отмечается также при разведении аспирата периферической кровью (технические погрешности при выполнении стернальной пункции).
Ретикулоциты миелограммы. Нормальное количество ретикулоцитов в костном мозге составляет 20-30%о. Увеличение их числа наблюдается при гемолитических и постгеморрагических анемиях.
Морфологический анализ клеток костного мозга (подсчет миелограммы) производят на 500 клеток костного мозга, после чего вычисляют процентное содержание каждого вида клеток.
При анализе миелограммы необходимо оценить клеточность костного мозга (нормо-, гипо- или гиперклеточный), дать качественную характеристику всех клеточных рядов с определением индексов созревания, лейкоэритробластического соотношения, характера эритропоэза (нормобластический, мегалобластический или с мегалобластоидными чертами) и количества митозов. Отдельно следует оценить мегакариоцитопоэз (количество и функция мегакариоцитов).
Костномозговой индекс созревания нейтрофилов определяется по формуле: (промиелоциты + миелоциты + метамиелоциты)/ (палочкоядерные + сегментоядерные нейтрофилы)
В норме костномозговой индекс созревания нейтрофилов равен 0,6-0,8.
Индекс созревания эритроидных клеток определяется по формуле: (полихроматофильные + оксифильные нормоциты)/(эритробласты + базофильные + полихроматофильные + оксифильные нормоциты)
В норме индекс созревания эритроидных клеток равен 0,8-0,9.
Уменьшение индекса свидетельствует о задержке гемоглобинизации и/или преобладании молодых базофильных нормоцитов, дает возможность ориентировочно оценить запасы и обмен железа в организме.
Лейкоэритробластическое соотношение определяется по формуле: (гранулоциты): (ядросодержащие клетки эритроидного ряда) и в норме составляет 3-4:1.
Количество митозов в норме составляет 3,5 на 1000 для клеток гранулоцитарного ряда и 5 на 1000 — для клеток эритроидного ряда.
Заключение по миелограмме не должно быть категоричным, поскольку для постановки диагноза необходимо учитывать клинические данные и показатели периферической крови.
Для более полной характеристики гемопоэза, особенно мегакариоцитопоэза, в ряде случаев требуется гистологическое исследование костного мозга методом трепанобиопсии.
Определение сидеробластов и сидероцитов в миелограмме
При железодефицитных и сидеробластных анемиях важно определять количество сидероцитов и сидеробластов — эритроцитов и эритробластов, содержащих в цитоплазме железо в виде гемосидерина и ферритина (зернышки синего цвета при окраске по Перлсу диаметром 0,2-1,5 мкм). У здоровых людей в периферической крови содержится 1,1-3,0% (в среднем 1,6%) сидероцитов. Содержание сидеробластов в костном мозге составляет 15-40% от всех клеток эритроидного ряда; количество гранул в них обычно 1-2 (не более 4).
Клиническое значение. При хронических железодефицитных анемиях отмечается снижение количества сидероцитов и сидеробластов в костном мозге, гранулы железа в них практически выявить не удается.
Увеличение количества сидеробластов с большим количеством гранул железа в каждом из них, появление кольцевых форм сидеробластов наблюдается при наследственных и приобретенных сидеробластных анемиях (интоксикация свинцом, один из вариантов миелодиспластического синдрома — рефрактерная анемия с кольцевыми сидеробластами).
Наряду с исследованием крови и костного мозга для диагностики специфических поражений и осложнений проводимой терапии в ряде случаев необходим анализ биологических жидкостей (мочи, кала, мокроты, экссудатов, ликвора).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Диагностика и лечение хронической аутоиммунной гемолитической анемии
Больная Ш., 80 лет, пенсионерка. Из анамнеза известно, что в течение последних двух лет неоднократно проходила амбулаторное и стационарное лечение по поводу хронической B12–фолиеводефицитной анемии, диагностированной на основании анемического синдрома в сочетании с гиперхромией и макроцитозом эритроцитов. Стернальная пункция, определение уровня витамина B12 и фолиевой кислоты не проводились. Отмечался временный незначительный положительный эффект лечения витамином B12. С конца 2011 года, несмотря на ежемесячное введение витамина B12 в дозе 500γ в сочетании с фолиевой кислотой, стала нарастать анемия (14.02.2012 г. гемоглобин – 54 г/л). Для обследования и лечения госпитализирована в больницу № 40 с диагнозом: B12–фолиеводефицитная анемия тяжелой степени. ИБС. Стенокардия напряжения II ф. к. Гипертоническая болезнь II ст. Желчнокаменная болезнь. Хронический калькулезный холецистит. Мочекаменная болезнь. Конкремент правой почки, простые кисты обеих почек. Полипы желудка.
При поступлении жалобы на выраженную общую слабость, головокружения, головную боль, учащенное сердцебиение, перебои в работе сердца.
При объективном осмотре отмечены субиктеричность кожи и слизистых оболочек, умеренная гепатомегалия (+2 см) и спленомегалия (+ 2 см).
Результаты клинического анализа в динамике представлены в таблице 1.
Таблица 1. Клинические анализы крови пациентки Ш. в динамике
 |  |  | 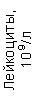 | 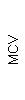 | 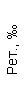 |  | 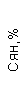 | 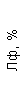 | 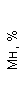 | 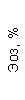 | 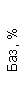 | 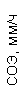 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 15.02.12 | 54 | 1.39 | 10.5 | 133 | 80 | 2 | 66 | 21 | 9 | 2 | — | 75 |
| 11.03.12 | 50 | 1.41 | 11.8 | 114 | 98 | 4 | 75 | 11 | 4 | 3 | 1 | 78 |
| 15.03.12 | 49 | 1.31 | 17.8 | 121 | 288 | 4* | 60 | 23 | 5 | 1 | — | 78 |
| 20.03.12 | 72 | 1.93 | 11.4 | 116 | 297 | 2 | 73 | 14 | 7 | 2 | 0 | 46 |
| 27.03.12 | 66 | 1.9 | 11 | 108 | 202 | 2 | 60 | 26 | 7 | 3 | 0 | 40 |
| 12.04.12 | 70 | 1.75 | 1.9 | 112 | 104 | 3 | 62 | 24 | 11 | 0 | 0 | 27 |
| 26.04.12 | 93 | 2.56 | 5.7 | 109 | 148 | 3 | 74 | 13 | 9 | 0 | 0 | 11 |
| 24.06.12 | 111 | 3.42 | 4.7 | 97 | 7 | 2 | 69 | 21 | 10 | 0 | 1 | 15 |
| 16.08.12 | 120 | 3.97 | 5.8 | 93 | 12 | — | 71 | 19 | 9 | 1 | 0 | 40 |
Примечание: * в лейкоцитарной формуле 15.03.12 выявлялись также миелоциты (2%) и метамиелоциты (5%).
В биохимическом анализе крови – повышение уровня креатинина (189 ммоль/л), билирубина (58 ммоль/л) за счет непрямого билирубина.
УЗИ органов брюшной полости: гепатоспленомегалия; камни желчного пузыря; диффузные изменения поджелудочной железы; простые кисты обеих почек, конкремент правой почки.
ФГДС: два полипа желудка размером до 0,5 см.
Учитывая высокий риск сердечно-сосудистых осложнений у пожилой пациентки с анемией тяжелой степени, проведены трансфузии эритроцитарной взвеси. На основании клинико-лабораторных данных (спленомегалия, гипербилирубинемия, гиперхромная анемия с ретикулоцитозом) и неэффективности лечения витамином B12 и фолиевой кислотой заподозрена гемолитическая анемия.
При исследовании крови на антиэритроцитарные антитела выявлены аутоантитела класса IgG ++++.
Результаты стернальной пункции представлены в таблице 2.
Таблица 2.Миелограмма пациентки Ш. от 17.02.12 г.
Заключение
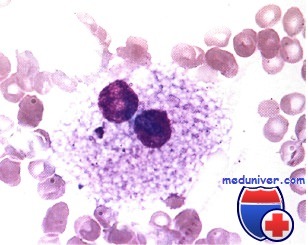
Клеточный костномозговой пунктат. Эритропоэз – нормобластический. Гиперплазия эритроидного ростка – 74,8%. Со стороны эритрокариоцитов отмечаются клетки с цитоплазматическими мостиками, скопления в виде «эритроидных островков».
Мегакариоциты различной степени зрелости с умеренным тромбоцитообразованием.
На основании данных миелограммы (гиперплазия эритроидного ростка при нормобластическом типе кроветворения) и выявления антиэритроцитарных антител диагностирована аутоимунная гемолитическая анемия с тепловыми антителами. При дополнительном обследовании признаков вторичного характера анемии не выявлено.
С 11.03.12 г. начата пульс-терапия метипреднизолоном в дозе 500 мг 1 раз в день внутривенно в сочетании с пероральным приемом преднизолона в дозе 45 мг в сутки под прикрытием гастропротекторов. После 5 дней лечения анемический синдром продолжал нарастать, появился выраженный сдвиг лейкоцитарной формулы влево, увеличение количества ретикулоцитов (табл.1). Доза преднизолона перорально увеличена до 75 мг в сутки, к лечению добавлен азатиоприн по 100 мг/сутки per os, проведена трансфузия1 дозы эритроцитарной взвеси.
С 20.03.12 г. с учетом сохраняющегося гемолиза (ретикулоциты 297‰) проведен второй курс пульс-терапии метилпреднизолоном в дозе 500 мг в сутки № 4, однократно введен внутривенно циклофосфан в дозе 600 мг.
Лечение больная переносила хорошо. С 27.03.12 г. отмечена тенденция к увеличению уровня гемоглобина без поддерживающих гемотрансфузий. Решено продолжить введение циклофосфана по 200 мг в сутки, отменить азатиоприн. Анемический синдром продолжал уменьшаться: к 12.04.12 г. уровень гемоглобина достиг 70 г/л, снизился гемолиз (ретикулоцитов 104‰), однако развилась лейкопения (1,9×10 9 /л), в связи с чем циклофосфан был временно отменен. После восстановления количества лейкоцитов лечение циклофосфаном по 200 мг дважды в неделю было возобновлено на фоне постепенного снижения дозы преднизолона.
Больная в удовлетворительном состоянии 28.04.12 г. выписана из стационара. На амбулаторном этапе продолжено введение циклофосфана по 200 мг в сутки 2 раза в неделю, преднизолон в течение месяца полностью отменен.
В течение нескольких месяцев получала поддерживающую терапию циклофосфаном по 200 мг в сутки 2 раза в неделю (суммарная доза составила 7200 мг). На этом фоне уровень гемоглобина стабилен в пределах 100–120 г/л, количество ретикулоцитов не превышает 20%.
Комментарий к клиническому случаю
Аутоиммунная гемолитическая анемия (АИГА) – гетерогенная группа заболеваний и синдромов, обусловленных повышенным разрушением эритроцитов вследствие образования аутоантител. Частота АИГА во всех возрастных группах составляет 1:40000 – 1:80000, причем женщины болеют в 2 раза чаще мужчин. Выделяют первичные (идиопатические) и вторичные АИГА, которые чаще всего развиваются при лимфомах, солидных опухолях и заболеваниях соединительной ткани. По серологическим свойствам различают АИГА с тепловыми (85%) и холодовыми (15%) антителами; по месту разрушения эритроцитов выделяют АИГА с внутриклеточным (наиболее частым), внутрисосудистым и смешанным гемолизом.
Клинические проявления АИГА:
При внутрисосудистом гемолизе моча приобретает темно-бурую или черную окраску.
Лабораторные критерии:
Стандарт первой линии терапии АИГА – пероральные глюкокортикостероиды в начальной дозе 1 мг/кг в сутки, возможно проведение пульс-терапии метилпреднизолоном в дозе 0,5–1,0 г/сутки внутривенно в течение 3-5 дней. Второй линией терапии является спленэктомия, которая используется при отсутствии эффекта глюкокортикостероидов в течение 4–6 месяцев. У пожилых пациентов показано назначение иммунодепрессивных и цитостатических препаратов (азатипоприн, циклофосфон, циклоспорин). Значительно реже используют моноклональные антитела (ритуксимаб) и иммуноглобулин. Выживаемость больных АИГА в течение 5 лет составляет 75%.
При анализе данного случая обращает внимание длительное латентное течение заболевания у больной преклонного возраста с гиперхромной анемией, что послужило причиной ошибочного диагноза B12–дефицитной анемии (для АИГА характерен нормохромный характер анемии). С учетом возраста пациентки и наличия сопутствующих заболеваний было принято решение о подключении к лечению цитостатической терапии, позволившее получить ремиссию заболевания, отменить глюкокортикостероиды и отказаться от проведения спленэктомии.
Эритроидный росток сужен что значит
Установление диагноза миелодиспластических синдромов (МДС) основывается на выявлении диспластических изменений одного или нескольких ростков гемопоэза. Морфологические изменения клеток эритро-, гранулоцито- и мегакариоцитопоэза в костном мозге и крови очень разнообразны, соотношение нормальных и диспластических элементов у разных больных существенно варьирует. Принято считать клеточную линию измененной, если число диспластических элементов в ней составляет более 10 %.
Для подтверждения клональности процесса и прогнозирования течения заболевания диагностика миелодиспластических синдромов (МДС) должна непременно включать цитогенетическое исследование клеток костного мозга, особенно при незначительном числе гемопоэтических клеток с признаками дисплазии или отсутствии цитопении.
Нарушения эритропоэза при миелодиспластических синдромах. Анемия — наиболее частая патология кроветворения, наблюдаемая у большинства пациентов. Как показали собственные исследования (82 больных первичными миелодиспластическими синдромами (МДС)), анемия была диагностирована у 95,2 % пациентов: наиболее часто — в составе панцитопении (47,6 %), только в сочетании с лейкопенией — 15,9 % и тромбоцитопенией — 17,1 %. Изолированная анемия обнаруживалась у 14,6 % больных. По данным другого отечественного исследования (71 больной первичным МДС), одноростковая цитопения определялась у 33,9 % больных, двухростковая — у 40,8 %, панцитопения выявлялась наиболее редко — у 25 %.
Обычно анемия носит макро- или нормоцитарный характер. В редких наблюдениях описана микроцитарная анемия, выражающаяся в преобладании микроцитов в общей популяции эритроцитов. По данным нашего исследования, наиболее часто отмечалась макроцитарная анемия (53 %), несколько реже — нормоцитарная (44 %). Микроцитарная анемия была выявлена только у 4 % пациентов.
Использование автоматических анализаторов крови позволяет точно измерить средний объем клеток и охарактеризовать распределение фракций по размеру в популяции эритроцитов. Увеличение среднего объема эритроцитов (MCV) более 100 фл свидетельствует о макроцитозе, уменьшение менее 85 фл — о микроцитозе. Показатель средней концентрации гемоглобина в эритроците (МСН) выше 31 пг свидетельствует о гиперхромном характере изменений, ниже 27 пг — о гипохромном.
В большинстве случаев у больных миелодиспластическими синдромами (МДС) констатируется нормохромная анемия. Следует отметить, что анемия у больных миелодиспластическими синдромами (МДС) может иметь смешанный характер и протекать на фоне хронической железодефицитной анемии, особенно у женщин, поэтому на основании данных автоматического анализатора анемия может быть квалифицирована как нормоили микроцитарная, а также нормо- или гипохромная. Только микроскопическое исследование мазков крови в этих случаях позволяет более точно охарактеризовать свойства эритроцитов.
Количество ретикулоцитов у больных миелодиспластическими синдромами (МДС) может колебаться достаточно широко, обычно их число нормальное или сниженное. Ретикулоцитоз может быть обусловлен появлением патологической фракции длительно живущих клеток (4 дня вместо 36 ч в норме), что позволяет обозначить этот процесс как «псевдоретикулоцитоз». В других случаях выраженность анемии при миелодиспластических синдромах (МДС) может усугубляться за счет продукции антиэритроцитарных антител и гемолиза эритроцитов, который сопровождается ретикулоцитозом. Аутоиммунный гемолиз с ретикулоцитозом определяют у 7—14 % больных, в связи с чем предложено выделять подвариант миелодиспластического синдрома с гемолитическим компонентом анемии.
Дисплазия эритроцитов выражается в изменении их формы, в частности, возникающем вследствие нарушения белков цитоскелета. В мазках крови выявляют пойкилоциты, овалоциты, эллиптоциты, стоматоциты и акантоциты. В литературе приводятся наблюдения о сфероцитозе эритроцитов, предшествовавшем развитию миелодиспластического синдрома. Для картины крови характерны также тельца Жолли, кольца Кеббота, базофильная пунктация цитоплазмы и ядросодержащие эритроциты. Подобные признаки не являются строго специфичными для миелодиспластического синдрома и могут быть обнаружены при различных других патологических состояниях.
Наличие нормоцитов в периферической крови наблюдается у 1/4— 1/3 больных миелодиспластическими синдромами (МДС). По нашим наблюдениям, нормоциты присутствуют у 26 % больных первичными миелодиспластическими синдромами (МДС), среднее количество нормоцитов составляет 1,7 ± 1,4 на 100 лейкоцитов.
Данные автоматических анализаторов и тщательное морфологическое исследование мазков являются важными условиями для правильной оценки количественных и качественных параметров красной крови.
В пунктате костного мозга определяется либо резкое уменьшение (до 5 % всех ядросодержащих клеток), либо расширение (до 90 %) красного ростка. Наиболее частым признаком дизэритропоэза является его мегалобластоидный характер, наблюдаемый почти у 90 % больных. В этих случаях определяются макронормобласты как с базофильной окраской цитоплазмы, так и с оксифильной. Встречаются многоядерные формы нормобластов и клетки с цитоплазматической перемычкой. Цитоплазма клеток окрашена неравномерно, включает тельца Жолли и имеет неправильные очертания. Ядра дольчатые, фрагментированные, клетки соединяются ядерными мостиками вследствие нарушенного митоза. Встречаются двух- и многоядерные формы. Структура хроматина — разреженная.
При цитохимическом исследовании реакции Перлса в части случаев в нормобластах определяют резкое увеличение числа (более 10) сидерофильных гранул, расположенных венчиком вокруг ядра. Они представляют собой митохондрии с избыточным накоплением железа. Такие клетки обозначаются как кольцевые сидеробласты. В отдельных работах имеются указания на то, что сидеробластоз при миелодиспластическх синдромах (МДС) может ассоциироваться с редко встречающимся микроцитарным характером анемии].
Нарушение строения органелл эритроцитов сопровождается образованием патологических форм гемоглобина. В литературных источниках указывается, что HbF обнаруживается у 87,5 % пациентов РА, причем преимущественно в эритробластах (F-бластах), но не в эритроцитах, что свидетельствует, по мнению авторов, о неспособности эритробластов к нормальной дифференцировке.
Диспластические нарушения клеток эритроидного ростка включают изменения энзимного спектра клеток. Снижается активность ферментов гликолиза, повышается содержание а-нафтилацетатэстеразы и кислой фосфатазы в нормобластах и эритроцитах. В части случаев наблюдается увеличение содержания ШИК-положительного вещества в диффузной и гранулярной форме. Однако эти цитохимические особенности не являются специфичными для миелодиспластических синдромов (МДС) и могут быть обнаружены при других гемобластозах.
Представляют интерес наблюдения миелодиспластических синдромов (МДС), при которых в клетках эритроидного ростка обнаружены ферменты, характерные только для нейтрофилов. Так, в нормобластах костного мозга цитохимическим методом обнаружена щелочная фосфатаза, а электронно-микроскопическим — пероксидаза. По нашим данным, щелочная фосфатаза в нормобластах присутствует у 69 % больных миелодиспластическими синдромами, число ферментсодержащих клеток составляет 2—63 %. Указанные цитохимические особенности эритроидных предшественников выявляются при любых вариантах заболевания и свидетельствуют о глубоких нарушениях процесса дифференцировки.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021